【BJH】双靶点CAR-T的四种策略及其优缺点
2024-02-22 聊聊血液 聊聊血液 发表于上海
CAR-T细胞疗法在多种血液系统恶性肿瘤的治疗中显示出巨大的希望,包括非霍奇金淋巴瘤(NHL)和急性淋巴细胞白血病(ALL),但原发性难治性或复发性疾病是一个相对常见的现象。
CAR-T细胞疗法在多种血液系统恶性肿瘤的治疗中显示出巨大的希望,包括非霍奇金淋巴瘤(NHL)和急性淋巴细胞白血病(ALL),但原发性难治性或复发性疾病是一个相对常见的现象。失败的原因很复杂,可能包括T细胞功能障碍、肿瘤微环境(TME)引起的免疫抑制、高肿瘤负荷和抗原逃逸等。

其中抗原逃逸(靶抗原表达缺失或下调)是侵袭性B细胞恶性肿瘤患者耐药的主要机制,其机制也有多种,包括选择预先存在的抗原阴性克隆、抗原表达减少、获得突变、剪接位点变异、谱系转换介导的抗原丢失(通常发生于有特定基因组异常[如KMT2A重排]的患者)和表面抗原呈递失败。当然,这些机制通常是同时发生的。
对于抗原逃逸,理论上可以通过给予靶向多抗原的多靶点CAR-T来克服这一机制,临床前数据也显示双靶点CAR-T细胞疗效优于单靶点CAR-T细胞,这些为具有两种或两种以上抗原特异性的产品(如CD19和CD20、CD19和CD22、CD19和BCMA等)的开发铺平了道路。
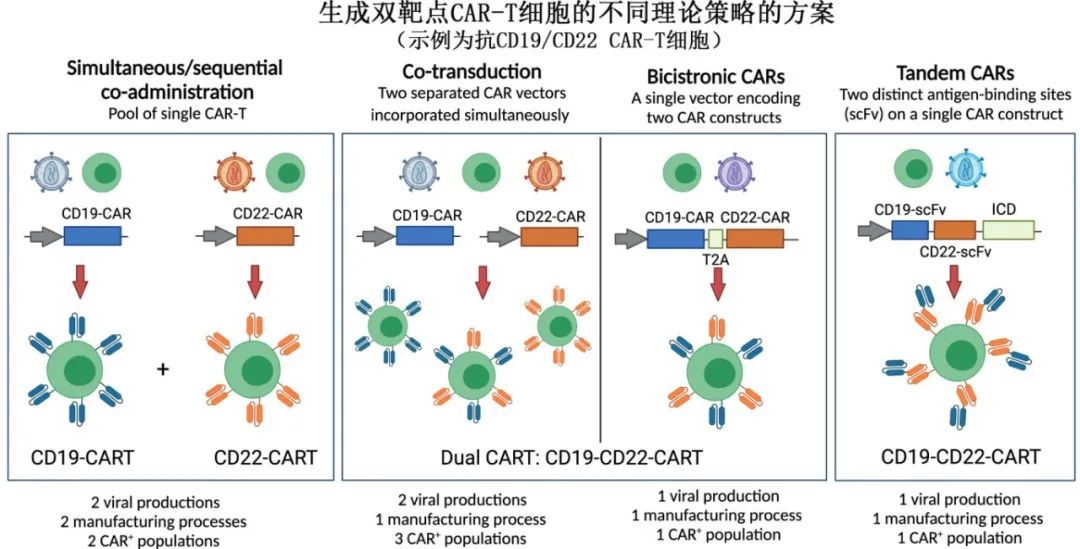
双靶点CAR-T细胞的治疗策略主要有如下四种:
•单靶点CAR-T细胞的联合给药:包括生产两种单独的CAR-T细胞产品,并在短时间内给药。
•共转导CAR-T细胞:将T 细胞共转导两个单独的病毒载体,每个载体编码不同的CAR。需要生产一次CAR-T 细胞产品,但包含两个单独的载体。
•双顺反子CAR-T细胞:使用编码两种不同 CAR 的单一载体生产一种 CAR-T 细胞产品。
•串联或环状CAR-T细胞:使用单一载体生产一种 CAR-T 细胞产品,该载体可编码具有两个不同单链可变片段 (scFv) 的单个 CAR。串联结构由一个 scFv 的 VL-VH 序列与第二个 scFv 的 VL-VH 序列直接连接组成(经典串联),而在环结构中,一个 scFv 的 VL 和 VH 序列被另一个 scFv 的 VL-VH 分离。
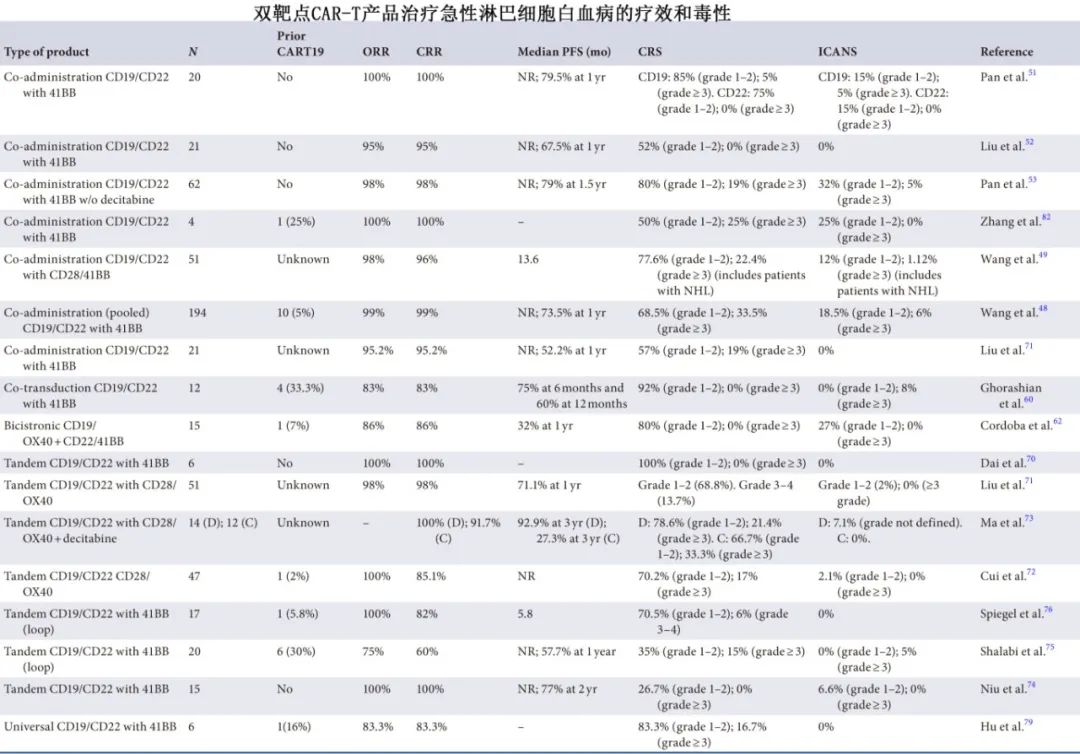
相关数据见下表,原文有部分研究的详细介绍(10.1111/ bjh.19348)。

事实上,四种策略均有自身的优缺点,具体如下。
单靶点CAR-T细胞的联合给药
合并或组合给予两种不同的CAR-T细胞产品是实现双靶点的最简单选择,特别是当两种CAR-T细胞产品都有成熟数据时,但它也是最昂贵的策略,因为每例患者需要两个完整且独立的制造流程。两种药物制成后,可混合使用并一起给药(一次输注)或单独给药(两次输注)。此外,两次给药可以几乎连续发生(即同一天或第二天),也可以相隔几个月。如果两次给药间隔太远,可重复进行清淋化疗。
共转导CAR-T细胞
共转导需要使用两种不同的病毒载体进行单细胞制造过程,虽然操作相对简单,但由于使用的是两种载体而非一种载体,因此比传统的CAR-T细胞制造成本更高,并且最终产品存在一定程度的异质性。此策略的关键特征在于,所得细胞产物含有以下四种细胞群的混合物:(i)具有一种抗原特异性的细胞;(ii)具有另一抗原特异性的细胞;(iii)具有两种抗原特异性的细胞;(iv)未转导的细胞。在共转导的CART细胞的制造过程中,由于CAR表达所需的细胞资源的竞争和/或其中一个细胞群的潜在优先扩增,存在着扭曲(skewed)转导和/或CAR群失衡的风险,而CAR群的不平衡可能会影响最佳双靶点的实现。与双顺反子盒(bicistronic cassette)相比,共转导通常可增强CAR表达,这是其优势之一。
双顺反子CAR-T细胞
在同一个 T 细胞中实现两个 CAR 双重表达的一个简单方法是使用包含双顺反子盒的单个载体。双顺反子载体包含两个基因,每个基因编码一个独特的CAR,由一个“自裂解”肽分隔,能够平行共表达两个独立的CAR,比例为1:1。
这种方法比联合给药或联合转导更简单、更便宜,因为每例患者只需要一个细胞产生和一个载体;且与共转导相比,双顺反子盒的产物更均一,因为所有转导的 T 细胞可在 T 细胞膜上表达两种CAR。但这些载体需要更长的序列来编码两个完整的 CAR 分子,可能损害病毒包装(packaging),降低转导效率和破坏 CAR 表达。
串联CAR-T细胞
串联 CAR 由编码具有两个配体结合结构域的嵌合受体的单个载体产生,具有很多优点。与双顺反子 CAR 相比,结构尺寸明显更小,能够实现更好的包装。此外,它只需要一个载体,双 CAR-T 细胞产物更均一,并防止一个 CAR 相对于另一个 CAR 的优势。其缺点在于,串联 CAR 的最佳设计尚不明确,可能因使用的scFv、靶向抗原的密度和靶向表位与 T 细胞膜的接近程度而异。很多参数都会影响 CAR 的效力,如 scFv 的顺序;每个 scFv 的 VH 和 VL 排列;VH和 VL 之间或两个 scFv 之间的连接体长度;连接体的刚性。因此需要复杂的结构优化,包括多个 CAR 结构的生成和实证测试。在靶向 CD22 时串联 CAR 优化尤为重要,CD22是一种低密度表达的抗原,高度糖基化,具有实质性的大小和刚性,可能损害免疫突触。
总结
尽管CART19细胞的出现显著改善了R/R ALL和NHL患者的预后,但仍有相当比例的患者复发和死于疾病进展。这一现状促使了大量旨在靶向多抗原(例如CD19和CD20或CD22)的新策略,旨在减轻抗原丢失或下调且不增加过度毒性。双靶点可以通过多种手段实现,包括从简单的两种不同产品的联合给药到更复杂的双顺反子盒或串联CAR的设计。到目前为止,没有确凿的证据表明这些新型产品具有显著不同的毒性特征,但也没有证据表明其中一种策略优于其他策略,甚至没有证据表明双靶点优于单靶点,但抗原丢失已部分减少。
部分双靶点产品已与表观遗传学药物(如地西他滨)或检查点抑制剂(如帕博利珠单抗和替雷利珠单抗)联用,显示出有前景的疗效,且不增加毒性。其他组合包括常规CD19 CART联合其他药物(如裸抗cd19单克隆抗体tafasitamab、双特异性单克隆抗体和抗体药物偶联物)。
双靶点CAR-T的缺陷可能包括:(i)未解决除抗原逃逸之外的其他耐药机制;(ii)大多数临床试验随访不足;(3)产品间异质性大,包括不同的额外靶点(CD20、CD22和其他);(iv)由于低传导效率和大尺寸的双顺反子和串联载体,导致需要复杂的制备优化。人们仍在寻找治疗B细胞恶性肿瘤的最佳产品和/或组合,但仍缺乏随机临床试验形式的明确证据(但这正是人们热切期待的)。
参考文献
Brillembourg H, Martínez-Cibrián N, Bachiller M, Alserawan L, Ortiz-Maldonado V, Guedan S, et al. The role of chimeric antigen receptor T cells targeting more than one antigen in the treatment of B-cell malignancies. Br J Haematol. 2024;00:1–11. https://doi.org/10.1111/ bjh.19348
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#CAR-T# #血液系统恶性肿瘤# #双靶点#
28