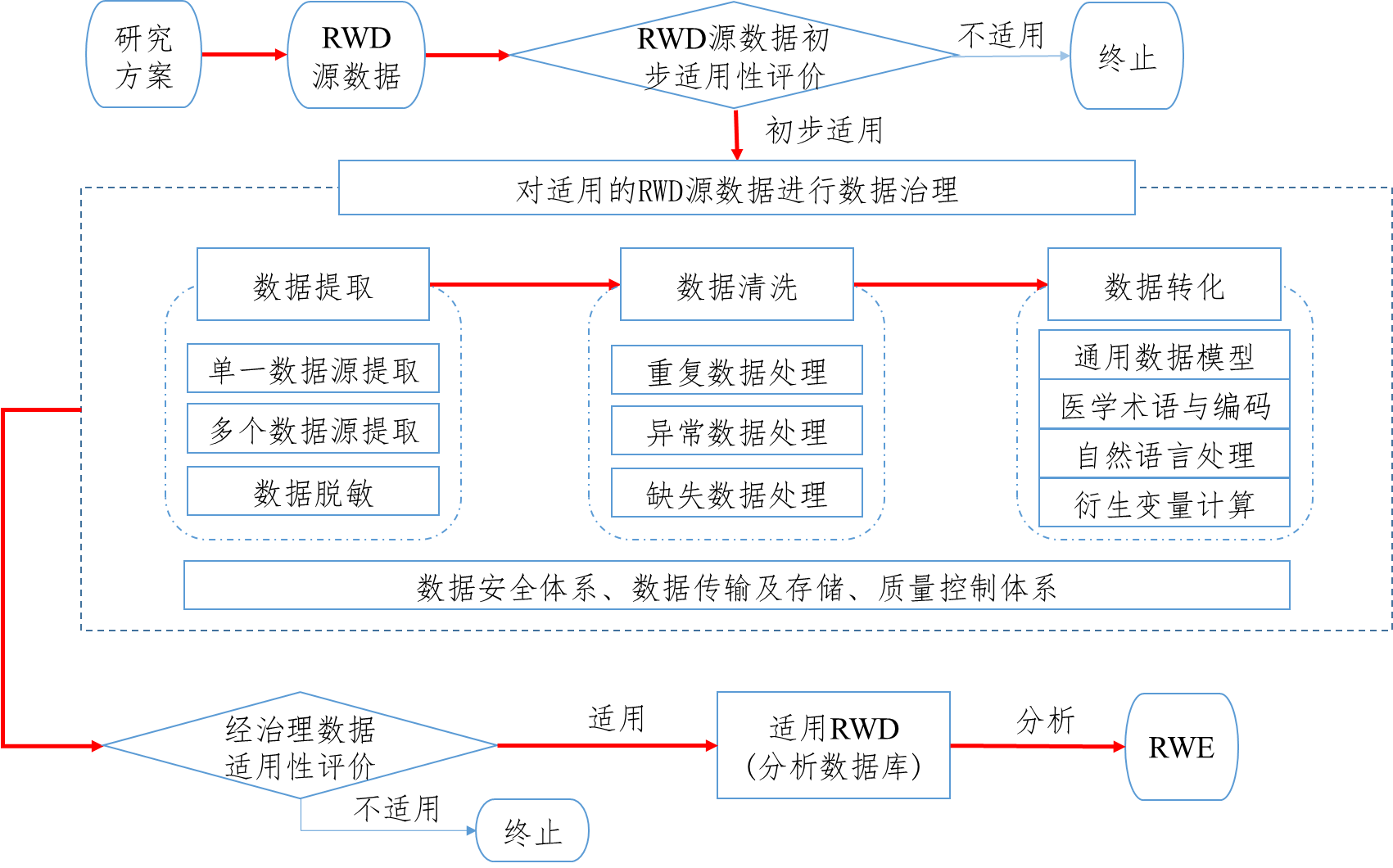
用于产生真实世界证据的真实世界数据指导原则(征求意见稿)
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,我中心组织起草了《用于产生真实世界证据的真实世界数据指导原则(征求意见稿)》,现在中心网站予以公示,以广泛听取各界意见和建议,欢迎
CDE - 真实世界证据,真实世界研究 - 2020-08-03
关于《基于疾病登记的真实世界数据应用指导原则(征求意见稿)》公开征求意见的通知
为了促进和规范基于疾病登记的真实世界数据应用,我中心组织起草了《基于疾病登记的真实世界数据应用指导原则(征求意见稿)》,现公开征求意见。欢迎各界提出宝贵意见和建议,并请及时反馈给我们。
国家药品监督管理局药品审评中心 - 真实世界数据,疾病登记 - 2023-11-24
真实世界证据支持药物研发? ——读真实世界证据支持药物研发征求意见稿的启示
真实世界研究、真实世界数据、真实世界证据、相信这三个名词我们的读者们都不陌生。真实世界这个概念近几年实在是太火了,以至于我们翻开一本期刊常常看到好几篇真实世界“冠名”的文章。今年五月二十九日药审中心发布了公开征求《真实世界证据支持药物研发的基本考虑》意见的通知(http://www.cde.org.cn/news.do?
临床流行病学和循证医学 - 药物研发 - 2019-10-08
关于《真实世界证据支持药物注册申请的沟通交流指导原则(征求意见稿)》公开征求意见的通知
为促进真实世界证据在药品注册申请中的应用实践,提高研发效率,针对申请人与审评机构开展真实世界证据支持注册申请的沟通交流给出具体要求和指导性建议,我中心组织起草了《真实世界证据支持药物注册申请的沟通交流
国家药品监督管理局药品审评中心 - 真实世界证据支持药物 - 2022-08-20
关于《药物真实世界研究设计与方案框架指导原则(征求意见稿)》公开征求意见的通知
为了指导申办者科学合理的设计真实世界研究,明确真实世界研究方案撰写的技术要求,我中心组织起草了《药物真实世界研究设计与方案框架指导原则(征求意见稿)》,现公开征求意见。
国家药品监督管理局药品审评中心 - 药物真实世界研究设计 - 2022-07-12
国家药监局药审中心关于发布《用于产生真实世界证据的真实世界数据指导原则(试行)》
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,药审中心组织制定了《用于产生真实世界证据的真实世界数据指导原则(试行)》(见附件)。
国家药品监督管理局药品审评中心 - 2021-04-15
真实世界证据支持药物研发的基本考虑(征求意见稿)
真实世界证据支持药物研发的基本考虑(征求意见稿)国家药品监督管理局药品审评中心2019年5月 一、 引言1.背景与目的随机对照临床试验(Randomized Controlled Trial,RCT)被认为是评价药物有效性的“金标准”,并为药物临床试验普遍采用。RCT严格控制试验入组与排除标准和其它条件,并进行随机化分组,因此能够最大限度地减少影响因果推断的因素,使得研究结论较为确定,所形成
CDE - 真实世界,药物研发 - 2019-05-29
《药物真实世界研究设计与方案框架指导原则(征求意见稿)》
为了指导申办者科学合理的设计真实世界研究,明确真实世界研究方案撰写的技术要求,我中心组织起草了《药物真实世界研究设计与方案框架指导原则(征求意见稿)》,现公开征求意见。欢迎各界提出宝贵意见和建议,并请
CDE - 真实世界研究 - 2022-07-08
CDE公开征求意见:儿童用药研究如何使用真实世界证据
5月18日,国家药监局药品审评中心发布通知,就《真实世界证据支持儿童药物研发与审评的技术指导原则(征求意见稿)》(以下简称指导原则)公开征求意见。征求意见时间为期一个月。
CDE - 儿童用药,真实世界证据 - 2020-05-19
用于产生真实世界证据的真实世界数据指导原则(征求意见稿)
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,我中心组织起草了《用于产生真实世界证据的真实世界数据指导原则(征求意见稿)》,现在中心网站予以公示,以广泛听取各界意见和建议,欢迎
CDE - 指导原则 - 2020-09-01
《用于产生真实世界证据的真实世界数据指导原则(试行)》
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,药审中心组织制定了《用于产生真实世界证据的真实世界数据指导原则(试行)》(见附件)。根据《国家药监局综合司关于印发药品
国家药品监督管理局药品审评中心 - 真实世界数据,真实世界研究 - 2021-04-15
药物真实世界研究设计与方案框架指导原则(征求意见稿)
为了指导申办者科学合理的设计真实世界研究,明确真实世界研究方案撰写的技术要求,我中心组织起草了《药物真实世界研究设计与方案框架指导原则(征求意见稿)》,现公开征求意见。欢迎各界提出宝贵意见和建议,并请
CDE - 真实世界研究 - 2022-07-08
【NMPA】公开征求《真实世界数据用于医疗器械临床评价技术指导原则》意见
各有关单位: 真实世界数据作为医疗器械临床评价可能的数据来源,因其具有数据资源丰富、研究结果的外推性可能较好、可获得长期临床结局数据等特点,日益受到监管机构、行业等各方重视。2019年4月国家药品监督管理局发布了中国药品监管科学行动计划,把“将真实世界数据用于医疗器械临床评价的方法学研究”列为首批研究项目,探索将真实世界数据用于监管决策的可行性和方法学,为医疗器械审评审批制度改革月国家药品监督管理局发布了中国药品监管科学行动计划,把“将真实世界数据用于医疗器械临床评价的方法学研究”列为首批研究项目,探索将真实世界数据用于监管决策的可行性和方法学,为医疗器械审评审批制度改革、加速创新产品的
CMDE - 真实世界 - 2019-12-30
CDE:《真实世界证据支持药物研发的基本考虑》意见稿
为落实国务院《关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)以及中共中央办公厅、国务院办公厅印发的《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号)鼓励研究和创制新药的要求,考虑到药物临床研发过程中,存在临床试验不可行或难以实施等情形,利用真实世界证据用以评价药物的有效性和安全性成为可能的一种策略和路径。
网络 - 真实世界证据,药物研发 - 2019-05-29
为您找到相关结果约500个