罕见病治疗药物Crysvita未被纳入NHS
X连锁性低磷血症(XLH)的儿童和年轻人不太可能在NHS上获得Kyowa Kirin's Crysvita的常规访问。
MedSci原创 - Crysvita - 2018-06-16
欧盟批准罕见的肌肉骨骼疾病药物Crysvita
医生现在可以利用Kyowa Kirin / Ultragenyx的Crysvita治疗在欧盟获得条件性批准的地区的患有罕见的慢性进行性肌肉骨骼疾病X连锁低磷酸盐血症的儿童。Crysvita(burosumab)是一种抗FGF23全人源单克隆
MedSci原创 - 欧盟,Crysvita - 2018-02-27
FDA批准FGF23阻断抗体Crysvita,治疗肿瘤诱发性骨软化症(TIO)
无法手术切除肿瘤的TIO,美国批准首个治疗药物
MedSci原创 - 低磷血症,肿瘤诱发性骨软化症,FGF23阻断抗体Crysvita - 2020-06-20
X连锁低磷血症(XLH):新数据表明Crysvita对XLH患者具有长期益处
Kyowa Kirin的Crysvita(burosumab)的最新长期数据显示,患有罕见遗传代谢性骨病X连锁低磷血症(XLH)的成年人能够从burosumab的治疗中持续受益。
MedSci原创 - Burosumab,XLH - 2021-09-26
首款突破性罕见病新药Crysvita今日获批 治疗遗传性软骨病
今日,Ultragenyx Pharmaceutical宣布美国FDA批准其新药Crysvita(burosumab),成为首个获批治疗1岁及以上儿童和成年人的X连锁低磷血症(XLH)的药物。
药明康德 - 2018-04-19
欧洲委员会(EC)批准CRYSVITA(burosumab)治疗老年人和成年人X连锁性低磷血症(XLH)
日本协和麒麟有限公司近日宣布,欧洲委员会(EC)已批准CRYSVITA(burosumab)用于老年人和成年人X连锁性低磷血症(XLH)。
MedSci原创 - Crysvita,Burosumab,X连锁性低磷血症,XLH - 2020-10-03
FDA批准首款遗传佝偻病药物burosumab
新闻事件今天FDA批准了Ultragenyx(RARE)/ Kyowa Kirin合作开发的FGF23抗体burosumab(商品名Crysvita?)用于治疗一岁以上X-连锁低磷性佝偻病(XLH)。Crysvita此前获得FDA突破性药物地位和优先审批资格,RARE因此将再获得一张优先评审券(PRV),因
美中药源 - 佝偻病 - 2018-04-19
FDA通过了一项遗传性佝偻病的治疗方法
Ultragenyx制药公司和Kyowa Hakko Kirin的Crysvita (burosumab-twza)是一种能阻止成纤维细胞生长因子23 (FGF23)的抗体,该激素能引起磷酸盐尿排泄,并
MedSci原创 - 遗传性佝偻病 - 2018-04-19
FDA发布2018年年度新药报告,罕见病药受关注
近日,美国食品药品监督管理局(FDA)发布了年度新药报告《2018 New Drug Therapy Approvals》,报告称2018年可谓”医药强势创新与进展的一年“。
独角兽工作室 - FDA,新药报告 - 2019-01-11
NMPA批准突破性罕见病药布罗索尤单抗上市,治疗X连锁低磷血症(遗传佝偻病)
中国国家药监局(NMPA)网站最新公示,已通过优先审评审批程序附条件批准了Kyowa Kirin Inc.公司的布罗索尤单抗注射液上市,用于成人和1岁儿童患者X连锁低磷血症(XLH)的治疗,这种疾病会
MedSci原创 - X连锁低磷血症 - 2021-01-16
2018年FDA批准的临床试验进展的新药汇总
新药和生物制品的提供常常意味着为患者提供新的治疗方案,从而促进公众的健康保健,而FDA的药物评价和研究中心(FDA’s Center for Drug Evaluation and Research,CDER)在帮助推进新药开发方面发挥关键作用。每年,CDER都批准许多新药和生物制品,其中一些产品是创新的新产品,以前从未在临床实践中使用,而一些产品是与先前批准的产品相同或相关,这些药品将进
MedSci原创 - 新药,FDA,2018 - 2018-12-19
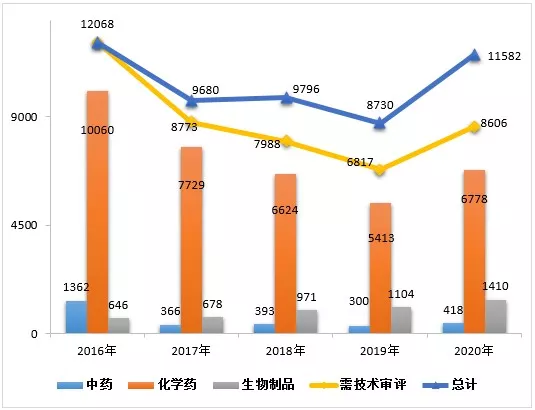
2020年度药品审评报告
2020年是极不平凡的一年,面对突如其来的新冠肺炎疫情,中国国家药品监督管理局药品审评中心(以下简称药审中心)在中国国家药品监督管理局(以下简称国家药监局)的坚强领导下,贯彻《药品管理法》《疫苗管理法
CDE - 药品审评报告 - 2021-06-23
为您找到相关结果约12个