FDA发布警告,将限制阿片类止痛药使用
在业内人士呼吁多年之后,近日FDA终于发表新指南,决定限制阿片类止痛药的使用,杜绝滥用。FDA在黑框警告中表示,阿片类止痛药的严重风险包括误用、滥用、成瘾、过量以及死亡。FDA表示,由于羟考酮、氢可酮、吗啡等止痛药会造成患者成瘾,因此药品标签上应当注明,只有在非成瘾性止痛药不足以达到止痛效果时,医生才能够给患者开具这些速效止痛药处方。FDA将列出新的警告剂量,并且警告不要让已产生身体依赖的患者
生物谷 - FDA,阿片类药物 - 2016-03-26
FDA:批准恩他卡朋辅助治疗帕金森病
近日,FDA的审查结果表明,没有明确证据表明使用恩他卡朋(一种用于治疗帕金森病的药物)会增加民众患心肌梗死、中风和其他心血管疾病的患病几率。因此,FDA在新闻发布会上解释道,恩他卡朋可作为标准药物左旋多巴/苄丝肼或左旋多巴/卡比多巴的辅助用药,用于治疗以上药物不能控制的帕金森病及剂末现象(症状波动)。
MedSci原创 - 帕金森,心血管,恩他卡朋 - 2015-10-30
FDA发布2019年度药品指南工作计划
美国FDA作为全球药品监管的权威机构和各类法规指南的风向标,一直被各国药政机构所关注,也是全球制药行业持续关注的热点机构。每年年初,FDA会对本年度需要新建和修订的指南发布工作计划,向社会公众和制药行业发出明确的引领信号;这份工作计划一直是制药行业所高度关注的。在2019年3月5日,FDA发布了2019年度药品指南工作计划,题目是《Guidance Agenda-New & Revised
CPhI制药在线 - FDA,药品 - 2019-03-07
FDA授予安斯泰来抗生素isavuconazole QIDP资格
安斯泰来(Astellas)2月27日宣布,FDA已授予实验性抗生素isavuconazole合格传染病产品(QIDP)资格认定,用于侵袭性毛霉菌病(nvasive mucormycosis,又名接合菌病此前,FDA已于2013年授予isavuconazole QIDP认定,用
生物谷 - 新药,FDA - 2014-03-04
拜耳肺动脉高压药物Adempas获FDA批准
拜耳(Bayer)10月9日宣布,FDA已批准Adempas(riociguat)用于2种类型的肺动脉高压:a)用于肺动脉高压(PAH)成人患者(WHO分级I)的治疗,以提高运动能力、WHO功能分级、推迟临床恶化
生物谷 - 动脉高压药物,FDA - 2013-10-11
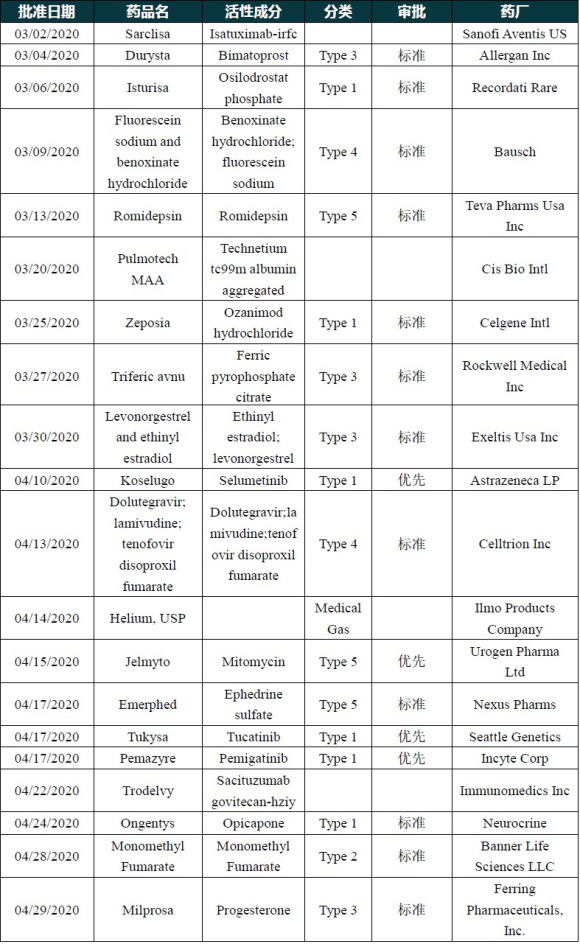
4月份,FDA和NMPA批准了哪些新药?
2020年1-4月批准了42个NDA/BLA申请新药,包括5个生物药,12个新分子实体(Type 1),7个新剂型(Type3),5个新组合(Type4),7个新配方或新制造商(Type5),2个已上
MedSci原创 - FDA,NMPA - 2020-05-07
FDA继续加快COVID-19新疗法的开发
美国食品和药品监督管理局(FDA)提出了一项新计划--冠状病毒治疗加速计划(CTAP),FDA正在使用该机构可使用的所有工具,以尽快为COVID-19患者提供新疗法。
MedSci原创 - FDA,Covid-19 - 2020-04-01
新癌症治疗技术导致病人死亡FDA紧急叫停
据美国媒体报道,就在美国食品药品管理局(FDA)批准制药公司诺华使用新的癌症治疗技术CAR-T一周后,该机构暂停了后面的试验,原因是用这种技术治疗的病人出现首例死亡病例。
网易科技 - FDA,CAR-T,安全 - 2017-09-06
FDA将三种药物列入安全观察清单
近日,美国食品与药物管理局(FDA)因潜在严重风险征象及新安全信息而将三种药物添加入安全观察清单。 拉科酰胺(Lacosamide)适用于治疗癫痫和肝、肾损伤;FDA不良事件报告系统(FAERS)于2012年接收到其致中毒性表皮松解坏死症和中性粒细胞减少报告。
医学论坛网 - FDA药物安全观察清单,拉科酰胺,达方吡啶,奥法木单抗 - 2013-02-17
FDA批准首个致密型乳腺患者超声检查仪器
美国食品药品管理局(FDA)今天批准了首个用于致密型乳腺患者联合乳房X线检查的超声检查仪器。 FDA在他们的批准声
网络 - FDA,致密型乳腺,超声检查仪器,X线检查 - 2012-09-26
FDA批准Axumin用于前列腺癌复发的检测
FDA批准Axumin(可注射放射性诊断试剂)用于前列腺癌复发的检测。适应于治疗后PSA升高,PET检查可疑前列腺癌复发的患者。FDA基于两项研究结果评价了Axumin (Blue Earth Diagnostics)的疗效和安全性。
MedSci原创 - Axumin,FDA,前列腺癌,复发 - 2016-05-29
FDA医疗器械临床试验设计指导原则解析
FDA发布了一则关于医疗器械关键性临床试验设计考量的指导原则,该指导原则旨在向参与以支持医疗器械上市前申报为目的的临床试验设计人员和FDA申报审评人员提供指导。可供医疗器械行业、临床试验实施人,机构评审委员会及FDA员工使用。FDA 在支持特定医疗器械类型相关研究方面已有明确的要求,在举证责任如何满足监管要求方面也已有一般要求,但尚未试图阐述适用于医疗器械上市前申报的各种临床 试验设计,或对委
MedSci原创 - 医疗器械,临床试验,FDA - 2013-12-20
FDA:淋巴瘤治疗药Adcetris新黑框警告
2012年1月13日,美国食品药品管理局(FDA)发布了关于使用Adcetris(brentuximab vedotin)与罹患进行性多灶性白质脑病(PML)风险的安全性通告。FDA新收到2例在接受Adcetris治疗的患者中发生的PML病例报告。该药品的说明书已经添加了强调此风险的新黑框警告。在2011年8月FDA批准Adcetris
MedSci原创 - Adcetris,淋巴瘤 - 2012-01-22
FDA支持新型超长效德谷胰岛素上市
11月9日,FDA顾问委员会以8比4投票支持新型超长效德谷胰岛素(insulin degludec,IDeg)用于治疗1型和2型糖尿病患者,但同时要求实施严格上市后研究,以便对心血管安全性加以评估。
医学论坛网 - 超长效德谷胰岛素,IDeg,FDA - 2012-11-16
为您找到相关结果约500个