最新临床试验专场试验揭晓
侯静波获CIT青年医师一等奖 刘健获CIT最具教育意义病例奖 昨日(3月16日)下午,第十届中国介入心脏病学大会(CIT)最新临床试验专场的四项研究在众人期待中揭晓,本报记者刘敏第一时间为您传递TRACK-D 与任何商业利益无关的TRACK-D研究通过大样本的前瞻性多中心随机对照试验纳入患者2998例。结果显示,瑞舒伐他汀可降低伴有慢性肾病2~3期的糖尿病患者对比
MedSci原创 - 临床试验 - 2012-03-23
化学药品创新药Ⅲ期临床试验前会议药学共性问题及相关技术要求(试行)
为鼓励创新,加快新药研发,提高申请人和监管机构沟通交流的质量和效率,在国家药品监督管理局的部署下,药审中心组织制定了《化学药品创新药Ⅲ期临床试验前会议药学共性问题及相关技术要求(试行)》。
国家药品监督管理局药品审评中心 - 化学药品创新药Ⅲ期临床试验 - 2023-03-30
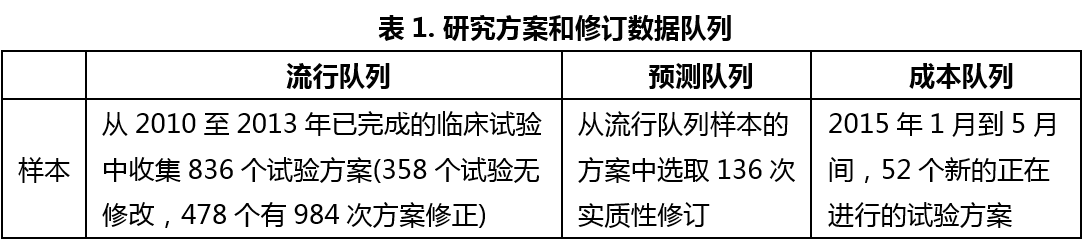
临床试验方案修订对临床试验结果和费用的影响
临床试验方案是保证临床试验顺利有序开展的前提,其一经制订并批准就应严格执行。在实际的临床试验开展过程中,有时对临床试验方案确有必要进行修订。但是,如果修订不够谨慎的话,就可能影响到试验结果、试验周期和试验经费。长期以来,对于制药公司和CRO公司而言,因临床试验方案的修订而导致的计划外的推迟、中断和花费都是很大的挑战。
国际药品检查动态研究 - 试验方案,修订 - 2019-12-26
临床试验用药品(试行)
根据《药品生产质量管理规范(2010年修订)》第三百一十条规定,现发布《临床试验用药品(试行)》附录,作为《药品生产质量管理规范(2010年修订)》配套文件,自2022年7月1日起施行。
国家药品监督管理局官网 - 临床试验 - 2023-06-10
实施临床试验报告规范,提高临床试验透明度
临床试验是指以人为对象的前瞻性研究,预先将受试者或受试人群分配至接受一种或多种医疗干预,以评价医疗干预对健康结局的影响。1、临床试验信息透明化的必要性 临床试验是获得防病治病知识的必要途径,主要目的是不断改进预防、诊断和治疗方法,提
MedSci原创 - 临床试验,规范,透明度 - 2014-04-24
Lancet Diab & Endo:心衰应该成为糖尿病药物临床试验的一项重点要求
研究人员表示,糖尿病药物临床试验应将检测心衰作为一项重要的结局试验。心衰住院治疗是糖尿病一项最常见并且是可预见的重要并发症,应该作为临床试验的一个终点,格拉斯哥大学医学博士John McMurray与其同事在The Lancet Diabetes & Endocrinology“我们认为在降糖新药的心血管结局临床试验中应该进行心衰的系统性评价,要么将其作
dxy - 糖尿病,心衰,临床试验 - 2014-03-18
《化学药品创新药I期临床试验申请药学共性问题相关技术要求》和《化学药品I期临床试验申请药学研究信息汇总表(修订版)》
为指导化学药品创新药研发,在国家药品监督管理局的部署下,药审中心组织制定了《化学药品创新药I期临床试验申请药学共性问题相关技术要求》,同时对原食品药品监管总局《关于发布〈新药I期临床试验申请技术指南〉
CDE - 2020-12-07
临床试验有关SOP汇总
临床试验方案修改SOP1. 申办者(包括药厂、CRO等)向中心药物临床试验办公室提出修改申请,填写“药物临床试验修改申请表”。2.提供资料,包括:药物临床试验前研究资料,含试验药物的化学、药学、毒理学、药理学和临床的(包括以前的和正在进行的试验)资料和数据、研究者手册、试验药品药检报告、申办者资质证明、SFDA药物临床试验批文、试验方案和知情同意书药物临床试验办公室根据
MedSci原创 - 临床试验,SOP - 2014-03-28
全球临床试验概况分析
根据美国clicaltrial网站中的临床试验进行统计分析结果,我们可以了解到全球临床试验的概况。整体来说,国际上临床试验处于快速发展阶段,但是美国仍然处于领先地位。中国临床试验数量约占全球的8%。一、临床试验分布情况 据美国clicaltrial统计的结果显示,全球约131,478个临床试验,全在美国占42%,而非美国42%,另外,还有6%的临床试验与美国有关。从些结果来看,美国还是全球绝
MedSci原创 - 临床试验 - 2012-08-26
如何开展新药临床试验:从GCP,SOP到临床试验管理和质量控制
GCP的原则与内容 GCP(Good Clinical Practice),即药物临床试验质量管理规范,它是临床试验过程的标准规定,包括方案设计、组织实施、监查、稽查、记录、分析总结和报告。其目的是保证药品临床试验过程规范,结果科学可靠,保护受试者的权益并保障其安全。 一、GCP的发展过程 19世纪末化学制药工业的兴起,开创了化学药品开始用于临床治疗的新纪元。
上海交通大学医学院附属第九人民医院 - 新药,临床试验 - 2015-07-04
揭露临床试验数据内幕
近日,一系列临床试验敏感数据的公开计划使制药公司、药物监管机构与研发团队们陷入了僵局。然而就在这场“斗争”似乎即将白热化时,一项研究揭示了为什么这些保密资料对于研究者而言是极其重要的。这项研究的分析结果表明,大多数公开的临床试验数据都缺少一些至关重要的信息(例如死亡率与严重的副作用)。但是这些信息却通常能在制药行业制定的、非公开化的标准文件中找到,而这类文件被称为临床研究报告(
生物探索 - 临床试验数据 - 2013-10-29
临床试验常见问题
一、课题负责人/主要临床研究者的职责 ? 准备研究方案 ? 提出统计分析要求 ? 定期访问个参加试验的分中心,监督研究进展 ?&nbs
MedSci原创 - 试验 - 2013-04-16
临床试验也能做公益?
有数据显示,近年来随着国家对生物医药技术创新领域的投入不断加大,药品生产企业及科研单位研发新药的热情日益高涨,我国每年所做的药物临床试验的数量以40%的惊人速度增加,我国正日益成为全球临床试验服务中心。然而与企业和科研单位高涨的热情相比,我国患者参与临床试验的程度的不高,其中的原因:(1)由于患者对临床试验不了解担心患者招募的安全性,(2)患者想参与临床试验,但缺乏途径。仔细分析其中的原因就是临床
MedSci原创 - 2017-07-18
临床试验中的自查
自从15年起国家局对临床试验的一大波动作之后,对临床试验行业的震慑力不用言语,首先是一小批项目被查出数据质量问题公示了,之后是各省局纷纷召集业界开会,一大批项目的自查四起,一时间医院机构神兵降临、烽烟
Clinical Discovery - 2020-03-29
为您找到相关结果约500个