CFDA半夜发文:临床试验机构拟改为备案制 鼓励社会资本投资
此次征求意见稿若通过,临床试验机构中将有更多社会资本的参与空间,有利于提高临床试验人员的积极性、临床试验的效率等。
CFDA - 临床试验机构,CFDA - 2017-05-12
CFDA发布《药物临床试验机构管理规定(征求意见稿)》
10月26日,为落实中共中央办公厅、国务院办公厅《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,做好药物临床试验机构资格认定调整为备案管理的相关准备工作,CFDA官网发布了公开征求《药物临床试验机构管理规定
CFDA - CFDA,药物临床试验管理规定 - 2017-10-27
定稿:2018年1月1日起施行医疗器械临床试验机构备案办法
医疗器械临床试验机构由资质认定改为备案管理,自2018年1月1日起施行。
国家食品药品监督管理总局 - 医疗器械,临床试验,备案 - 2017-11-25
医疗器械临床试验机构监督检查要点及判定原则(二次征求意见稿)
为进一步加强医疗器械临床试验机构管理,指导药品监管部门规范开展监督检查工作,国家药监局组织起草了《医疗器械临床试验机构监督检查要点及判定原则(二次征求意见稿)》,现向社会公开征求意见。
国家药品监督管理局 - 医疗器械临床试验 - 2024-03-13
落实医疗器械临床试验机构由“资质认定”改为“备案管理”
按照《国务院关于修改〈医疗器械监督管理条例〉的决定》(中华人民共和国国务院令第680号)的要求,医疗器械临床试验机构由资质认定改为备案管理。8月4日晚,CFDA正式印发了《医疗器械临床试验机构条件和备案管理办法(征求意见稿)》。
CFDA - CFDA,医疗器械,备案管理 - 2017-08-05
国家药监局综合司公开征求《药物临床试验机构监督检查办法(试行)(征求意见稿)》意见
为进一步规范药物临床试验机构监督检查工作,加强药物临床试验管理,国家药监局组织起草了《药物临床试验机构监督检查办法(试行)(征求意见稿)》,现公开征求意见。
国家药监局综合司 - 药物临床试验 - 2023-07-04
12月1日起,全面实施药品上市许可持有人制度,临床试验机构备案管理,取消药品GMP、GSP认证
《中华人民共和国药品管理法》(以下称药品管理法)已由第十三届全国人大常委会第十二次会议于2019年8月26日修订通过,自2019年12月1日起施行。国家药监局正在抓紧开展配套规章、规范性文件和技术指南的制修订工作,并将按程序陆续发布。
国家药监局 - 国家药监局,GSP,GMP - 2019-11-30
上海医疗机构率先成功为小年龄儿童完成Wada试验
国家儿童医学中心、复旦大学附属儿科医院27日披露,该院癫痫中心多学科专家率先为6岁女孩完成了Wada试验,定位大脑优势半球,让家长免去了抉择的痛苦。据查,为如此低龄儿童完成Wada试验此前中国未有报道。Wada试验,又称阿米妥试验,是国际上术前对优势大脑半球判断的一种有创术检查,
中国新闻网 - 上海,医疗机构,Wada试验 - 2018-09-27
印度监管机构:批准Favipiravir抗病毒片剂治疗COVID-19的临床试验
制药公司Glenmark今日宣布,它已获得印度监管机构(DCGI)的批准,可开展Favipiravir抗病毒片剂治疗COVID-19患者的临床试验。
MedSci原创 - Covid-19,Favipiravir - 2020-05-01
两高:药物临床试验等机构提供报告严重失实可构提供虚假证明文件罪
药物临床试验数据造假直接影响药品质量、医疗效果,扰乱医疗行业监管秩序,危及人民群众身体健康和生命安全。
新华网 - 药物临床试验,两高,解释 - 2017-08-15
北京养老机构补贴将首次向民营营利机构开放
今后,北京面向民营养老机构的补贴将不再局限于非营利的范围内。11月22日上午,北京市民政局正在召开新闻发布会解读新发布的《北京市养老机构运营补贴管理办法》(以下简称《管理办法》)、《北京市社区养老服务驿站运营扶持办法》(以下简称《扶持办法》)。北京市民政局副局长李红兵告诉北京商报记者,本次发布的《管理办法》是北京出台的、对于养老机构运营补贴的2.0版本政策,其中最大的亮点之一就是将补贴范围进一步的
北京商报 - 北京养老机构,补贴,首次,民营营利机构 - 2018-11-22
筹备申报药物临床试验(GCP)机构资格认定的关键环节
我国政府对实施临床试验的医疗机构实行资格准入制度,即临床试验必须在国家食品药品监督管理局 (SFDA)批准的临床试验机构进行。而医疗机构资格认定具有明确程序与标准[1],以保证医疗机构具备一定的条件和资质,降低申报者选择研究机构的盲目 性及受试者参加临床研究的风险[2]。一些实力较强的医疗机构或实力较为雄厚的专业因未申请机构认证而无法参加新药的临床试验,这是一种资源的浪费 [3]。作
华西医学 - GCP,临床试验 - 2014-03-03
欧洲药监机构就替格瑞洛临床试验问题向阿斯利康进行询问
欧洲药品监管机构已经写信给阿斯利康,要求阿斯利康提供更多有关美国调查其心脏病新药替格瑞洛的信息。位于伦敦的欧洲药品管理局(EMA)于11月7日表示,在阿斯利康于10月31日披露了DOJ的调查之后,该机构已与该英国第二大制药商进行了接触。“EMA重视
丁香园 - 替格瑞洛,欧洲药监,临床试验,阿斯利康 - 2013-11-11
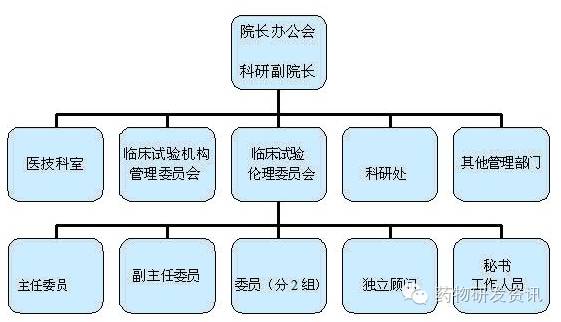
组织机构
主办单位: 中华人民共和国科技部 中华人民共和国卫生部 中华人民共和国教育部 国家人口和计划生育委员会 国有资产管理委员会 国家食品药品监督管理局 国家中医药管理局 中国科学院 中国工程院 解放军总后勤部卫生部 中国科学技术协会 山东省人民政府 承办单位: 中国生物技术发展中心 烟台市人民政府 国药励展展览有限责任公司 &nb
会议 - 2008-06-04
为您找到相关结果约500个