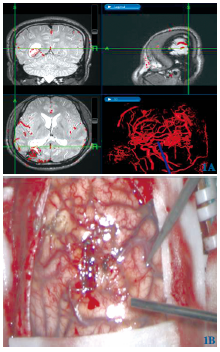
多模态影像融合神经导航在脑动静脉畸形手术的应用
男6例,女4例;年龄14~62岁。病灶部位:枕叶5例,颞枕3例,额叶2例。首发症状为癫疒间4例,脑出血2例,头痛头晕症状检查发现4例。
中国微侵袭神经外科杂志 - 脑动脉,畸形 - 2019-05-15
经十二指肠镜行逆行胰胆管造影术后感染及防控策略现状
目前经内镜逆行胰胆管造影术(endoscopic retrograde cholangiopancreatography,ERCP)是临床处理胆膜疾病的重要手段,如今诊断性ERCP已逐步发展为治疗性ERCPERCP是一项具有一定风险的侵入性操作,与操作有关的并发症并不罕见,胆道感染是常见的并发症之一。尤其是2015年美国特大耐药大肠杆菌爆发感染事件更将十二指肠镜清洗消毒质量控制的重要性提升到
《中华医学杂志》 - ERCP,术后感染,防控 - 2017-01-03
CDE和注册司专家发文:基于风险的监查(RBM)应用和挑战
作者:苏娴a,崔孟珣b(国家食品药品监督管理总局 a.药品审评中心,b.药品化妆品注册管理司,北京 100038) 来源:中国新药与临床杂志 2018年6月 第37卷第6期 摘要:本文结合国际人用药品注册技术要求协调会(ICH)及美国食品和药物管理局(FDA)关于基于风险的监查(RBM)的指南,概述RBM的目的及在不同类型临床试验中的应用,介绍目前实施RBM方法的流程,包括
中国新药与临床杂志 - CDE,风险的监查 - 2018-08-16
总局发布质子碳离子治疗系统临床评价技术审查指导原则
1月8日,食品药品监管总局发布通告称,为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了质子碳离子治疗系统临床评价技术审查指导原则(见附件),现予发布。
新浪医药新闻 - CFDA,质子碳离子治疗,质子碳离子治疗 - 2018-01-09
CFDA:质子碳离子治疗系统临床评价技术审查指导原则
昨日(1月8日),国家食品药品监督管理总局发布了《质子碳离子治疗系统临床评价技术审查指导原则(2018年第4号)的通告》。通告称,为加强医疗器械产品注册工作的监督和指导,进一步提高注册审查质量,国家食品药品监督管理总局组织制定了质子碳离子治疗系统临床评价技术审查指导原则(见附件),现予发布。
CFDA - CFDA,临床评价,质子碳离子 - 2018-01-09
随机试验中的样本量考量
普遍的概念认为随机试验需要产生样本量大小相等的各个比较组。这种概念上的误解导致研究者强行达成样本量相等而产生偏倚,尤其如果应用的是不科学的方式。在随机对照试验中,尤其是使用排列区组随机法(permuted-block randomisation) 的非双盲试验(non-douhle-blindedtrials) 中,绝对均等的样本量对提高统计学的把握度没有什么帮助
天坛临床试验与临 - 随机,样本 - 2015-01-18
CFDI最新分享了核查中发现的常见问题总结,探讨了新形势下申办方的应履职责
从药物临床试验数据核查看申办者的职责履行情况 作者:高荣王安娜唐静方翔王佳楠 国家药品监督管理局食品药品查验中心 来源:中国新药杂志 2019 年第 28 卷第 8 期摘要:申办者作为药物临床试验的发起组织者、经费提供者和试验监查者,在药物临床试验中发挥着至关重要的作用。本文根据《药物临床试验质量管理规范》(GCP)的相关规定及药物临床试验监督检查新形势下对申办者的职责要求,结合药物临床
网络 - 药物临床试验,药物临床试验质量管理规范,数据核查,申办者,职责 - 2019-06-09
《预防新型冠状病毒感染公众佩戴口罩指引(2023年4月版)》印发(附解读)
养老机构、社会福利机构及托幼机构、学校、校外培训机构等重点机构医护、餐饮、保洁、保安等公共服务人员工作期间应佩戴口罩。
国家疾控局 - 新型冠状病毒,佩戴口罩 - 2023-04-12
傅向华:4Fr指引导管从造影到支架一步到位完成PCI
2010年8月10日,傅向华教授在国内首次应用4Fr指引导管完成了一例支架内再狭窄且右冠开口于左冠窦的复杂冠脉病变患者的冠脉介入治疗,应TCT2012大会的邀请,傅向华教授在美国迈阿密举行的TCT2012大会上报告挑战性病例《经尺动脉入径应用4Fr指引导管一步到位完成右冠开口畸形复杂冠脉介入治疗》,这标志着经前臂(桡/尺)动脉更加微创化冠状动脉介入治疗取得了新
心网 - PCI,支架 - 2013-05-15
临床试验:方案违背和方案偏离的定义和区别
方案违背(Protocolviolation)和方案偏离(Protocol deviation)一般外企的公司都会把他们归为一类,其实PD和PV的差别很多情况的差别在于严重程度不同,但是关于PD和PV
Clinical Discovery - 临床试验 - 2020-03-29
新药临床试验设计中的基础问题解读
1新药临床试验管理规范1.1受试者权益安全性保障(即伦理性) 1.临床试验必须获得国家药品监督管理局的批准 2.为确保受试者的权益,并为之提供公众保证。必须经伦理委员会批准 3.中国GCP规定参加临床试验的研究单位必须是国家药品临床研究基地 4.中国GCP规定,负责临床试验的研究者(investigator)必须具备的条件
MedSci原创 - 新药,临床试验,设计 - 2012-12-25
为您找到相关结果约500个