多篇突破性研究直击抗癌药物新发现
人类基因组测序不仅加深了我们对机体运作机制的认识,同时也为开发疾病治疗药物提供了新的可能。一项刊登在Nature Communications杂志上的研究报告中,格拉斯哥大学英国癌症研究中心的科学家就开发出了一种名为mito-priming的新技术,该技术能够帮助研究者们识别新型有效的抗癌药物
生物谷 - 癌症,药物 - 2016-11-06
CONTEPO治疗复杂尿路感染取得突破性进展
Nabriva是一家临床阶段的生物制药公司,致力于研究和开发治疗严重感染的创新抗感染药物,近日宣布美国食品和药品管理局(FDA)已接受CONTEPO™(注射用磷霉素)的新药申请(NDA),并进行优先审查,以治疗包括急性肾盂肾炎在内的复杂尿路感染(cUTIs)。
MedSci原创 - CONTEPO,复杂尿路感染,肾盂肾炎 - 2019-01-10
CAR-T疗法拟纳入突破性治疗药物名单
8月5日,国家药监局(NMPA)药品审评中心(CDE)最新公示,传奇生物旗下生物制品1类新药西达基奥仑赛(cilta-cel,LCAR-B38MCAR-T细胞自体回输制剂)拟纳入突破性治疗药物名单,中
健康界 - 创新药,CAR-T疗法,突破性治疗 - 2020-08-07
肝脏疾病突破性研究进展
【1】Nat Biotech:基因治疗应用CRISPR/Cas9治疗肝脏疾病 在过去35年基因治疗发展进程中,James Wilson是其中一位开拓者,近期他把病毒载体和最新CRISPR/ Cas9技术结合
生物谷 - 基因治疗 - 2016-03-21
FDA批准帕金森突破性药物Nuplazid上市许可
近日Acadia在美国监管方面收获好消息,其帕金森药物Nuplazid获得专家委员会支持,有望在美国获批。此次专家咨询委员会以12:2的投票结果赞成Nuplazid (pimavanserin)获批,认为其在帕金森治疗方面的效果大于风险,预计将有可能在今年的5月1日得到FDA的最终审批结果。
MedSci原创 - 帕金森,Nuplazid - 2016-04-30
Xolair被认为是治疗食物过敏的“突破性”疗法
罗氏(Roche) /诺华(Novartis)的Xolair在美国被授予突破性地位,用于治疗意外接触食物过敏原后出现的严重过敏反应。Xolair (omalizumab)是一种针对免疫球蛋白E的单克隆抗体,已在美国获准用于治疗哮喘和慢性特发性荨麻疹(无已知病因的慢性荨麻疹)。突破性治疗指定食物过敏 - 影响美国高达8%的儿童和4%的成年人--来自七项临床研究的数据,这些研究评估了该药物对一系列食物
MedSci原创 - Xolair,食物过敏 - 2018-08-15
FDA授予IgE单抗Xolair突破性疗法认定,治疗食物过敏
罗氏和诺华公司的过敏药物Xolair(omalizumab)获得FDA突破性认定,用于治疗新的适应症--食品过敏。
MedSci原创 - IgE单抗,Xolair,食物过敏 - 2018-08-14
国内自主CAR-T疗法被纳入突破性治疗品种
据国家药监局药审中心官网信息显示,合源生物CAR-T细胞治疗产品CNCT19细胞注射液(抗CD19嵌合抗原受体T细胞注射液)获准纳入“突破性治疗药物”(CDE受理号:CXSL1800106),拟适应症
医谷网 - 淋巴细胞白血病 - 2020-12-24
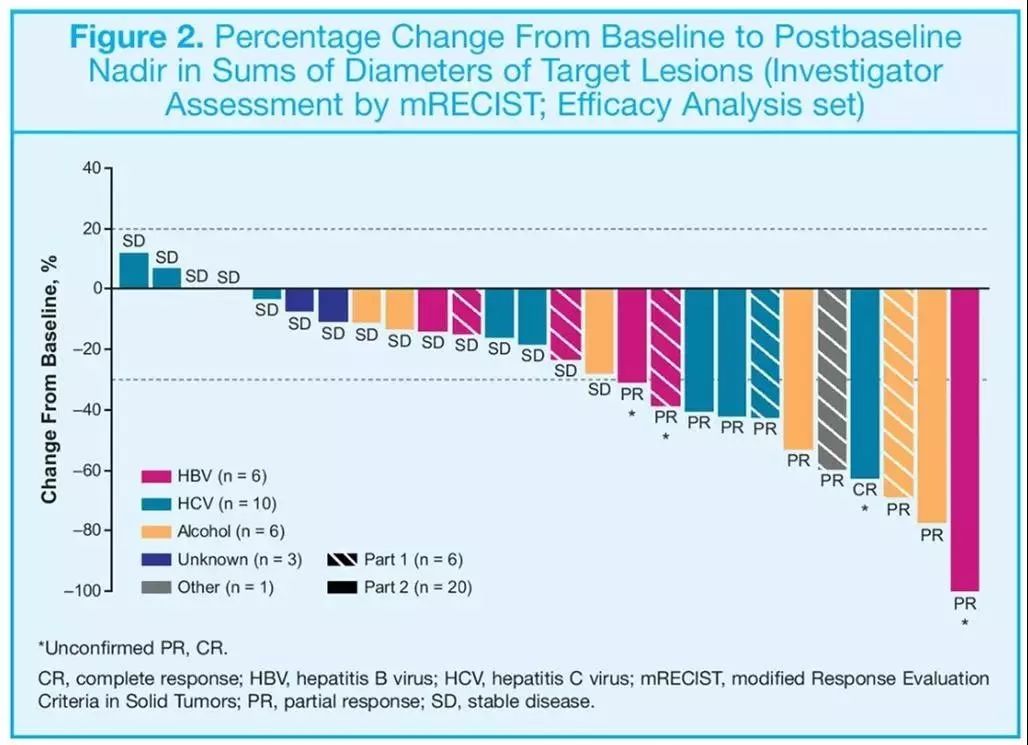
FDA授予肝癌突破性疗法:免疫+靶向治疗豪华组合疗法
2019/7/23,默沙东(MSD)和卫材(Eisai)联合宣布,美国FDA已经授予帕博丽珠单抗(Pembrolizumab)与仑伐替尼(Lenvatinib)的KL组合疗法针对不能局部治疗的晚期不可切除的肝细胞癌(HCC)患者的一线治疗突破性疗法认定[1]。
网络 - 免疫,靶向 - 2019-08-06
Keytruda组合疗法治疗肝癌获FDA突破性疗法认定
默沙东(MSD)和卫材(Eisai)联合宣布,美国FDA已经授予Keytruda(pembrolizumab)与Lenvima(lenvatinib)组合疗法突破性疗法认定,用于一线治疗不能局部治疗的晚期不可切除的肝细胞癌
药明康德 - 药明康德 - 2019-07-25
勃林格殷格翰同类首创在研免疫新药Spesolimab获得CDE突破性治疗药物认定
6月25日,勃林格殷格翰宣布,其在研免疫新药Spesolimab已获得国家药品监督管理局药品审评中心(CDE)认定为突破性治疗药物,用于治疗泛发性脓疱型银屑病(GPP)。
梅斯医学 - 泛发性脓疱型银屑病 - 2021-06-25
绝佳反击:FDA授予罗氏眼科药物Lucentis突破性疗法认定
罗氏(Roche)本周收获了一个好消息,FDA已授予眼科药物Lucentis治疗糖尿病性视网膜病变(DR)的突破性疗法认定。此前,FDA于今年9月接受审查Lucentis治疗糖尿病性视网膜病变(DR)的补充生物制品许可(sBLA)并授予优先审查资格。FDA将于2015年2月6日做出最终审查决定。“突破性疗法”认定,旨在加快某些重症治疗新药的开发和审评。目前,“突破性疗法”新药研发正呈上升势
生物谷 - 眼科,药物 - 2014-12-19
默沙东黑色素瘤药物Lambrolizumab获FDA“突破性疗法”资格
突破性疗法资格的获得使lambrolizumab(代号 MK-3475)引起众人关注,授予lambrolizumab这一资格意味着FDA认可该治疗药物对威胁生命的疾病表现出明显收益
丁香园 - 黑色素瘤,药物,Lambrolizumab,FDA - 2013-04-26
CDE发布了《突破性治疗药物工作程序》和《优先审评审批工作程序》征求意见
本周五,CDE发布关于《突破性治疗药物工作程序》和《优先审评审批工作程序》征求意见的通知,对突破性治疗药物工作程序和优先审评审批工作程序做了说明。突破性治疗药物程序、附条件批准程序、优先审评审批程序、特别审批程序是为我国鼓励创新和满足临床急需而设立的四个加快通道。其中,突破性治疗药物程序定位于药品临床试验研制阶段;优先审评审批程序定位于药品上市注册阶段。 这让人不禁联想到美国FDA的四种加快
网络 - CDE,突破性治疗药物 - 2019-11-09
Cell Reports:帕金森的突破性发现
都柏林三一学院科学家在帕金蛋白(parkin protein)的认识上取得了重要突破,该蛋白是调节大脑内神经细胞维持和更换的蛋白质。这一突破性发现对在帕金森氏症中神经细胞是如何死亡的产生了新的研究视角。 该小组研究结果发表在Cell Reports杂志上。
生物谷 - 帕金森 - 2014-11-20
为您找到相关结果约500个