临床试验透明度达到历史最高水平
ABPI赞助的研究显示,行业资助的12个月临床试验信息披露率已经从2009年的71%大幅提高到2014年的93%。根据一项研究,及时报告制药公司赞助的新批准药物临床试验的结果已达到93%的最高记录水平。该研究是欧洲药物管理局(EMA)连续六年(2009-2014)批准的所有142种新药的所有试验系列中最新的一项。
MedSci原创 - 临床试验透明度 - 2017-12-25
NMPA发布新增154家药物临床试验机构认定机构!
根据《中华人民共和国药品管理法》《药物临床试验机构资格认定办法(试行)》,经资料审查和现场检查,认定北京陆道培医院等154家医疗机构具有药物临床试验机构资格、北京大学第一医院等86家药物临床试验机构新增专业资格,发给《药物临床试验机构资格认定证书》。国家药监局2019年10月16日附件具备药物临床试验机构资格的医疗机构及认定专业
国家药品监督管理局 - NMPA,临床试验,验证机构 - 2019-10-31
临床试验中的核查/检查需要注意的关键要点
临床试验在CFDI审核之前需要经历一场大考,就是我们所说的临床试验核查。如果核查通过了,就等于之前所做的一切努力没有白费,团队的经验得到认可,能力也有质的飞越(感觉),投资人的来电响个不停...假如核
临床研发资讯 - 2020-03-29
FDA合作推动在印度进行临床试验的安全和质量
经过16个多小时的飞行,我们深夜在孟买机场降落,当我们离开机场候机楼时,立刻被一阵热拉潮湿的空气包围。坐在机场去往酒店的车上,孟买庞大的天际线让人惊讶不已。这就是印度,拥有世界17%的人口,但却占据了约20%的全球传染性疾病和非传染性疾病总量。
FDA Voice - FDA,印度,临床试验,安全质量 - 2017-07-14
CFDA官网干货:抗肿瘤药物临床试验重要终点指标
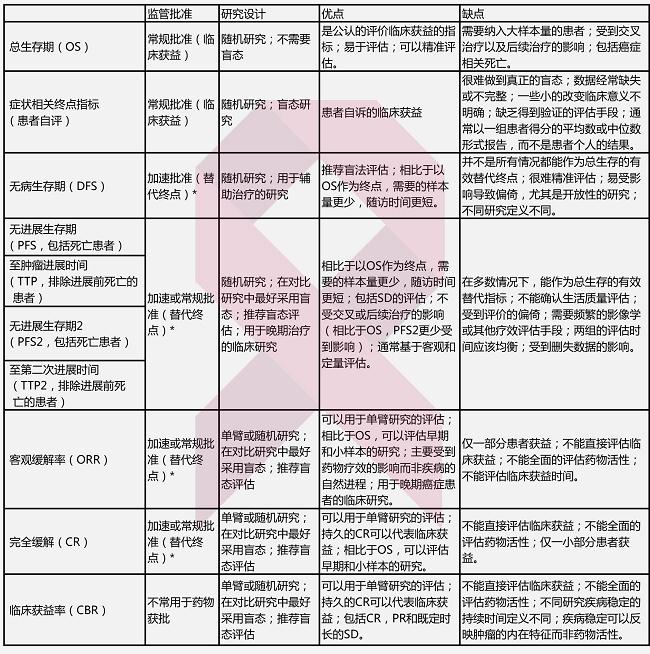
美国FDA在公示抗肿瘤新药审批结果时,绕不开一系列的临床试验观察指标,如总生存期、无进展生存期、客观缓解率等,这些终点指标如何定义?作为研究终点各自有何差异?肿瘤资讯小编特整理CFDA官网的相关信息,带您了解抗肿瘤药物临床试验重要终点指标。
肿瘤资讯 - CFDA,抗肿瘤,药物,临床试验,终点指标 - 2017-08-30
美国一款新冠病毒疫苗进入临床试验
目前,全球多种疫苗路线正齐头并进,中国沿着5条技术路线加速疫苗攻关工作。而北京时间3月5日,据美国生物技术公司Moderna官方宣称,美国食品药品监督管理局(FDA)已完成对该公司研制的新型冠状病毒m
科技日报 - 新冠病毒,疫苗 - 2020-03-11
重磅:全球干细胞治疗糖尿病临床试验现状梳理!
干细胞治疗糖尿病潜在的治疗机制。潜在的机制包括了保护内源性胰岛和恢复β细胞两种。MSCs通过免疫调节和抑制缺氧诱导的细胞凋亡来保护内源性β细胞。
干细胞者说 - 干细胞治疗,糖尿病临床试验现状 - 2022-11-02
Science:多种抗埃博拉病毒药物相继开展临床试验
蒙罗维亚一家医院的工作人员。很多埃博拉患者在此接受治疗。图片来源:DOMINIQUE FAGET 10月2日,利比里亚首都蒙罗维亚,Ashoka Mukpo给父亲留了一封语音邮件,表示自己“得到一个难以接受但又并非意料之外的消息”。 Mukpo是美国国家广播公司的自由摄影师,刚得知自己的埃博拉病毒检测呈阳性。他的父亲Mitchell&n
科学网 - 埃博拉病毒,临床试验,ZMapp - 2014-12-08
2011 ESPGHAN 儿童和青少年慢性丙型肝炎临床试验指南
J Pediatr Gastroenterol Nutr. 2011 Feb;52(2):233-7. - 2011-02-01
抗肿瘤药物临床试验技术指导原则(第二稿)
为达到延长生存的目标,患者往往愿意承担比其他药物更大的安全性风险,这使得对肿瘤药物的风险效益权衡不同于其他药物,也使得肿瘤药物的临床研究完全遵循一
MedSci原创 - 肿瘤,试验 - 2013-04-17
临床试验中采用非劣效设计应该关注的问题
非劣效性设计在国内新药临床研究中被普遍应用,本文就非劣效性试验的适应条件、设计中需要关注的问题进行了阐述,提出非劣效性设计并不是能够普遍应用的临床试验设计方法的观点。 临床试验是探索和确证研究药物在特定适应症人群安全有效性的重要研究方法,根据其研究目的主要有两种类型的设计,一种为优效性设计,一种为非劣效性设计。
审评四部 - 非劣效,临床试验 - 2014-03-13
临床试验数据管理之数据记录的常见问题
做临床试验的数据管理,那肯定需要对数据记录进行核查的,虽然有程序核查来完成大部分数据库核查工作,不过毕竟机器不是万能,还是有一些东西需要经验老道的数据管理员来完成的。
MedSci原创 - 数据管理 - 2012-12-13
为您找到相关结果约500个