药物临床试验机构监督检查办法(试行)(征求意见稿)起草说明
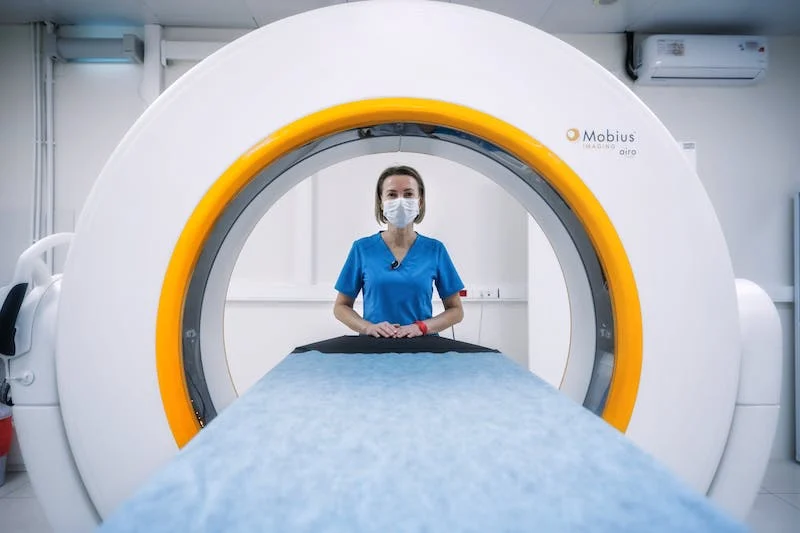
为进一步规范药物临床试验机构监督检查工作,加强药物临床试验管理,国家药监局组织起草了《药物临床试验机构监督检查办法(试行)(征求意见稿)》,现公开征求意见。
国家药品监督管理局官网 - 药物临床试验 - 2023-07-04
依托咪酯乳状注射液生物等效性研究指导原则(征求意见稿)
国家药品监督管理局药品审评中心起草了《依托咪酯乳状注射液生物等效性研究指导原则(征求意见稿)》。
国家药品监督管理局药品审评中心 - 依托咪酯乳状注射液 - 2023-07-27
CDE「以患者为中心」临床指导原则3连发(征求意见稿)
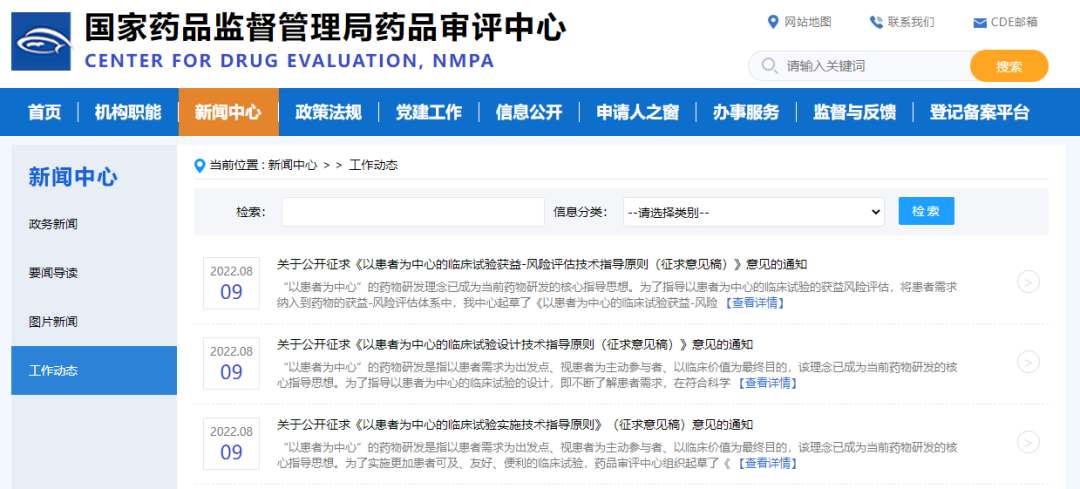
以患者为中心”的药物研发理念已成为当前药物研发的核心指导思想。为了指导以患者为中心的临床试验的获益风险评估,将患者需求纳入到药物的获益-风险评估体系中,我中心起草了《以患者为中心的临床试验
CDE - 指导原则,以患者为中心 - 2022-08-09
《药物真实世界研究设计与方案框架指导原则(征求意见稿)》
为了指导申办者科学合理的设计真实世界研究,明确真实世界研究方案撰写的技术要求,我中心组织起草了《药物真实世界研究设计与方案框架指导原则(征求意见稿)》,现公开征求意见。欢迎各界提出宝贵意见和建议,并请
CDE - 真实世界研究 - 2022-07-08
《化学药品3类注册申请药学自评估报告(原料药)(征求意见稿)》
为了更好地服务申请人,指导化学药品3类仿制药的研发和申报,提高申报资料质量,推动仿制药高质量发展,药审中心结合药品审评工作实践,起草了《化学药品3类注册申请药学自评估报告(原料药)(征求意见稿)。
国家药品监督管理局药品审评中心 - 化学药品 - 2024-04-08
化学仿制药透皮贴剂药学研究技术指导原则(征求意见稿)
为贯彻《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)、《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号)和国家局、药审中心关于化学药品仿制药的
CDE - 指导原则 - 2020-10-03
预防抗肿瘤药物所致恶心呕吐药物临床研究设计指导原则(征求意见稿)
用于预防或减少抗肿瘤药物所致恶心呕吐的治疗方法是恶性肿瘤患者支持疗法中的必要组成部分,目前依然存在未被满足的临床需求,同时快速进展的抗肿瘤药物的研发对于相关止吐药物临床试验提出新的挑战。现阶段国内尚无
CDE - 抗肿瘤药物 - 2021-08-23
NMPA发布疫情期间药物临床试验管理指导原则征求意见稿
小编注:CDE发布了祖国版疫情期间临床试验管理指南征求意见稿,虽然略显迟些,但可以看到监管部门在应急管理方面的进步,该指南对于行业具有指导意义。该指南和EMA和FDA的指南中内容有很多相似之处,想必各
NMPA - 临床试验,指导原则 - 2020-05-05
克罗恩病治疗药物临床试验技术指导原则(征求意见稿)
为进一步规范和指导克罗恩病治疗药物临床试验,提供可参考的技术规范,我中心起草了《克罗恩病治疗药物临床试验技术指导原则》,经中心内部讨论,已形成征求意见稿。
CDE - 克罗恩病 - 2021-07-04
2015 NICE指南:成人,儿童和青少年哮喘的诊断和监测(征求意见稿)
2015年1月,英国国家卫生与临床优化研究所(NICE)发布了成人,儿童和青少年哮喘的诊断和监测指南(征求意见稿)。
NICE官网 - 哮喘,诊断和监测 - 2015-01-28
纳米药物非临床安全性研究技术指导原则(试行)(征求意见稿)
近年来随着纳米技术的发展,纳米药物研究逐渐成为药物开发热点之一。目前国际药监机构对纳米类药物尚无统一认识,未形成统一监管要求,但总体持谨慎态度。在这种情况下,探索不同类型纳米类药物的非临床安全性评价及
CDE - 纳米药物 - 2021-05-13
新型冠状病毒中和抗体类药物技术资料要求(药学)(征求意见稿)
为了积极应对新冠肺炎疫情,加快和规范新型冠状病毒中和抗体类药物研制,我中心组织起草了《新型冠状病毒中和抗体类药物技术资料要求(药学)(征求意见稿)》,现在中心网站予以公示。
CDE - 新型冠状病毒 - 2021-06-27
基因转导与修饰系统药学研究与评价技术指导原则(征求意见稿)
为了规范细胞治疗产品基因转导与修饰系统的药学研究,统一评价标准,引导相关产品的研究与申报,我中心在借鉴国内外相关监管标准的基础上,通过前期调研、文件撰写、专家咨询以及部门讨论
CDE - 指导原则 - 2020-10-02
涉及人的生命科学和医学研究伦理审查办法(征求意见稿)
为保护人的生命和健康,维护人的尊严,尊重和保护受试者的合法权益,促进生命科学和医学研究健康发展,我委将《涉及人的生物医学研究伦理审查办法》(国家卫生和计划生育委员会令第11号)中行之有效的制度安排进行
卫健委 - 伦理 - 2021-03-16
为您找到相关结果约500个