用于产生真实世界证据的真实世界数据指导原则(征求意见稿)
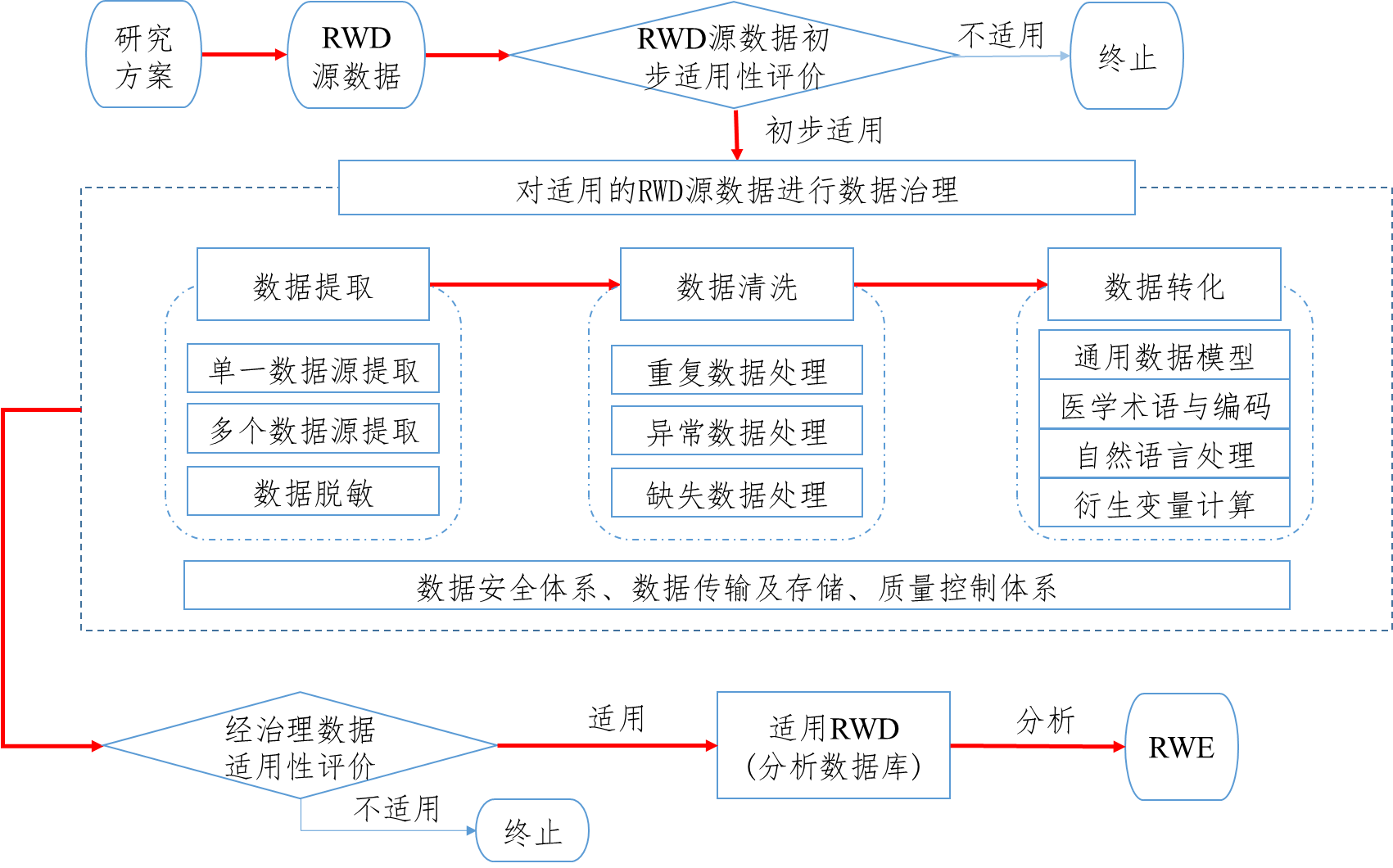
为进一步指导和规范申办者利用真实世界数据生成真实世界证据支持药物研发,我中心组织起草了《用于产生真实世界证据的真实世界数据指导原则(征求意见稿)》,现在中心网站予以公示,以广泛听取各界意见和建议,欢迎
CDE - 真实世界证据,真实世界研究 - 2020-08-03
自体CAR-T细胞治疗产品药学变更研究问题与解答(征求意见稿)
为规范和指导CAR-T类产品的变更研究和申报,我中心形成了《自体CAR-T细胞治疗产品药学变更研究问题与解答(征求意见稿)》。
国家药品监督管理局药品审评中心 - CAR-T - 2023-06-28
《瑞戈非尼片生物等效性研究技术指导原则(征求意见稿)》
为持续完善仿制药生物等效性研究技术指导原则,国家药品监督管理局药品审评中心起草了《瑞戈非尼片生物等效性研究技术指导原则(征求意见稿)》。
国家药品监督管理局药品审评中心 - 瑞戈非尼片 - 2023-08-23
晚期前列腺癌临床试验终点技术指导原则(征求意见稿)
前列腺癌是常见的泌尿系统恶性肿瘤,和其他实体瘤相比具有独特的疾病特征,如按照对雄激素剥夺治疗的敏感性及是否转移分为不同疾病阶段、有高发骨转移及血清生物标志物PSA等,临床试验终点有特殊的定
CDE - 前列腺癌 - 2021-12-09
化学仿制药透皮贴剂药学研究技术指导原则(征求意见稿)
为贯彻《国务院关于改革药品医疗器械审评审批制度的意见》(国发〔2015〕44号)、《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(厅字〔2017〕42号)和国家局、药审中心关于化学药品仿制药的
CDE - 指导原则 - 2020-10-03
SCI 投稿全过程信件模板一览(Cover letter,催稿信等)
一、最初投稿Cover letterDear Editors:We would like to submit the enclosed manuscript entitled “Paper Title”, which we wish to be considered for publication in “Journal Name”. No conflict of interest exits i
MedSci原创 - SCI,投稿 - 2013-04-11
利拉鲁肽用于体重管理的临床试验设计指导原则(征求意见稿)
为引导我国利拉鲁肽产品临床研发体重管理适应症,根据该品种特点及我国临床实践,综合既往讨论意见,在已发布的《利拉鲁肽注射液生物类似药临床试验设计指导原则》和《体重控制药物临床试验技术指导原则(征求意见稿
CDE - 体重 - 2021-09-03
新药研发过程中食物影响研究技术指导原则(征求意见稿)
为进一步鼓励和引导新药研发过程中合理和规范地开展食物影响研究,经广泛调研和讨论,我中心组织起草了《新药研发过程中食物影响研究技术指导原则(征求意见稿)》
CDE - 新药研发 - 2021-08-28
胰岛素类产品药学研究与评价技术指导原则(征求意见稿)
为有效规范和指导胰岛素类产品的研发、生产和注册,明确技术评价标准,保护用药患者的用药安全,我中心在文献查阅、专题研讨、初稿撰写、学术沟通交流的基础上,形成了《胰岛素类产品药学研究与评价技术指导原则(征
CDE - 胰岛素 - 2021-08-23
抗肿瘤药首次人体试验扩展队列研究技术指导原则(征求意见稿)
为进一步规范抗肿瘤药首次人体试验扩展队列研究,我中心组织起草了《抗肿瘤药首次人体试验扩展队列研究技术指导原则(征求意见稿
CDE - 肿瘤,指导原则 - 2021-08-04
为您找到相关结果约500个