JCO:PROSTVAC在转移性去势抵抗性前列腺癌中的III期试验
PROSTVAC是一种基于病毒载体的免疫疗法,在II期研究中,与安慰剂相比,接受治疗的转移性去势抵抗性前列腺癌患者的中位总生存期(OS)延长了8.5个月。
MedSci原创 - 前列腺癌,PROSTVAC - 2019-03-02
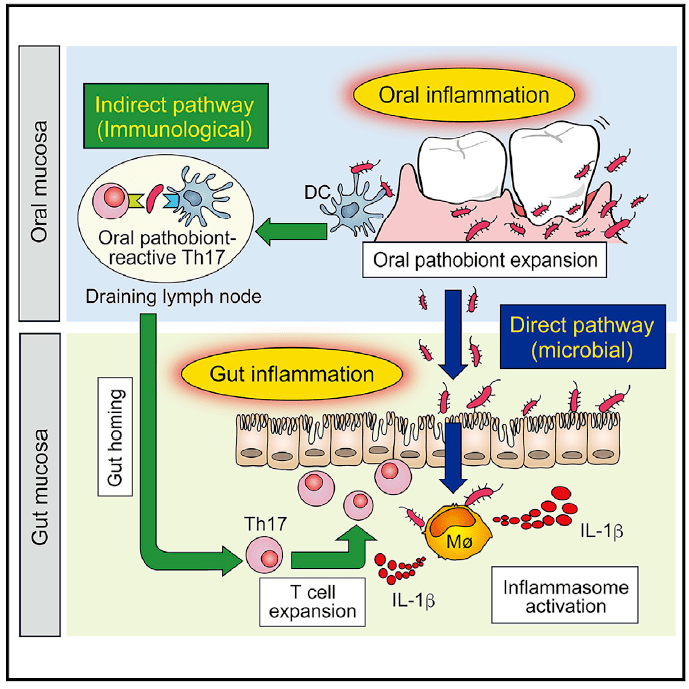
Cell:口腔微生物可能会引发炎症性肠病
不健康的口腔通常能反映出一个人的整体健康状况,甚至可能是发生全身性疾病的原因,包括从心脏病到糖尿病。
MedSci原创 - 炎症性肠病,口腔微生物 - 2020-06-20
FDA 行业指南:急性髓性白血病的开发治疗药物和生物制品
本指南的目的是协助申办者进行用于治疗急性髓细胞白血病(AML)的药物和生物制品的临床开发。具体而言,本指南涉及 FDA 目前关于开发药物的总体开发计划和临床试验设计的想法,以支持 AML 治疗的适应症
FDA - 急性髓性白血病 - 2022-11-11
《EBioMedicine》:家族性脑海绵状畸形的循环生物标志物
普萘洛尔在家族性CCM患者中是安全且耐受性良好,可能有利于降低临床事件的发生率。
MedSci原创 - 脑海绵状畸形 - 2024-01-17
J Endod:负载抗生素壳聚糖水凝胶作为牙髓再生支架的抗微生物活性和生物相容性
这篇研究的目的是为了评估数种负载抗生素水凝胶支架对粪肠球菌的作用以及刺激牙髓干细胞(DPSCs)增殖与分化的能力。
网络 - 生物相容性,抗菌活性,支架材料 - 2020-09-18
PLoS One:Marfan综合征的生物特征和结构性眼部表型!
德国柏林大学医学院心脏病学系的Gehle P近日在PLoS One发表了他们最近的研究工作,他们研究了Marfan综合征(MFS)的生物特征和结构性眼部表型。
MedSci原创 - Marfan综合征,结构性表型,生物特征 - 2017-09-21
JCO:恶性胸膜间皮瘤患者预防性照射:开放标签,多中心,III期随机临床试验
在诊断或治疗后,恶性胸膜间皮瘤(MPM)患者对胸壁进行预防性放射治疗已成为整个欧洲的一种普遍做法,但是这种治疗的疗效尚不确定。
MedSci原创 - 恶性胸膜间皮瘤,预防性辐照 - 2019-03-30
FDA“药物、生物制品和器械去中心化临床试验供企业、研究者和其他利益相关者用的指导原则”介绍
去中心化临床试验(DCT)是指在传统临床试验场所以外的场所进行部分或全部与试验相关活动的临床试验。详细介绍FDA该指导原则草案,期待对中国开展DCT及其监管有所益处。
药物评价研究 - FDA - 2024-01-22
首个人体生物可降解冠脉支架长期安全性获证据
日本研究者4月16日在《循环》(Circulation)在线发表了首个置入人体的生物可降解聚乳酸冠脉支架——Igaki-Tamai支架的长期安全性结果。
医学论坛网 - 生物可降解支架,MACE,心脏 - 2012-04-20
【中文】ICH指导原则:在特定的上市前后期或上市后临床试验中选择性收集安全性数据E19
本指导原则旨在提供关于选择性收集安全性数据的国际协调指南,可用于特定的上市前后期或上市后临床试验。
国家药品监督管理局药品审评中心 - 临床试验 - 2023-10-13
Catheter Cardiovasc Interv:R-ZES在ST-Elevation心肌梗死患者中的安全性和有效性——Resolute-STEMI试验
本研究旨在评估DAPT-STEMI试验(NCT01459627)中入组患者使用第二代Resolute™佐他林洗脱支架(R-ZES)进行初级经皮冠状动脉介入治疗(pPCI)后的安全性和疗效结
MedSci原创 - 心肌梗死,经皮冠状动脉介入术 - 2020-11-13
2022 ASCO 指南更新:转移性乳腺癌全身治疗的生物标志物
更新 ASCO 生物标志物以指导转移性乳腺癌 (MBC) 的全身治疗指南。
Journal of Clinical Oncology - 生物标志物,转移性乳腺癌 - 2022-06-29
Arthritis Rheum:生物制剂治疗类风湿关节炎安全性探索
最近的一项试验显示利妥昔单抗联合肿瘤坏死因子(TNF)拮抗剂和甲氨蝶呤(MTX)治疗活动性类风湿关节炎(RA)患者的安全性与TNF拮抗剂在其他RA试验相一致。
来宝网 - 生物制剂:类风湿,利妥昔单抗 - 2017-08-24
Lancet:临床II期试验表明LCZ696可用于难治性心力衰竭治疗(PARAMOUNT研究)
诺华公布的PARAMOUNT临床II期研究结果表明,针对射血分数保留型心力衰竭 (HF-PEF) 疾病患者,临床试验药物LCZ696可以显著降低与其发病率和死亡率相关的一种关键性预测因子
MedSci原创 - PARAMOUNT,LCZ696,心力衰竭 - 2012-08-28
人源性干细胞及其衍生细胞治疗产品临床试验技术指导原则(征求意见稿)
2019年4月,国家药监局启动了中国药品监管科学行动计划,首批研究项目包括“细胞和基因治疗产品技术评价与监管体系研究”,该项目将通过发布一系列技术指南,建设和完善细
CDE - 指导原则 - 2020-09-01
为您找到相关结果约500个