吸入型干扰素β制剂SNG001降低COVID-19发展为重症的风险
制药公司Synairgen今日宣布,与之安慰剂相比,其吸入型干扰素β制剂SNG001治疗COVID-19患者时,大大降低了患者患上严重疾病的机会。
MedSci原创 - 干扰素β,Covid-19,SNG001 - 2020-07-20
中国原创抗肿瘤药物SNG1153获准美国临床试验
北京盛诺基医药科技有限公司近日收到美国食品药品监督管理局(FDA)通知,公司品种SNG1153获准在美国开展临床试验。SNG1153作为抗肿瘤药物开发,用于晚期癌症患者,是继阿可拉定之后公司又一具有完全自主知识产权的抗肿瘤创新药物。SNG1153是阿可拉定的化学合成衍生物,可以直接杀伤肿瘤,在体外实验观察到SNG1153可抑制肝癌、肺癌、黑色素瘤、多发性骨髓瘤等多种肿瘤细胞系的增殖,在动物实验中,
MedSci原创 - SNG1153,试验 - 2018-10-06
梅斯呼吸疾病进展(第001期)
编者按:梅斯医学将定期进行汇总,帮助大家概览呼吸领域最新进展。下面是呈现给大家的最近一期的呼吸进展。enjoy~
MedSci原创 - 呼吸,新冠 - 2021-05-17
奥斯卡临床医疗指南:助听器 (CG001)
助听器是用来帮助补偿听力损失的放大设备,它们有几种不同的类型。它们包括耳外或耳道内的设备,将声音更有效地送入鼓膜;附着在耳朵骨骼上的装置,通过振动帮助传递声音;还有一种特殊设备可以植入耳朵或头骨,帮助
hioscar - 助听器 - 2022-10-24
造福4亿+,新风口| 海外创业家访谈.001
他领导的创业公司Sensulin,正在研发一种每日仅需用药一次的新型智能胰岛素,目前在中美两国同时开展B轮融资。而十年前就开始与中国合作的Mike非常看重中国市场,希望可以探索更多形式的合作。
medscizl - 2017-10-19
Equillium宣布开发EQ001以治疗狼疮性肾炎
Equillium宣布计划开发EQ001用于治疗狼疮性肾炎(LN)。
网络 - EQ001,狼疮性肾炎,Equillium - 2019-02-27
CTX001获得FDA快速通道资格用于治疗镰状细胞病
CRISPR治疗公司和Vertex制药公司近日宣布,美国食品和药品管理局(FDA)已授予CTX001快速通道资格用于治疗镰状细胞病(SCD)。CTX001是针对患有严重血红蛋白病患者的研究性、自体性、CRISPR基因编辑的造血干细胞疗法。
MedSci原创 - CTX001,镰状细胞病,地中海贫血,CRISPR - 2019-01-10
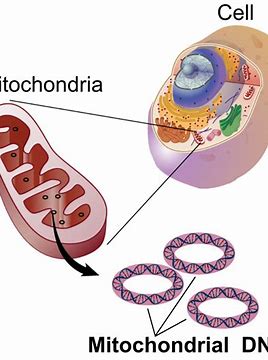
原发性线粒体肌病的治疗:REN001获得FDA孤儿药称号
Reneo Pharmaceuticals今日宣布,美国食品药品监督管理局(FDA)已授予该公司的主要候选药物REN001治疗原发性线粒体肌病(PMM)的孤儿药称号。
MedSci原创 - 原发性线粒体肌病,REN001 - 2020-06-24
FDA批准CMN-001治疗晚期转移性肾细胞癌的IND
CoImmune制药公司今日宣布,FDA批准了CMN-001的研究性新药申请(IND),以推进CMN-001治疗晚期转移性肾细胞癌(mRCC)的IIb期临床试验。
MedSci原创 - CMN-001,FDA,晚期转移性肾细胞癌 - 2020-02-20
JCO:淀粉样变性新药NEOD001初步临床试验结果
NEOD001是一种以这些错误折叠的蛋白质为靶点的单克隆抗体。目前,NEOD001正在进行临床I/II期试验,用于治疗轻链淀粉样变性。 受试者在参与试验时已经至
MedSci原创 - 淀粉样变性,单抗 - 2016-02-09
为您找到相关结果约500个