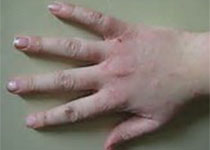
FDA批准Shire血友病药物新增加适应症
12月27日,Shire公告称FDA批准了公司半衰期延长的重组人凝血因子VIII(rFVIII)药物ADYNOVATE(聚乙二醇化重组抗血友病因子),扩大适应症用于12岁及以下A型血友病患儿的治疗,同时批准了该药用于
新浪医药 - FDA,血友病 - 2016-12-30
FDA对抗体生物仿制药产品批准在2019年明显增加
抗体协会的调查结果显示,美国食品和药物管理局(FDA)对生物仿制药抗体治疗药物的批准在2019年显着增加。今年前七个月共批准了六种抗体产品。
MedSci原创 - FDA,抗体生物仿制药,批准增加 - 2019-08-10
BMJ:FDA批准一种临床效果不明显但增加死亡风险的新型抗精神病药物
抗精神病药物brexpiprazole(Rexulti)未能提供具有临床意义的益处,并增加了死亡风险。然而,美国食品和药物管理局(FDA)已经快速批准了它。
MedSci原创 - 抗精神病药物,阿尔兹海默症 - 2023-08-21
JAMA:FDA加速批准药物的预批准研究和批准后研究有无差别?
2017年8月,发表在《JAMA》的一项研究调查了美国食品药物管理局(FDA)加速批准授权药物预批准和批准后研究的特点。研究结果显示,验证性试验和预批准试验具有相似的设计元素,加速批准授权药物的有效性通常在批准后3年内的批准后研究中得到证实。
环球医学 - 药物,FDA - 2017-09-18
新型降脂药Alirocumab获FDA批准和欧洲CHMP批准建议
正如业内广泛预期,6月24日新型降低密度脂蛋白胆固醇(LDL-C)药物Alirocumab(Praluent)获得美国食品与药物管理局(FDA)批准。alirocumab是第一个获得FDA批准的PCSK9抑制剂,尽管业内广泛预期FDA会在接下来几周之内批准另一种PCSK9抑制剂evolocumab。据heartwire
中国医学论坛报 - 新型降脂药,Alirocumab - 2015-07-29
Herz:开滦研究, 腰围增加则高血压风险增加
开滦研究发布最新数据提示,腰围与国人高血压的发病独立相关,随着腰围的增加,高血压发病风险逐渐增加,即使是体重正常和腰围在阈值以下也是如此。 本研究中,BMI<24kg/m2和腰围<80cm者的高血压风险随腰围的增加而增加。 基于以往的研究结果,男性的腰围标准为80.5~95.1cm,女性的腰围标准为71.5~83.7 cm。
中国循环杂志” - 腰围,高血压 - 2016-12-13
体重增加与消化系统癌症风险增加相关
近日发表在《英国癌症期刊》上的一篇研究表明,体重增加是引起两种存活率很低的癌症非常大的风险因素,确诊食道癌或胃癌的患者中只有26%生存超过5年。 美国国家癌症研究所(NCI)的研究人员分析了大约40万人的数据,试图弄清楚体重增加是否与这两种消化系统癌症有关,近年来,这两种癌症的患病率在快速增加。 研究
中国生物技术网 - 体重,消化系统,癌症 - 2017-02-21
JAMA Cardiol:心率小幅增加亦可增加不良事件风险
JAMA Cardiology发表的一项最新研究显示,随时间推移相对较小的心率变化即使在正常范围内也可增加一般人群的不良心血管及非心血管风险。
国际循环 - 心率,不良事件,风险 - 2018-02-03
Heart:体重的增加会增加房颤的发生风险
全球范围内肥胖的发病率逐渐上升,由于肥胖是房颤的危险因素,这也可以部分解释房颤的发病率也呈逐渐上升。本次荟萃分析研究的目的旨在评估体重的变化对房颤的影响。本研究对MEDLINE, Embase, Pubmed, Web of Science, Cochrane Central Register of Controlled Trials, Database of Abstracts of Revie
网络 - 心血管,房颤,肥胖 - 2019-11-23
J Gastroenterology:腰围增加,食道癌的风险也增加!
据报道,通过体重指数(BMI)衡量的总体肥胖与食道鳞状细胞癌(ESCC)风险之间存在负相关关系。然而,以腰围(WC)衡量,ESCC(在韩国约占食管癌的90%)与腹部肥胖的关系可能不同。因此,本项
MedSci原创 - 肥胖,食管癌,腰围 - 2020-03-08
PLOS MED:增加烟草税,健康收益增加,医疗支出减少
提高烟草税有许多好处,比如完善政府的职责与功能、可以增加政府额外的税收收入并且可以以此收入来资助其他方面的控烟工作。
MedSci原创 - 烟草税,医疗 - 2015-07-29
美国批准首个基因疗法
美国政府8月30日批准一种基于改造患者自身免疫细胞的疗法治疗白血病,这是第一种在美国获得批准的基因疗法。专家认为,这开辟了癌症治疗的新篇章。
健康报 - 基因疗法 - 2017-09-01
FDA批准了第一种增加红细胞生成性原卟啉病患者无痛光照的黑色素生成药Scenesse
Scenesse(afamelanotide)获得美国食品和药物管理局的批准,用于增加罕见病——红细胞生成性原卟啉病成年患者的无痛光照,该类患者具有的光毒反应史。
MedSci原创 - 红细胞生成性原卟啉病,无痛光照,黑色素生成药,Scenesse - 2019-10-14
FDA 指南:关于已批准/已批准医疗产品的未批准用途的科学信息,公司与医疗保健提供者的通信行业问答指南
本修订后的指南草案定稿后,将提供FDA目前对公司向医疗保健提供者(HCPs)通报已批准/已批准医疗产品未批准用途(SIUU)的19项科学信息的18个常见问题的看法。
FDA官网 - FDA - 2023-10-26
为您找到相关结果约500个





_1583672517000.jpeg?x-oss-process=image/resize,m_fill,w_250,h_175,limit_0)