Eur. J. Cancer:三氟尿苷/替吡拉西(FTD/TPI)治疗转移性乳腺癌的II期研究(无论先前是否接受过氟嘧啶治疗)
2023-08-30 daikun MedSci原创 发表于上海
该研究旨在评估三氟尿苷/替吡拉西(FTD/TPI)治疗转移性乳腺癌的疗效和安全性(无论先前是否接受过氟嘧啶治疗),结果显示FTD/TPI显示出有希望的抗肿瘤活性,毒性可控,是MBC患者的临床有效选择。
转移性乳腺癌(MBC)的治疗结果仍然令人沮丧,IV期MBC的中位总生存期(OS)约为31个月。化疗是护理治疗的标准,激素受体阳性癌症患者还可以选择内分泌治疗和/或靶向治疗,最近还考虑了三阴性乳腺癌患者的免疫治疗。在治疗化疗患者时,序贯单药治疗通常是首选,因为与序贯单药治疗相比,没有研究表明联合治疗具有令人信服的OS益处。
多种活性化学治疗剂可用于治疗MBC,包括紫杉烷类,蒽环类,氟嘧啶类,吉西他滨,艾瑞布林和长春瑞滨。FTD/TPI是一种口服活性抗肿瘤药物组合,由三氟尿苷(一种基于胸苷的核苷类似物)和替吡拉西(一种胸苷磷酸化酶抑制剂)组成,可防止三氟尿苷的快速降解,从而增加对活性剂的暴露。
有趣的是,FTD/TPI在结直肠癌和胃癌患者之前暴露于其他氟嘧啶后显示出活性,尽管之前进行了氟嘧啶治疗,但在III期治疗中OS获益,导致其获得美国(美国)食品药品监督管理局(FDA)批准用于治疗结直肠癌和胃癌患者。
虽然FTD/TPI已被研究并发现在治疗难治性MBC患者的I期研究中具有活性,但尚未在较大的II/III期试验中进行研究。基于在转移性结直肠癌中观察到的临床活性,假设FTD/TPI可能在MBC患者中有活性,即使之前接触过其他常用的氟嘧啶,如卡培他滨,5-氟尿嘧啶,因此报告了一项单臂II期研究,评估FTD/TPI在MBC患者中的作用。

方法:MBC患者首先进入磨合剂量确认阶段,然后是两个平行队列,包括(队列a)暴露于和未(队列B)暴露于氟嘧啶的患者,他们接受FTD/TPI治疗。每个队列的主要终点包括确定无进展生存期(PFS),次要终点包括确定客观缓解率(ORR),安全性和耐受性。
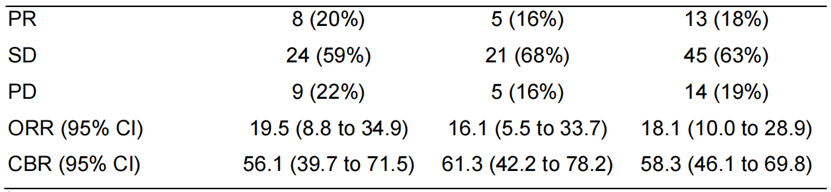
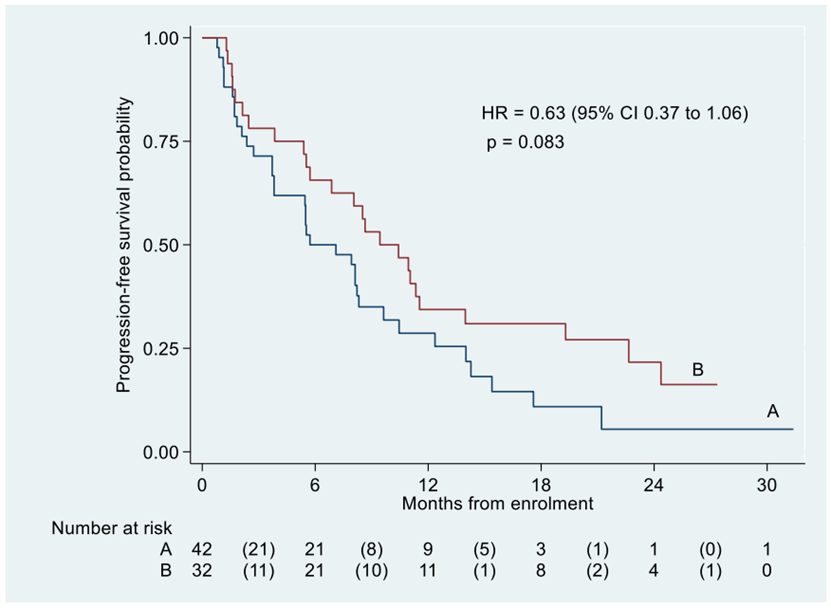
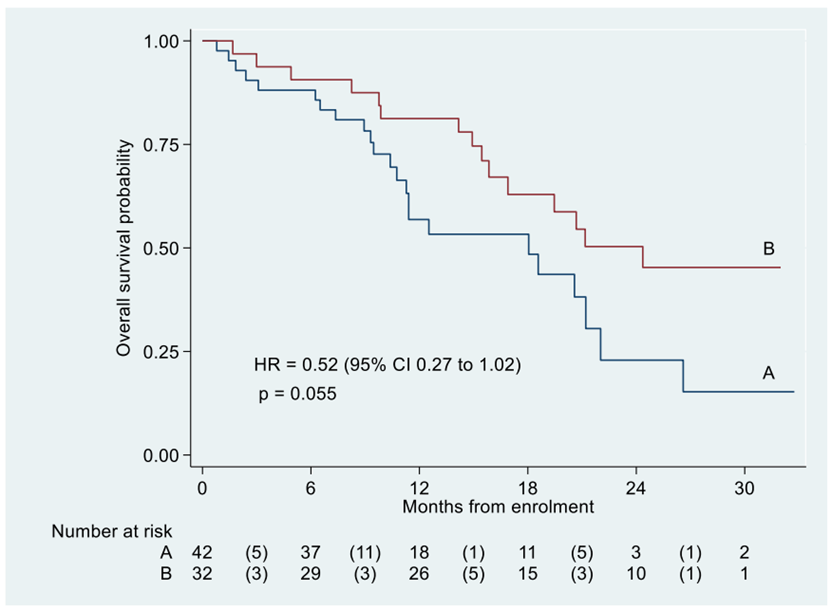
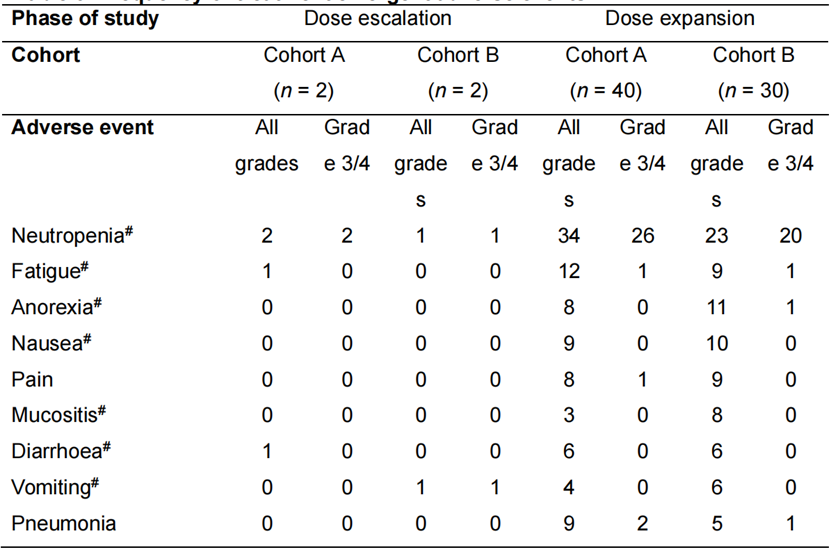
研究结果:招募了74名患者(42名队列A,32名队列B),所有患者的毒性和生存率均可评估,其中72名可评估反应。A组和B组的中位PFS分别为5.7个月(95%可信区间3.8-8.3)和9.4个月(95%可信区间5.5-14.0)。无论先前是否接触氟嘧啶,均观察到反应,A组和B组的ORR分别为19.5%(95%CI 8.8至34.9)和16.1%(95%CI 5.5至33.7),6个月的临床获益率分别为56.1%(95%CI 39.7至71.5)和61.3%(95%CI 42.2至78.2)。安全性与FTD/TPI的已知毒性一致,包括中性粒细胞减少症,疲劳,恶心和厌食症,并通过剂量调整得到缓解。

结论:FTD/TPI显示出有希望的抗肿瘤活性,毒性可控,是MBC患者的临床有效选择。
原始出处:
Lim JSJ, et al. 2023. Phase II study of Trifluridine/Tipiracil (FTD/TPI) in metastatic breast cancers with or without prior exposure to fluoropyrimidines. European Journal of Cancer:113311. DOI: 10.1016/j.ejca.2023.113311.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言