新一代靶向药物在中国获批 肺癌患者迎来新希望
勃林格殷格翰中国总部 27 日在上海宣布,第二代 EGFR 靶向药物阿法替尼已在国内获批,为中国的肺癌患者带来了新的希望。
中国新闻网 - 肺癌,靶向药,阿法替尼 - 2017-02-28
强生的抑郁症药物Spravato鼻喷雾剂,在欧洲获批
强生的抑郁症药物Spravato(esketamine)鼻喷雾剂,已在欧洲被批准用于治疗患有抗药性重度抑郁症的成年人。欧盟委员会(EC)批准该药物与选择性5-羟色胺再摄取抑制剂(SSRI)或5-羟色胺和去甲肾上腺素再摄取抑制剂(SNRI)结合使用,用于对至少两种抗抑郁药没有反应的成年患者。
MedSci原创 - 强生,抑郁症,Spravato,鼻喷雾剂,欧洲获批 - 2019-12-21
临床急需,国内首个法布雷病特效药物法布赞在华获批
作为国内首个获批的法布雷病特效药,法布赞填补了国内特异性治疗药物的空白和临床未被满足的需求,可长期稳定肾功能、减轻疼痛、改善患者生存质量,使患者回归正常生活成为可能。
医谷 - 法布雷病,特效药 - 2019-12-20
新型抗抑郁药SpravatoFDA获批
一般来说,重性抑郁症患者如果既往至少接受过两种适当剂量的抗抑郁药物治疗,但效果不佳,则被视为难治性抑郁症。这是一种严重危及生命的精神疾病,患者自杀、自残的风险极高。这些患者占多大比重呢?
汉鼎好医友 - 抑郁药 - 2019-03-11
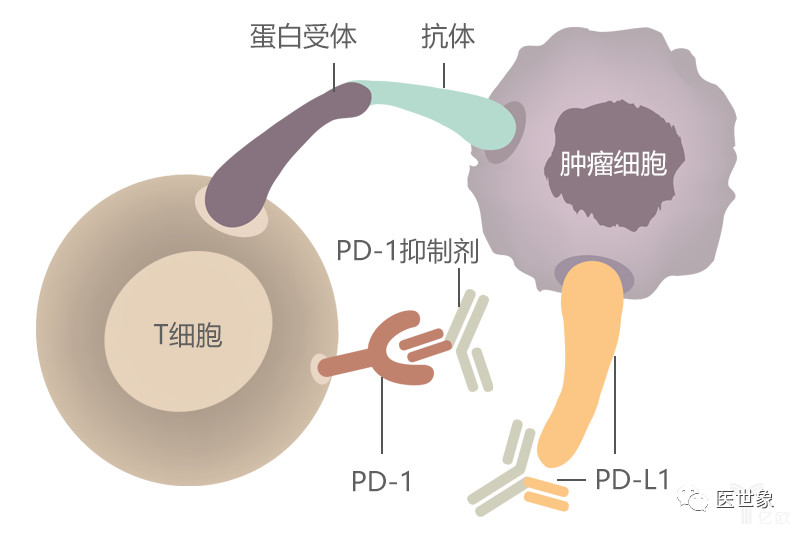
首个国产PD-1抗体药物——君实生物特瑞普利单抗获批!
从3月8日递交上市申请,到今天以优先审评方式获批,第一家国产PD-1的中国上市审批过程历时284天。
国家药品监督管理局、医药魔方Plus - 癌症,PD-1,获批,单抗 - 2018-12-17
辉瑞抗体偶联药物Mylotarg欧洲获批用于治疗急性髓细胞白血病
欧洲食品药品监督管理局批准Mylotarg与柔红霉素和阿糖胞苷联合使用,用于治疗CD33阳性的急性髓细胞白血病(AML)患者,不包括急性早幼粒细胞白血病。
MedSci原创 - 急性髓细胞白血病,Mylotarg,抗体偶联药物 - 2018-04-25
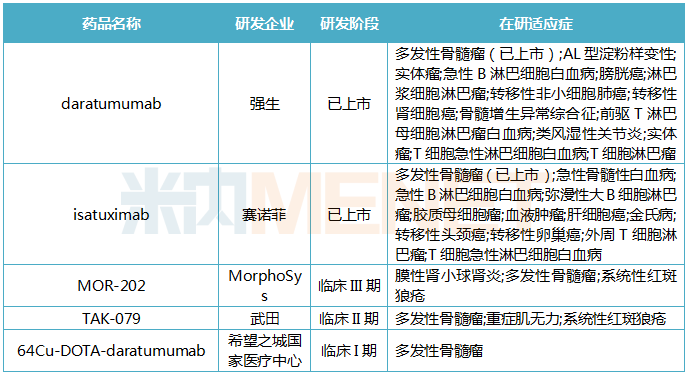
FDA:审批了3款创新药获批,罕见病药物市场热潮涌动
根据美国FDA官网公布的消息,2020年3月FDA批准3款创新药物,分别是赛诺菲公司的Sarclisa,Recordati公司的Isturisa,以及百时美施贵宝公司的Zeposia。2020年一季度
米内网 - 2020-04-04
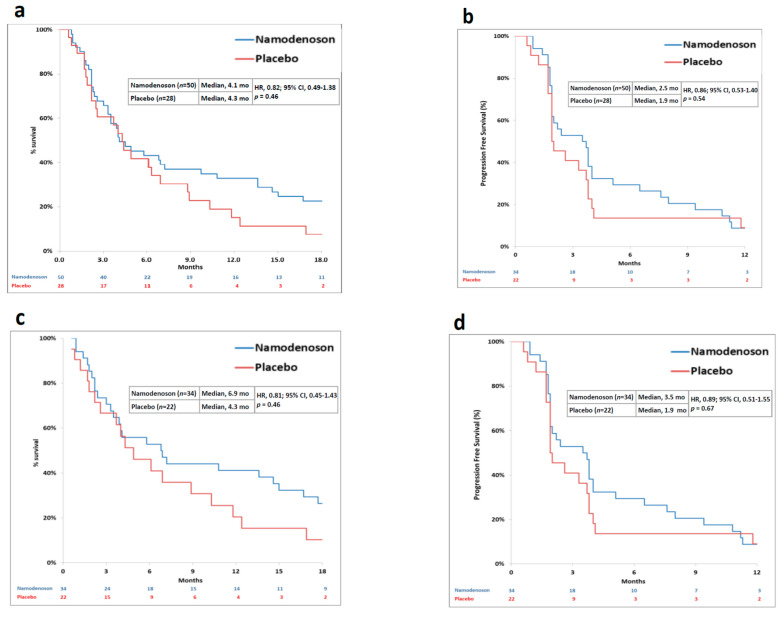
肝癌药物Namodenoson在罗马尼亚获批作为同情用药治疗晚期肝癌
制药公司Can-Fite BioPharma宣布,旗下在研肝癌药物Namodenoson在罗马尼亚获批作为同情用药治疗晚期肝癌患者,已有一位接受治疗的患者完全缓解,全身的转移灶全都消失。
MedSci原创 - 肝癌 - 2022-08-24
君实TIGIT 单抗获批临床
1月27日,君实生物发布公告称,其抗TIGIT 单抗JS006注射液临床试验申请已获得NMPA批准。用以开展晚期实体瘤治疗研究。
医药魔方 - 实体瘤 - 2021-01-29
Amicus的Galafold在美国获批
Amicus Therapeutics的Galafold已被美国批准为首个用于治疗成人法布瑞式症的口服药物。医生现在可以根据实验室数据为成年人患者开具药物,这些患者的基因突变被确定为对Galafold治疗有反应。
MedSci原创 - Amicus的Galafold - 2018-08-14
AZ的Lokelma在美国获批
该药物是一种不溶于水、不被吸收的化合物,其结构被设计成优先捕获钾离子,而此前由于生产问题,它曾两次被监管机构否决。对于慢性肾脏疾病患者以及那些采用普通救命药物治疗心力衰竭的患者,发生高血钾的风险显着增加,如肾素 - 血管紧张素 - 醛固酮系统(RAAS)抑制剂,可增加血液中的钾含量。为了帮助预防高钾血症
MedSci原创 - AZ,Lokelma - 2018-05-21
帕博利珠单抗获批新增剂量方案 适用在华获批的6个适应证
3月17日,中国国家药品监督管理局(NMPA)批准了默沙东PD-1抑制剂帕博利珠单抗(商品名:可瑞达®)新增400mg每6周一次(Q6W)的剂量方案,适用于该药物目前在国内获批的全部6个适应证,覆盖肺
medsci - 帕博利珠单抗 - 2021-03-17
中国首个胃癌免疫治疗药物欧狄沃®获批, 生存期显著延长
2020年3月13日,百时美施贵宝今日宣布,欧狄沃(纳武利尤单抗注射液)已正式获得中国国家药品监督管理局批准用于治疗既往接受过两种或两种以上全身性治疗方案的晚期或复发性胃或胃食管连接部腺癌患者。
medsci - 2020-03-13
FDA委员会:安全性问题不妨碍赛诺菲MS药物Lemtrada的获批
FDA顾问委员会周三举行会议,认为赛诺菲(Sanofi)开发的实验性多发性硬化症(MS)药物Lemtrada的安全性问题,并不妨碍(preclude)该药的批准,但该委员会对相关临床研究的质量表示了担忧
生物谷 - 新药,FDA - 2013-11-20
为您找到相关结果约500个