FDA指南:医疗器械510(k)提交的电子提交模板
本指南规定了以电子格式提交上市前通知(510(k))的标准、制定这些标准的时间表,以及为满足法定要求而豁免和豁免要求的标准。该指南还旨在代表FDA对开发电子提交模板的承诺的几个步骤之一,该模板可作为行
FDA官网 - 医疗器械 - 2023-12-06
AbbVie向美国提交risankizumab
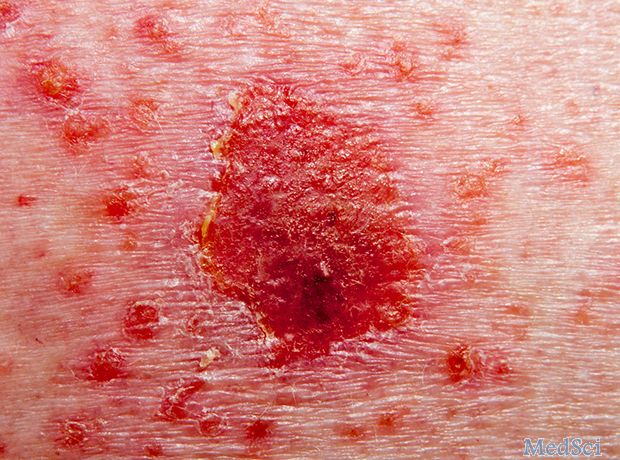
AbbVie已在美国提交risankizumab,寻求批准其用于治疗中度至重度斑块型银屑病。这项提交得到了四项III期研究的支持,涉及2000多名患有该病的患者,数据显示,接受该药物的患者中有一半以上在一年内实现了完全皮肤清除(PASI 100)。AbbVie研发部门首席科学官执行副总裁Michael Severino表示:"risankizumab提交是我们推进免疫介导疾病患者治疗目标的重要里程
MedSci原创 - risankizumab - 2018-04-29
FDA指南:在上市前通知中提交和审查无菌信息(510(k))标记为无菌的器械提交
本指导文件还提供了有关我们建议申办者在 510(k) 提交中包含的热原性信息的详细信息。
FDA官网 - 无菌 - 2024-01-14
武田在日本提交甲吡唑新药申请
武田(Takeda)12月25日宣布,已向日本卫生劳动福利部(MHLW)提交了甲吡唑(fomepizole)的新药申请(NDA),该药用于治疗乙二醇(ethylene glycol)和甲醇(methanol
生物谷 - 新药,FDA - 2013-12-26
GSK提交药物Promacta的补充新药申请
葛兰素史克(GSK)2月28日宣布,已向FDA提交了药物Promacta(eltrombopag,艾曲波帕)的补充新药申请(sNDA),寻求批准该药用于对免疫抑制疗法(IST)响应不足的重型再生障碍性贫血Promacta sNDA的提交,是基于一项开放标签II期NIH
生物谷 - 新药,FDA - 2014-03-04
赛诺菲计划重新提交单抗药Lemtrada sBLA
赛诺菲(Sanofi)及旗下健赞(Genzyme)4月7日宣布,经过与FDA之间富有建设性的讨论,计划于第二季度重新向FDA提交单抗药物Lemtrada(alemtuzumab,阿伦单抗)的补充生物制品许可申请此次sBLA的提交,将提供对FDA于2013年12月27日完整回应函(CRL)中所指出问题的回复。 去年12月,FDA审查后发现,L
生物谷 - 新药,FDA - 2014-04-08
【FDA指南分享】在上市前通知中提交和审查无菌信息(510(k))标记为无菌的器械提交
本指导文件还提供了有关我们建议申办者在 510(k) 提交中包含的热原性信息的详细信息。
网络 - 2024-01-17
百时美向FDA提交丙肝新药NDA
百时美施贵宝(BMS)4月7日宣布,已向FDA提交了实验性丙肝药物daclatasvir(DCV)和asunaprevir(ASV)的新药申请(NDA),daclatasvir是一种实验性NS5A复制复合物抑制剂
生物谷 - 新药,FDA - 2014-04-08
武田在日本提交TAK-438新药申请
武田(Takeda)3月3日宣布,已向日本劳动卫生福利部(MHLW)提交了实验性胃酸分泌抑制剂TAK-438(通用名:vonoprazan富马酸)的新药申请(NDA),该药属于钾离子(K+)竞争性酸阻滞剂
生物谷 - FDA,武田,TAK-438 - 2014-03-05
百特向FDA提交HyQvia修正版BLA
百特(Baxter)12月2日宣布,已向FDA提交了有关HyQvia的一份修订版生物制品许可申请(BLA),以便重新启动关于HyQvia治疗原发性免疫缺陷(primary immunodeficiency
生物谷 - 新药,FDA - 2013-12-04
吉利德提交丙肝新药Ledipasvir/Sofosbuvir新药申请
吉利德(Gilead)2月10日宣布,已向FDA提交了ledipasvir(LDV)+sofosbuvir(SOF)固定剂量组合片剂(LDV/SOF,90mg/400mg)新药申请(NDA),该药开发用于基因型LDV/SOF NDA的提交,
生物谷 - 新药,FDA - 2014-02-13
FDA医疗器械 510(k) 提交的电子提交模板
FDA 正在发布这份指导文件草案,以向器械和放射健康中心 (CDRH) 和生物制品评估与研究中心 (CBER) 介绍上市前通知 (510(k)) 提交者的当前资源和相关内容开发和公开以支持向 FDA
FDA - 医疗器械 - 2021-10-24
现场警报报告提交:FDA行业问答指南
本指南提供了 FDA 当前关于新药申请 (NDA) 和简易新药申请 (ANDA) 申请人提交现场警报报告 (FAR) 要求的想法,并概述了 FDA 对 FAR 提交的建议,以帮助提高其一致性和相关性。
FDA - 现场 - 2021-10-24
FDA:近红外分析程序的开发和提交
本指南为申请人提供建议,以帮助开发、验证和使用基于近红外 (NIR) 的分析程序来评估原料药和药品的特性、强度、质量、纯度和效力。这些建议适用于新药申请 (NDA)、缩写新药申请 (ANDA) 以及小
FDA - 药物分析 - 2021-10-25
葛兰素史克提交Albiglutide上市申请
葛兰素史克公司于2013年3月7日表示,已向欧洲药监部门提交了旗下每周注射一次的糖尿病新药Albiglutide的上市申请,力求能在竞争激烈的糖尿病药物市场占有一席之地。
丁香园 - 糖尿病,Albiglutide,GLP-1 - 2013-03-09
为您找到相关结果约500个