FDA批准CAR-T细胞疗法Tecartus治疗复发难治套细胞淋巴瘤
2020-07-25 Allan MedSci原创
Tecartus是第一个获批用于治疗MCL的CAR-T细胞疗法。
吉利德科学公司旗下的Kite近日宣布,FDA已批准CAR-T细胞疗法Tecartus(brexucabtagene autoleucel)(也称为KTE-X19)治疗复发难治套细胞淋巴瘤(MCL),Tecartus是第一个获批用于治疗MCL的CAR-T细胞疗法。这是美国FDA批准的第三款细胞治疗方法。
吉利德在美国获批的首个CAR-T细胞疗法是Yescarta(axicabtagene ciloleucel),该药已于2017年被FDA批准用于大B细胞淋巴瘤患者。
FDA的这项决定是基于ZUMA-2研究的最新结果,该研究招募了74例曾经接受过蒽环类、苯达莫司汀化疗、抗CD20抗体治疗和BTK抑制剂的患者。结果显示,在60例可评估患者中,有87%的患者对Tecartus输注有反应,其中62%的患者获得了完全缓解。Tecartus带有框状警告,提示细胞因子释放综合征和神经系统毒性的风险。FDA还要求Kite对用该疗法进行上市后观察研究。
Kite指出,在ZUMA-2试验中,该公司从白细胞分离术到交付的平均时间为15天,制造成功率为96%。
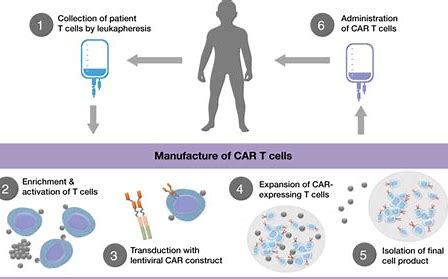
这款最新获批的CAR-T细胞疗法就是针对复发或者难治的MCL患者,获批的依据则是最新的临床研究数据——在这项共计有74名成年MCL患者入组参与的Zuma-2临床试验中,对于疗效可评估的60例患者进行了6个月的随访,结果显示该疗法达到了超出预期的治疗效果:
-
在初次注射CAR-T细胞之后,87%的患者产生直接的治疗反应;
-
接受治疗的患者,有62%的患者完全缓解,包括肿瘤完全消失。
而正是基于这一数据,最终让这款药物获得了FDA批准,可以用于复发难治的MCL患者的治疗,同时该药也通过了优先审查和加速审批,才得以如此迅速的和患者见面。
当然对于CAR-T细胞疗法比较常见的副作用,包括细胞因子风暴(CRS)和神经毒性,这款获批的疗法同样也存在,一般在接受治疗后的第一周~第二周出现。此外还可能出现的副作用包括:严重感染、血细胞计数低等。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#TEC#
38
厉害啊
87
#细胞淋巴瘤#
38
#复发难治#
42
#CAR-#
36
#FDA批准#
0
学习了,谢谢🙏
79
#Car-T细胞疗法#
35
#ART#
33
#cART#
57