【Hematol Oncol】中国多中心研究:HBV相关MCL的治疗模式、临床结局和基因突变
2024-05-05 聊聊血液 聊聊血液 发表于上海
中国8家中心开展回顾性分析,分析了2001-2020年期间684例初诊MCL患者的临床数据,并分析了乙型肝炎表面抗原阳性(HBsAg+) MCL患者的临床特征、预后、治疗模式、生存结局和基因突变特征。
HBV相关MCL
套细胞淋巴瘤(MCL)是一种罕见且无法治愈的B细胞淋巴瘤亚型,病程具有侵袭性,仍然无法治愈。乙型肝炎病毒(HBV)感染与B细胞淋巴瘤的风险增加有关,并且具有独特的临床和遗传特征。
中国8家中心开展回顾性分析,分析了2001-2020年期间684例初诊MCL患者的临床数据,并分析了乙型肝炎表面抗原阳性(HBsAg+) MCL患者的临床特征、预后、治疗模式、生存结局和基因突变特征。该研究是目前唯一关注HBsAg+ MCL患者的研究,结果近日发表于《Hematological Oncology》。

研究结果
HBsAg+ MCL患者特征
该研究共纳入684例初诊MCL患者,其中9.5%的患者为HBsAg+ (64/684),高于一般人群(7.16%)。诊断时的中位年龄为57岁。87%(56/64)的患者为III/IV期,37%为高危MIPI, 39%为血红蛋白<100g/L, 19%为血小板减少症(血小板<100x109/L),39%在诊断后24个月内进展(POD24)。HBsAg+ MCL患者乳酸脱氢酶(LDH)升高的发生率 (50.0% vs 36.9%;p=0.041)高于HBsAg-患者。在初始治疗中接受利妥昔单抗治疗的HBsAg+患者比例显著低于HBsAg-患者(56% vs. 72%,p=0.008),但客观缓解率(ORR)无显著差异(83% vs. 77%,p=0.367)(表1)。共评估了153个T淋巴细胞亚群,CD19+、CD3+、CD4+、CD8+、CD4+/CD8+或CD16+CD56+细胞在HBsAg+患者和HBsAg-患者之间无差异
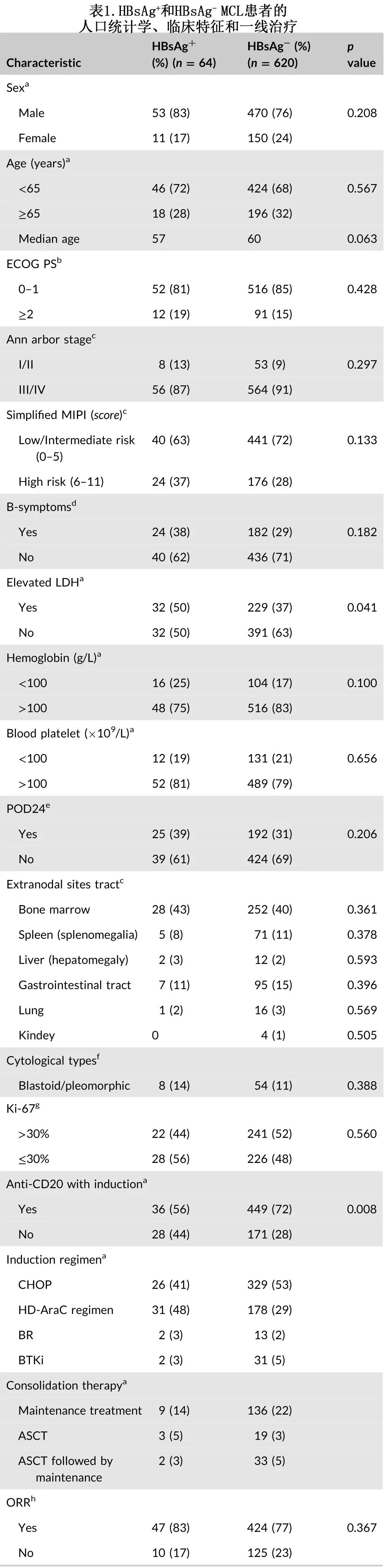
HBsAg+ MCL患者的预后因素
中位随访31个月(2.6年),2年PFS率和5年OS率分别为50%和48%。根据单因素回归分析,较短的PFS与高危MIPI (p=0.007)、血小板<100x109/L (p=0.002)和未使用HD-AraC (p=0.018)相关,而较短的OS与高危MIPI (p=0.011)、骨髓受累(p=0.008)和血小板计数<100x109/L (p<0.001)相关。根据多因素回归分析,较短的PFS与血小板<100x109/L和未使用HD-AraC相关,而较短的OS仅与血小板计数<100x109/L相关。
HBsAg+ MCL患者的治疗模式和生存结局
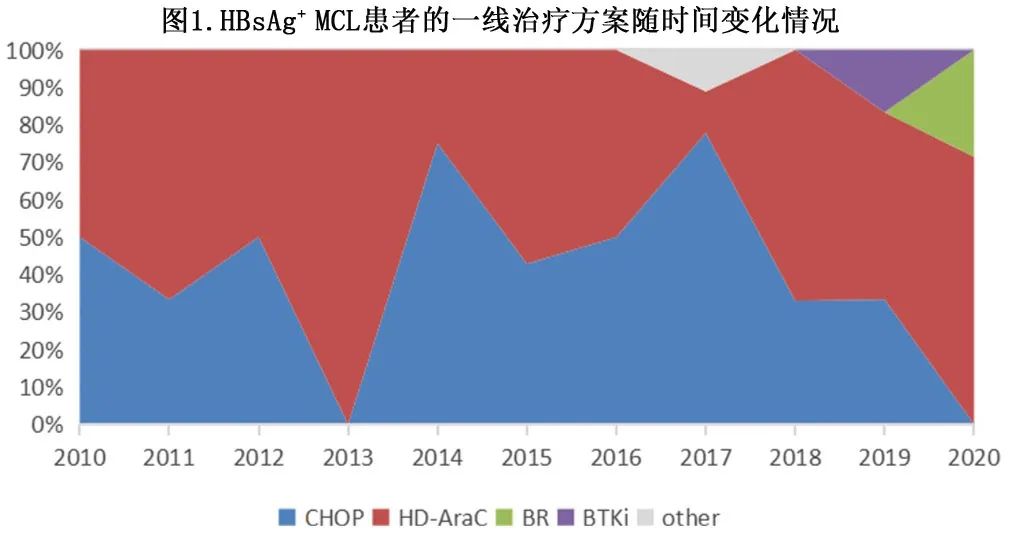
54%的年轻患者接受HD-AraC±R方案,而44%的老年患者接受CHOP±R方案。2010年至2020年,HBsAg+患者的化疗方案没有明显变化,CHOP和HD-AraC方案是主要化疗方案(图1)。此外22%的患者接受了巩固治疗(表1)。
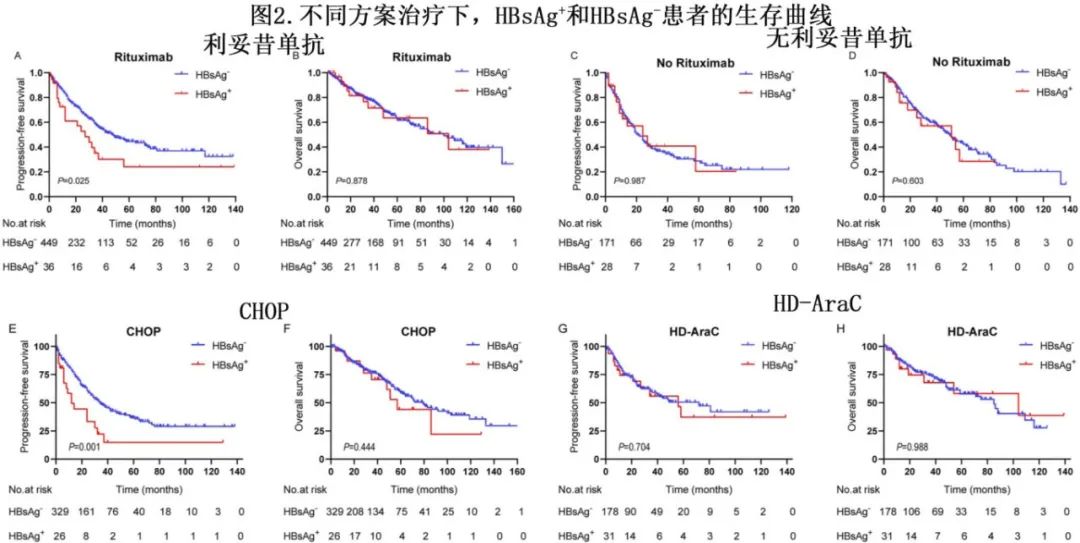
对不同诱导方案的生存结局进行亚组分析。在接受利妥昔单抗诱导化疗的患者中,HBsAg+患者的PFS明显劣于HBsAg-患者(HR=0.56;P=0.025;图2A),而OS差异无统计学意义(HR=1.05;P=0.878;图2B)。在未接受利妥昔单抗治疗的患者中,PFS和OS无显著差异(图2C,D)。在接受CHOP诱导化疗的患者中,HBsAg+患者的PFS明显劣于HBsAg-患者(HR=2.56;P=0.001;图2E),但OS无差异(HR=1.29;P=0.444;图2F)。在接受HD-AraC化疗的患者中,PFS (HR=1.09;p=0.704,图2G)和OS (HR=1;P=0.988;图2H) 无差异。
与CHOP诱导相比,HD-AraC方案与更长的PFS相关(HR=0.4;p=0.017,图3A),其中R‐HD‐AraC与HD‐AraC的PFS无显著差异(HR=0.72;p=0.569,图3B)。CHOP方案的POD24率为56%,而HD-AraC方案为32%。
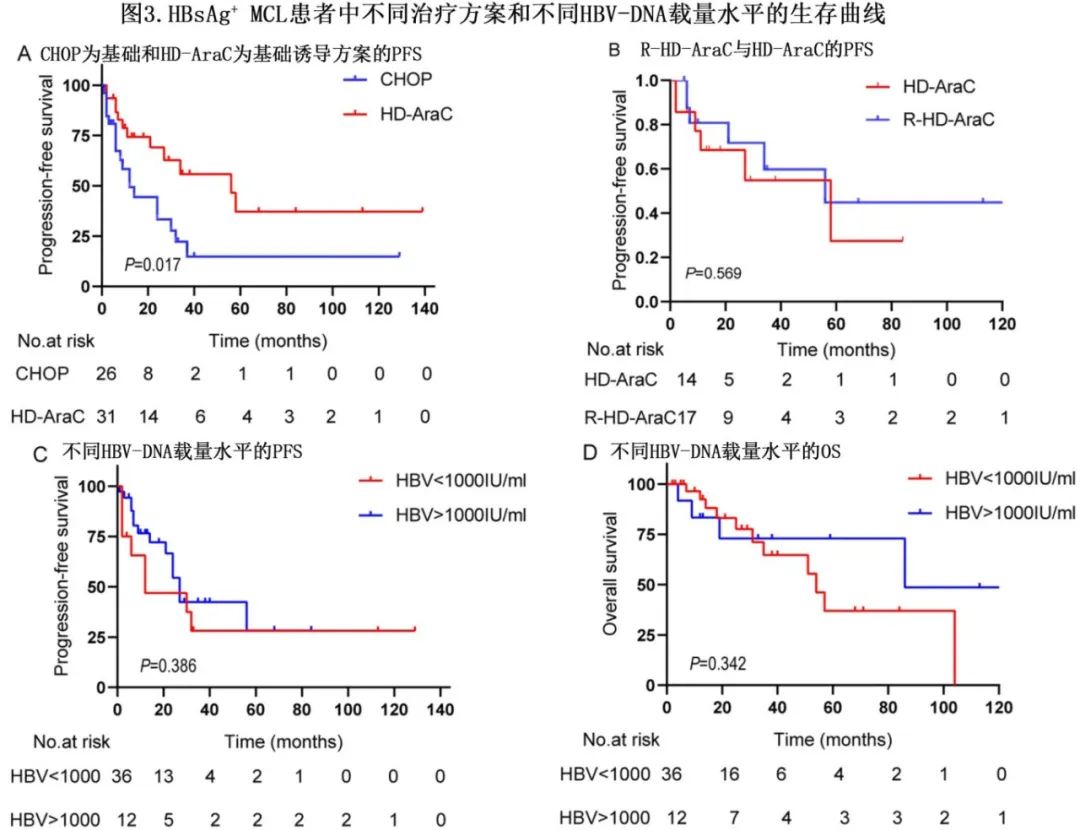
共48例HBsAg+患者在基线时进行了HBV‐DNA评估,对于不同HBV‐DNA载量水平的患者(≥1000 IU/mL的12例患者vs <1000 IU/mL的36例患者),其PFS (HR=1.48;p=0.386,图3C)或OS (HR=0.56;p=0.342,图3D) 均无显著差异。
HBV再激活
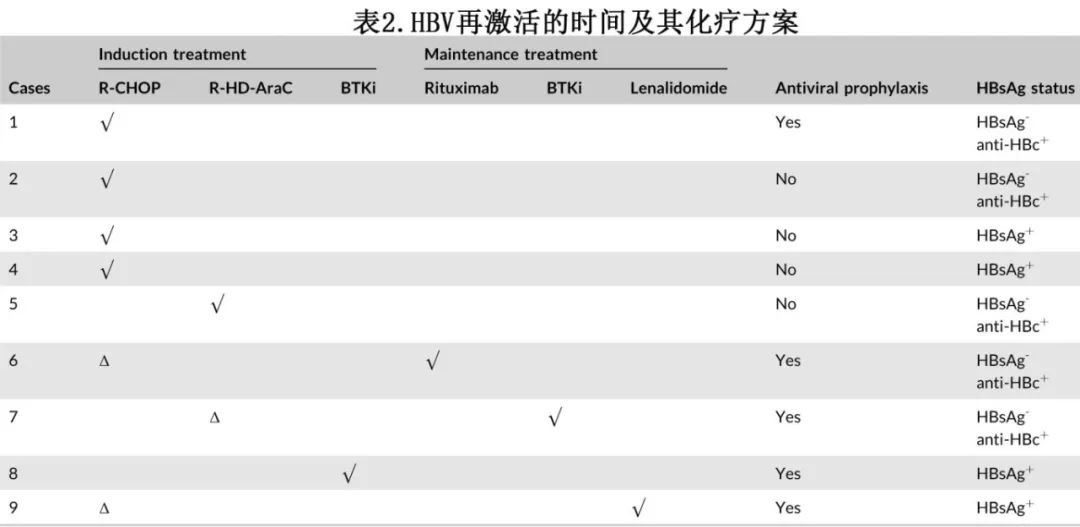
在64例HBsAg+(慢性乙型肝炎)和163例HBsAg+但抗HBc+ (乙型肝炎恢复)MCL患者中,9例(4%)患者发生HBV再激活(HBsAg+中3例和HBsAg+但抗HBc+中6例)。其中44%的患者未使用抗病毒治疗。在诱导化疗期间,56% (n=5)的患者发生HBV再激活,均接受利妥昔单抗为基础的化疗(R‐CHOP组4例,R‐HD‐AraC组1例)。44% (n=4)的患者接受了利妥昔单抗(n=2)、BTKi (n=1)或来那度胺(n=1)维持治疗(表2)。除1例仅接受BTKi治疗的患者外所有HBV再激活的患者均接受了利妥昔单抗治疗。
HBsAg+ 和HBsAg- MCL患者的突变谱
74例患者中共检测到3029个细胞突变,涉及410个基因,中位突变负荷为0.68/Mb。在整个队列中,错义突变发生频率最高,其次为移码突变、无义突变、剪切位点突变和框内突变。突变频率最高的前10位基因分别为NQO1(72%)、MTHFR(70%)、KMT2D(69%)、TCF3(59%)、XRCC1(59%)、ATM(50%)、DPYD(50%)、KMT2C(45%)、GSTP1(46%)和ASXL1(45%)。
基于靶向深度测序(TDS)比较了HBsAg+ 和HBsAg-患者的基因组差异。74例MCL患者样本中有5例来自HBsAg+患者。HBsAg+ MCL患者的非同义突变突变负荷大于HBsAg-患者(图4B)。HBsAg+样本中每个样本的平均非同义突变数为57.4个,而HBsAg-样本为39.5个。然后比较HBsAg+和HBsAg- MCL患者中不同突变频率的基因,HBsAg+ MCL患者中HDAC1、TRAF5、FGFR4、SMAD2、JAK3、SMC1A、ZAP70、BLM、CDK12、PLCG2、SMO、TP63、NF1、PTPR、EPHA2、RPTOR和FIP1L1浓度显著较高(图4A、C)。接下来比较了HBsAg+ 和HBsAg-患者受突变影响的信号通路的差异,发现PI3K信号、染色质组蛋白修饰因子、染色质SWI/SNF复合物和基因组完整性相关的变化在5例HBsAg+ MCL患者中富集。表观遗传修饰相关变化的频率与在特定基因中观察到的突变相似。此外,在HBsAg+ MCL患者中,细胞周期、TGFβ信号通路和MTOR信号通路的改变率更高(图4D),可能表明HBsAg+ MCL患者具有更复杂的信号通路失调。
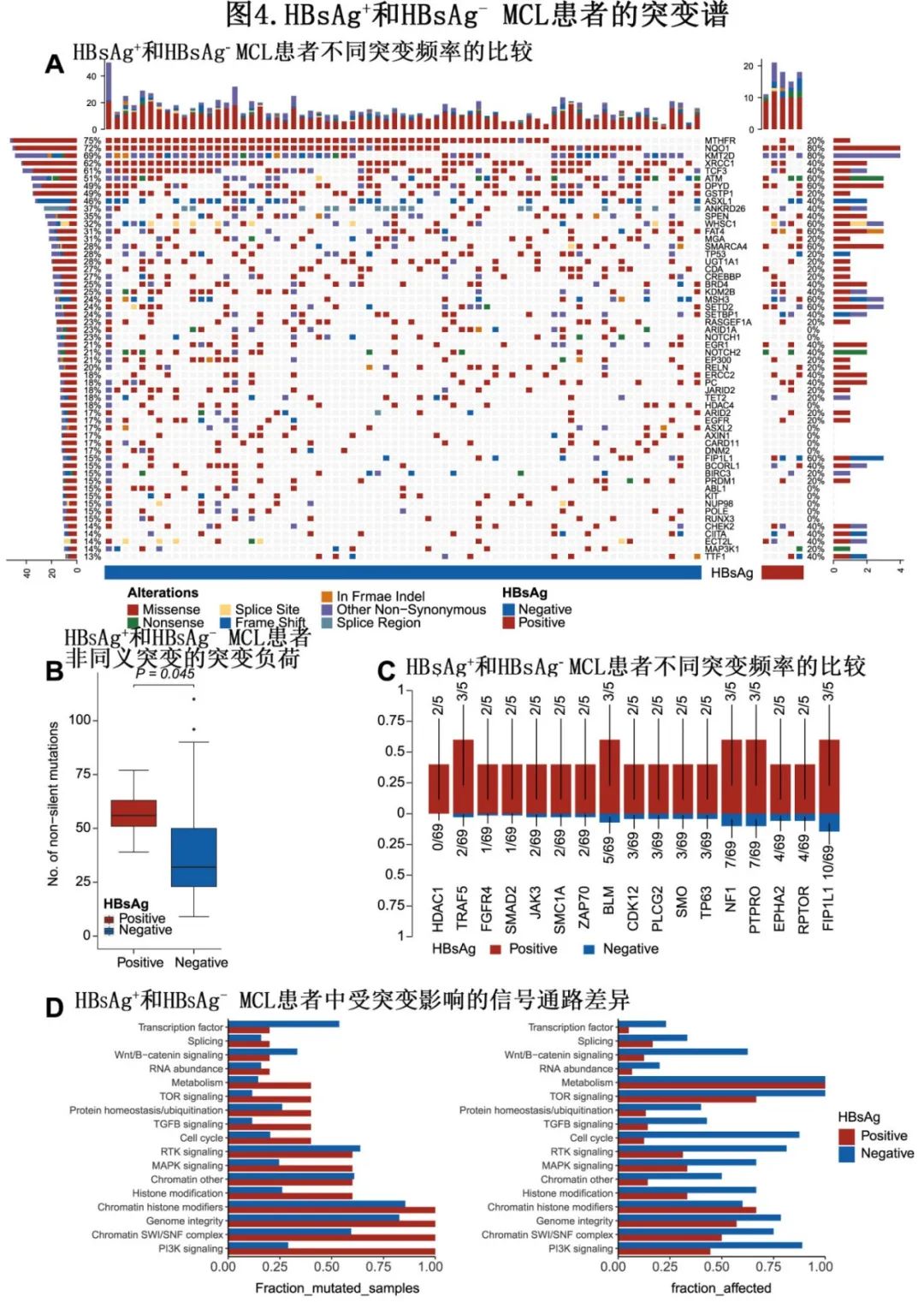
此外,根据突变基因和药基因数据库的比较,HBsAg+ MCL患者在组蛋白修饰和DNA修复相关基因(ATM, ERBB2, FLT4, GSTP1, MAP3K1)中显著富集突变,靶向这些基因的药物可能使HBsAg+ MCL患者获益。
总结
该研究系统回顾了HBV在MCL患者中的发病率,并详细描述了HBsAg+ MCL患者的治疗模式、临床结局和基因突变特征。共纳入中国684例初诊MCL患者,发现9.5%的患者为乙型肝炎表面抗原阳性(HBsAg+)。与HBsAg阴性(HBsAg-)患者相比,HBsAg+ MCL患者LDH升高的发生率更高,但在其他临床特征,包括性别、年龄、ECOG、Ann Arbor分期、MIPI、结外累及和Ki‐67方面没有观察到差异。HD-AraC方案是年轻HBsAg+患者的主要一线诱导方案,老年患者则使用CHOP。当患者接受利妥昔单抗或基于CHOP的方案治疗时,HBsAg血清阳性患者的PFS显著短于HBsAg血清阴性。与CHOP相比,HD-AraC方案与HBsAg+患者更长的PFS相关。单独使用BTKi治疗也可引起HBV再激活。在74例接受靶向深度测序的患者中,HBsAg+ MCL患者的非同义突变负荷大于HBsAg- MCL患者。HDAC1、TRAF5、FGFR4、SMAD2、JAK3、SMC1A、ZAP70、BLM、CDK12、PLCG2、SMO、TP63、NF1、PTPR、EPHA2、RPTOR和FIP1L1在HBsAg+ MCL患者中显著富集。
参考文献
Feng J, Fei Y, Gao M, et al. Treatment patterns, clinical outcomes and gene mutation characteristics of hepatitis B virus‐associated mantle cell lymphoma. Hematol Oncol. 2024;e3268. https://doi.org/10.1002/hon.3268
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#套细胞淋巴瘤# #MCL#
6