翰森制药全球首创抗真菌药ibrexafungerp(艾瑞芬净)已递交中国Ⅲ期临床试验申请
2021-09-14 网络 网络
9月13日,翰森制药(豪森药业,3692.HK)宣布,公司拥有大中华区权益的ibrexafungerp已向中国国家药品监督管理局(NMPA)递交III期临床试验申请,用于治疗霉菌性阴道炎(VVC)。
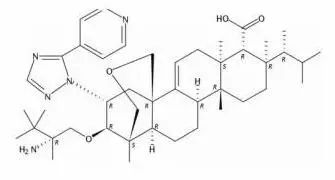
9月13日,翰森制药(豪森药业,3692.HK)宣布,公司拥有大中华区权益的ibrexafungerp已向中国国家药品监督管理局(NMPA)递交III期临床试验申请,用于治疗霉菌性阴道炎(VVC)。 早在今年2月11日,翰森制药发布公告,与SCYNEXIS, Inc.(纳斯达克股份代号:SCYX)订立独家许可及合作协议。根据许可协议,被许可人翰森制药将获得SCYNEXIS的独家特许权,在中华人民共和国(包括香港、澳门及台湾)研究、开发及商业化ibrexafungerp。作为独家特许权的代价,被许可人同意向SCYNEXIS支付1000万美元的首付款加潜在的里程碑付款及提成。 ibrexafungerp属于全球首创、作用机制全新的第四代新型三萜类抗真菌剂,具有广谱的抗菌活性,而且能够发挥静脉和口服制剂的治疗优势。ibrexafungerp作为一种新型葡聚糖合成酶抑制剂,它将葡聚糖合成酶抑制剂的良好活性与口服和静脉注射给药的潜在灵活性结合在一起,有望在住院和门诊环境中得到广泛使用。 ▲ibrexafungerp分子结构式 2021年6月2日,ibrexafungerp(商品名:BREXAFEMME®)获得美国食品药品监督管理局(FDA)批准,成为全球首款且唯一一款获批用于阴道酵母菌感染的口服非唑类药物。 此前,美国FDA曾授予Brexafemme合格传染病产品资格(QIDP),快速通道资格,以及孤儿药资格。Brexafemme 预计将在美国获得十年的市场独占权:五年的新化学实体独占权加上由于 QIDP 指定而额外延长五年的独占权。Brexafemme 还受到多项专利的保护,包括一项涵盖 ibrexafungerp 分子的物质组合专利。随着专利期限的延长,该专利预计将于2035年到期,在美国提供14年的保护。 全球约70%-75%的女性一生中至少经历一次阴道酵母菌感染,该领域自1990年起无创新疗法。阴道酵母菌感染临床表现为外阴瘙痒、灼痛等,严重影响生活质量。目前常见疗法为局部外用或口服唑类抗真菌药,临床应用受限,抗真菌药耐药性持续上升,因此患者需要更加安全有效的抗真菌创新疗法,临床医疗需求迫切。 ibrexafungerp能够开发为口服和注射等剂型,使用方便,其多项适应症已处于后期临床开发阶段,包括由念珠菌(包括耳念珠菌)和曲霉属等真菌引起的院内感染。体内和体外实验已显示出ibrexafungerp具有广谱的抗真菌活性,可以用于唑类和棘白菌素类等多种药物耐药菌株引起的感染。 有关ibrexafungerp的报道: 来源:药论 作者:微微南来风
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







#GER#
49
#抗真菌#
45
#抗真菌药#
45
#真菌#
46
#Ⅲ期临床#
49
7号线下
50