JNNP:在接受芬戈莫德治疗的多发性硬化症患者中,SARS-CoV-2 mRNA疫苗接种未能引发体液和细胞免疫反应
2022-08-05 网络 网络
新冠肺炎是由SARS-CoV-2引起的,表现出多种症状,从无症状到严重,甚至致命。除年龄和生活方式相关疾病外,严重新冠肺炎疾病病程的其他主要风险因素包括慢性疾病或免疫抑制治疗引起的免疫抑制。对于自身免
新冠肺炎是由SARS-CoV-2引起的,表现出多种症状,从无症状到严重,甚至致命。除年龄和生活方式相关疾病外,严重新冠肺炎疾病病程的其他主要风险因素包括慢性疾病或免疫抑制治疗引起的免疫抑制。对于自身免疫性疾病多发性硬化(MS)患者,主要由于治疗方法的差异,有关新冠肺炎患者易感性和严重性的研究结果喜忧参半。使用利妥昔单抗和奥雷利珠单抗以及鞘氨醇-1-磷酸(S1P)受体功能拮抗剂芬戈莫德的aCD20 BCD治疗增加了感染、住院和死亡的风险。幸运的是,抗SARS-CoV-2的疫苗在新病毒株出现后一年内可用,两种mRNA疫苗BNT162b2(辉瑞生物技术公司)和mRNA-1273(Moderna)在2020年底获得批准的相应临床试验中显示出强大的免疫原性、有效性和安全性。由于严重新冠肺炎的风险增加,MS患者优先接种疫苗,然而,预期其高度免疫调节的MS治疗会损害疫苗的免疫原性并改变保护。初步结果表明,经aCD20 BCD治疗的MS患者表现出较低或缺失的SARS-CoV-2棘突糖蛋白特异性抗体和B细胞反应。功能性T细胞反应得以维持,但抗原特异性滤泡辅助T细胞存在部分选择性缺陷。接受芬戈利莫德治疗的患者体液反应受损,此外,他们的T细胞反应降低。尽管有这些选定的免疫原性降低的报告,但从初级疫苗接种前到强化疫苗接种后,仍缺乏详细的体液和细胞免疫反应谱研究报告。
在本研究中,旨在评估经aCD20 BCD、芬戈莫德、干扰素-β(IFNβ)、醋酸格拉替拉末(GA)、富马酸二甲酯(DMF)、特氟米特(TFN)或α4-整合素单克隆抗体纳他珠单抗(NTZ)治疗的MS患者对初次、二次和强化SARS-CoV-2疫苗接种的体液和细胞免疫应答。由于多发性硬化的高发病率和早期开始免疫调节治疗的趋势,研究该患者群体的疫苗免疫原性和诱导免疫的寿命对于临床实践和疫苗开发变得越来越重要。目前可用的SARS-CoV-2 mRNA疫苗依赖于具有高度免疫原性的SARS-CoV-2surface spike糖蛋白,该糖蛋白可诱导强大的T细胞和中和抗体反应。棘突糖蛋白由两个亚单位S1和S2组成,其中S1亚单位通过受体结合域(RBD)介导病毒-受体接触,是从头免疫应答的靶点,也是引发保护性免疫应答的相关因素。S2亚基介导膜融合,相对于地方性冠状病毒更为保守。本文分析了对这两个亚单位的免疫反应。本文发表在《神经病学,神经外科学和精神病学杂志》上()。

作为一项前瞻性队列研究的一部分,研究了多发性硬化症(MS)患者在同源初次、二次和加强型SARS-CoV-2 mRNA疫苗接种后,在不同的DMT上诱导、稳定和增强疫苗特异性抗体、B细胞和T细胞。分析的126例MS患者中,105例接受了基于抗CD20的B细胞去除(aCD20 BCD)、芬戈莫德、干扰素-β、富马酸二甲酯、醋酸格拉替拉末、特氟米特或纳他珠单抗治疗,21例未经治疗的MS患者进行比较。与所有其他MS患者相比,即使在增强治疗后,大多数aCD20 BCD和芬戈利莫德治疗患者的抗S1 IgG、血清中和活性没有明显降低,并且缺乏受体结合域特异性和S2特异性B细胞。接受芬戈莫德治疗的患者还缺乏尖峰反应性CD4+T细胞反应。fingolimod治疗的持续时间,而不是疫苗接种前的外周血B细胞和T细胞计数,决定了是否引发体液免疫反应。
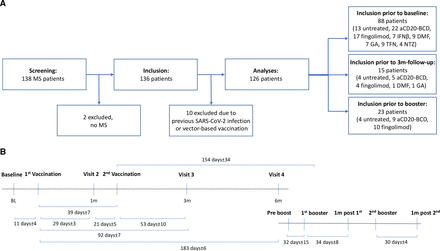
研究流程
分析了经S1P受体功能拮抗剂fingolimod或aCD20 BCD治疗的MS患者对SARS-CoV-2 mRNA疫苗的初级、次级和增强免疫应答,并与其他标准免疫调节治疗方案和未经治疗的MS病人进行了比较。SARS-CoV-2疫苗通过诱导特异性T细胞和B细胞记忆。来减轻新冠肺炎的感染风险和症状严重性,但B细胞和T细胞如何单独发挥作用目前尚不清楚。在aCD20 BCD治疗的MS患者中,尽管接种了疫苗,但严重新冠肺炎疾病的发病率较高,感染风险增加,这表明缺乏特异性抗体和B细胞可严重损害新冠肺炎免疫。有趣的是,即使在没有已知免疫缺陷的健康个体中,对SARS-CoV-2的抗体反应似乎也相对短暂,因此将重点转移到B和T细胞免疫记忆上,以提供对严重疾病的长期保护。对SARS-CoV-2疫苗接种的T细胞反应已被证明是稳定的,并在保护、增强抗体反应和病毒清除方面发挥着核心作用一直以来,T细胞对SARS-CoV-2的反应降低也与严重疾病相关。在接受aCD20 BCD治疗的患者中,由于缺乏B细胞并且无法产生特异性体液免疫反应,T细胞反应是保护性免疫反应的有希望的指标,通过提供B细胞非依赖性保护以抵抗严重的新冠肺炎。

aCD20 BCD治疗和芬格莫德治疗患者接种SARS-CoV-2 mRNA后体液反应降低
研究结果与其他疾病疫苗接种的现有文献相结合,表明除aCD20 BCD疗法和芬戈利莫德外,未经治疗的MS患者和DMT患者对初次和二次SARS-CoV-2疫苗接种的体液免疫应答水平与正常健康献血者相当。此外,对接受aCD20 BCD治疗的患者在6个月间隔内接受600 mg奥雷利珠单抗或1000 mg利妥昔单抗输注的结果证实了先前的报告,表明初次接种后的抗S1 IgG水平与绝对外周B细胞计数相关,并且与接种前最后一次aCD20 BCD输注后的持续时间相关,但程度较小,最后,aCD20 BCD对诱发SARS-CoV-2尖峰特异性T细胞应答的主要能力没有影响。此外,一半以上接受aCD20 BCD治疗的患者在加强疫苗接种后仍然没有体液反应,这一次与加强疫苗接种前的外周B细胞计数没有显著相关性。然而,此处研究的aCD20 BCD治疗患者显示出非常低的B细胞计数(平均2.1个B细胞/µL,不包括一个378个细胞/µL的异常值,这些细胞具有正常的体液反应),这可能会由于这些小数量的不确定性而导致相关计算产生偏差。另一种可能的解释是,B细胞数量与加强疫苗接种的体液反应之间缺乏相关性,可能是疫苗接种后不久进行的aCD20 BCD再融合。
长期芬戈利莫治疗下缺乏免疫原性表明,功能性免疫反应不仅需要免疫细胞本身,还需要这些细胞进入接种部位并畅通无阻地移动。体液和T细胞反应的缺乏表明,芬戈莫德治疗的MS患者尽管接种了强化疫苗,但仍存在严重SARS-CoV-2感染的风险,这与临床决策和适应性保护措施高度相关。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#多发性#
43
#硬化症#
46
#RNA疫苗#
64
#SARS-CoV#
46
#疫苗接种#
44
#免疫反应#
47
#SARS#
43
#细胞免疫#
39
#芬戈莫德#
50