论文解读|Hua Jiang/Denggang Fu/Jueping Feng教授团队揭示肺鳞状细胞癌肿瘤免疫微环境的新见解
2024-04-16 Genes and Diseases Genes and Diseases 发表于上海
该研究揭示了肺鳞状细胞癌免疫基因组学特征,为我们理解肿瘤免疫微环境及其对癌症治疗的影响提供了新见解。

肺鳞状细胞癌(LSCC)是非小细胞肺癌(NSCLC)的一个主要亚型,约占所有NSCLC病例的30%。尽管LSCC的治疗取得了一定进展,但由于LSCC肿瘤免疫微环境的异质性,有效的免疫治疗仍然难以实现。
美国印第安纳大学的Hua Jiang/Denggang Fu教授团队联合武汉市第四医院Jueping Feng教授团队在本刊发表了题为“Immunogenomic classification of lung squamous cell carcinoma characterizes tumor immune microenvironment and predicts cancer therapy”的研究快讯,揭示了肺鳞状细胞癌免疫基因组学特征,为我们理解肿瘤免疫微环境及其对癌症治疗的影响提供了新见解。主要发现如下:
1. 亚型区分与肿瘤微环境特征
研究团队基于29个免疫特征,运用层次聚类算法将502例LSCC患者分为高免疫亚型(n = 383)和低免疫亚型(n = 119)(图1A)。ESTIMATE算法分析发现,两种亚型的肿瘤微环境(TME)中呈现出显著差异。高免疫亚型的患者免疫及基质评分较高(图1B),肿瘤干细胞指数较低,表明此类患者具有较强的抗肿瘤免疫力。
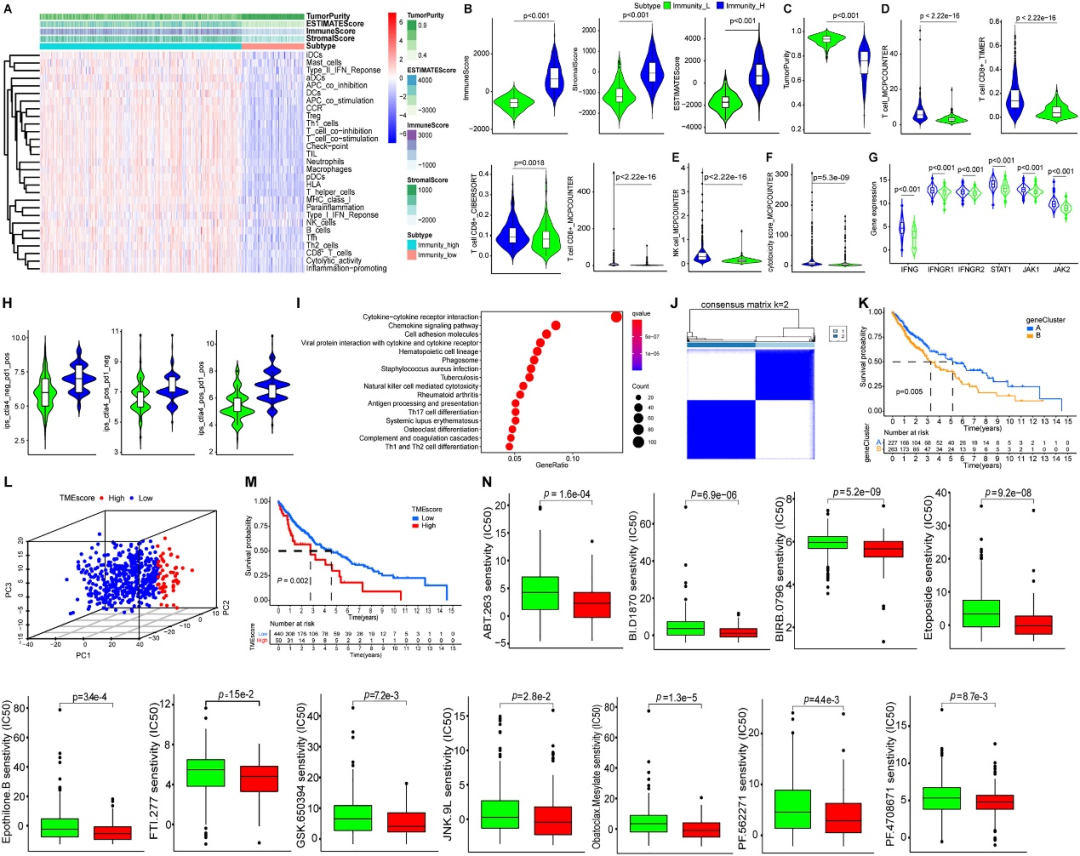
图1. LSCC 患者的免疫基因组分类表征了肿瘤免疫微环境和癌症治疗
2. 免疫细胞浸润与细胞毒性
进一步通过多重反卷积算法分析,研究团队发现高免疫亚型中总T细胞、CD8+ T细胞和自然杀伤(NK)细胞的浸润程度更高(图1D、E),同时细胞毒活性也更显著(图1F),表明该亚型的抗肿瘤免疫力较强。研究还注意到表达IFNγ的CD8+ T细胞在TME中数量显著增加(图1G),这可能是NSCLC患者对免疫检查点抑制剂(ICIs)治疗响应性的一个重要指标。
3. 基因表达与通路分析
在两种亚型间,研究团队识别出2 646个差异表达基因(DEGs),其中大部分在高免疫亚型中上调。这些DEGs主要涉及免疫反应相关过程和通路,如细胞因子-受体相互作用、趋化因子信号传导通路以及自然杀伤细胞介导的细胞毒性等(图1I)。值得注意的是,高免疫亚型中辅助T 细胞的1/IFNγ基因和T细胞细胞毒性标志物的表达均显著升高,进一步印证了高免疫亚型中免疫反应的增强。
这项研究强调了免疫基因组分析在肺鳞状细胞癌肿瘤免疫微环境研究中的重要性。该研究的发现为基于免疫分型的个性化癌症治疗提供了可能的方向,凸显了根据免疫分型优化治疗策略的潜力。
文章来源
免费全文下载链接:
https://www.sciencedirect.com/science/article/pii/S2352304223000454
引用这篇文章:
Fu D, Zhang B, Zhang Y, et al. Immunogenomic classification of lung squamous cell carcinoma characterizes tumor immune microenvironment and predicts cancer therapy. Genes Dis. 2023;10(6):2274-2277.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















赞
8
#肺鳞状细胞癌# #免疫微环境#
0