ASCO 2020:Pembrolizumab或替代化疗在MSI-H / dMMR CRC中一线治疗的地位
2020-06-04 任冉 健康界
在2020年美国临床肿瘤学会(ASCO)年会第二天,Thierry Andre代表其团队发表了派姆单抗与化疗联合用于微卫星不稳定性高/错配修复缺陷性转移性结直肠癌:KEYNOTE-177 3期研究。
在2020年美国临床肿瘤学会(ASCO)年会第二天,Thierry Andre代表其团队发表了派姆单抗与化疗联合用于微卫星不稳定性高/错配修复缺陷性转移性结直肠癌:KEYNOTE-177 3期研究。
之前的Pembrolizumab治疗难治性,微卫星不稳定性高/错配修复缺陷的转移性结直肠癌的II期开放标签研究(KEYNOTE-164)提示:派姆单抗对MSI-H / dMMR CRC患者有效,安全性可控。
Thierry Andre指出:MSI-H患者占mCRC患者的5%,FDA批准pembrolizumab用于先前接受msi - htumor治疗的成人和儿童患者,无论肿瘤类型或部位。
下面是研究报告的主要内容。
背景:
KEYNOTE-177(NCT02563002)是一项3期随机开放标签研究,评估了Pembrolizumab(pembro)与标准护理化疗±贝伐单抗或西妥昔单抗(chemo)作为微卫星不稳定性高/错配修复缺陷(MSI-H/dMMR)转移性结直肠癌(mCRC)患者一线治疗的疗效和安全性。
方法:
总共307例局部测定的MSI-H / dMMR mCRC和ECOG PS 0或1的患者被随机分配为1:1,分别给予一线pembro 200 mg 每3周一次,持续2年或研究者选择mFOLFOX6或FOLFIRI Q2W±贝伐单抗或西妥昔单抗(随机选择化疗方案)。
继续治疗直至PD、不可接受的毒性、患者/研究者决定退出治疗或完成35个周期(仅pembro)。确诊PD后,接受化学疗法的患者最多可过渡到pembro 35个周期。

图3.数据分析
主要终点是PFS(RECIST v1.1,中央审查)和OS。关键的次要终点包括ORR(RECIST v1.1,中央评审)和安全性。该中期分析的数据截止日期为2020年2月19日。该研究将继续进行,无需评估OS。
结果:
数据截止时,将153个患者随机分配给pembro,154个患者随机分配给化疗。Pembro的研究中位(范围)随访为28.4 mo(0.2-48.3),而化学治疗为27.2 mo(0.8-46.6)。Pembro治疗PFS优于化疗(中位16.5个月vs 8.2个月;心率0.60;95%CI,0.45-0.80;P=0.0002)。
pembro组12个月和24个月的PFS发生率分别为55.3%和48.3%,而化疗组分别为37.3%和18.6%。
确认的ORR为43.8%比33.1%;pembro组与化疗组分别为10.6mo(2.8-37.5+)和2.3+-41.4+,均未达到反应的中位(范围)持续时间。
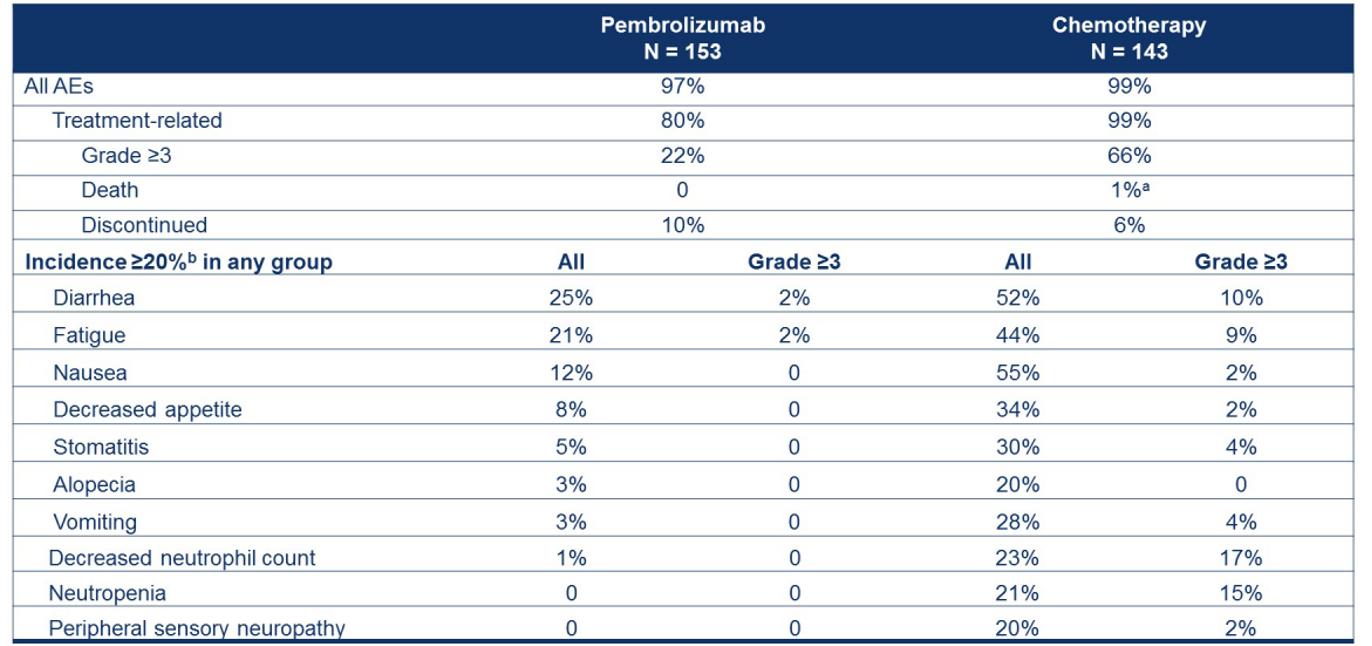 图7所有患者中的不良事件
图7所有患者中的不良事件
pembro与化疗的3-5级治疗相关不良事件(AE)发生率分别为22%和66%。化疗组1例患者死于治疗相关的AE。
结论:
Pembro作为MSI-H / dMMR mCRC患者的一线治疗,与化学疗法相比,PFS具有临床意义和统计学意义的显著改善,反应更持久,同时2、3级相关事件发生率较低,应成为这些患者的新治疗方案。
拓展:
本次ASCO 除去该项试验报告外,还有另外三项项与Keytruda相关的研究报告,分别是:
1. Keytruda与Herzuma(曲妥珠单抗生物类似药)和化疗联用,一线治疗HER2阳性的晚期胃癌的研究数据,该1b/2期试验研究结果显示:用这种三联方案一线治疗HER2阳性胃癌患者,无论PD-L1状态如何,患者均可以获得临床意义的改善。
2. KEYNOTE-524/study 116试验,该研究是一项开放标签、单臂的1b期临床试验,意在评估Keytruda和Lenvima联合疗法在之前未经系统治疗的不能切除的HCC患者中的效果。该研究结果表明:基于RECIST v1.1标准,Keytruda组合疗法达到36%的ORR,完全缓解率为1%,部分缓解率为35%,中位DOR是12.6个月。
3. KEYNOTE-146/study 111试验,该实验是一项开放标签,单臂1b/2期临床试验,旨在评估Keytruda和Lenvima组合疗法对某些实体瘤患者的效果。其结果显示,根据RECIST v1.1标准评估的ORR为52%,全部为部分缓解。中位DOR为12个月。中位PFS为11.3个月,12个月PFS率为44%。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#CRC#
29
#PE#
28
#ASC#
37
#mAb#
19
#Pembro#
27
#Pembrolizumab#
30
#ASCO 2020#
24
#MMR#
31
#MSI#
31