【blood】成人ALL的治疗:2023 ELN指南
2024-02-08 聊聊血液 聊聊血液 发表于陕西省
欧洲成人ALL工作组总结了当前的技术发展水平,并对诊断方法、生物学和临床特征、预后因素、风险分层和治疗,以及终点和结局的定义提供了全面的建议,旨在为成人ALL患者的初始治疗提供指导。
ALL的治疗
多个欧洲国家研究组在欧洲白血病网络 (ELN)框架内开展合作,命名为欧洲成人 ALL 工作组 (EWALL),曾发表AML和CML的指南。ALL在成人肿瘤中相对罕见,有许多不同的临床和生物学亚组,对疾病生物学和治疗选择的认识也呈指数增加。
欧洲成人ALL工作组总结了当前的技术发展水平,并对诊断方法、生物学和临床特征、预后因素、风险分层和治疗,以及终点和结局的定义提供了全面的建议,旨在为成人ALL患者的初始治疗提供指导。关于“诊断、风险因素、缓解评估”和“治疗”的两篇指南近日发表于《blood》。现整理关于治疗的全文共2万字,水平有限如有错误敬请谅解。

该指南总结了临床治疗的内容,包括使用新的免疫治疗、应用 MRD 进行治疗决策、治疗特定亚组和具有挑战性的情况以及晚期效应和支持治疗。
Ph- ALL 的诱导和巩固治疗
一般原则
强化诱导和巩固治疗的目的是尽可能多的患者获得完全缓解 (CR),并尽可能更早、更安全、更深。15-18岁至55-65岁成人Ph/BCR::ABL1阴性 (Ph-) ALL 的 CR 率约为90%。大约5%会在两个周期后显示原发性耐药,约5%早期死于疾病相关或治疗相关并发症。治疗通常为风险适应性(risk-adapted),利用预后因素 (PF) 和 MRD 疗程决定化疗强度、免疫治疗的使用或干细胞移植 (SCT) 的指征。此外全面的诊断特征是最佳治疗的基础。
成人ALL中儿童样化疗(Pediatric-based Chemotherapy,p-b)
在一项荟萃分析中,27份报告中的25份明确支持 p-b 方法作为标准治疗 (SoC)。在高达45-55岁的患者中,总生存期 (OS)可改善至平均60%。单中心研究比较了p-b方案与标准 Hyper-CVAD,结果得出相似的结论。P-b治疗在标危 ALL 和 MRD 阴性患者中特别有效,可确保 OS 约为70%。其典型药物包括皮质类固醇(尤其是地塞米松)、长春新碱、抗代谢物(6-硫嘌呤、阿糖胞苷、甲氨蝶呤)和门冬酰胺酶(ASP;聚乙二醇化或非聚乙二醇化)联合强化支持治疗,避免不恰当的剂量降低/延迟和风险适应性SCT。
诱导治疗
对于前期阶段,皮质类固醇通常给药5-7天;偶尔还会添加其他药物,例如脑脊液 (CSF) 采样后环磷酰胺 (CP) 和鞘内 (IT) 预防。首次诱导持续约4周,此时并发症风险最高,必须进行强化支持,包括粒细胞集落刺激因子 (G-CSF)、输血以及感染的最佳预防和管理。诱导骨架由长春新碱、类固醇、蒽环类药物和 ASP 组成。地塞米松 (Dexa) 具有高度活性,包括对中枢神经系统 (CNS) 的活性,但需要仔细调整剂量和给药方案。长期给予地塞米松时重度感染的风险增加,在诱导治疗期间,多个小组已经实施了中断给药的短期应用。早期大剂量 (HD) 蒽环类药物可加重骨髓毒性和粘膜炎。一项随机试验未显示一线增加环磷酰胺剂量具有优势,但分次给药对接受较低强度巩固治疗的>55岁患者有益。与天然化合物相比,聚乙二醇化天冬酰胺酶 (PEG-ASP) 可提供更长的天冬酰胺耗竭(根据剂量,在14-30天内可检测到血清酶活性≥0.1 IU/mL);且与天然 ASP 相比,其很少引起严重过敏反应。ASP一般可引起凝血功能障碍、血栓形成、高血糖、胰腺炎和肝毒性,后者在成人中比儿童更常见和更受关注。因此建立毒性监测和管理的具体时间表至关重要;PEG-ASP方案和给药应根据下列因素进行调整:年龄、体重指数(>30 kg/m2时毒性更高)和肝脂肪变性(如果超声扫描呈阳性,则毒性更高)以及预期的活性持续时间。除严格的临床指征外,在预期的 ASP 活性期间不应给予任何其他潜在的肝毒性药物。最近讨论了使用 PEG-ASP 前的前驱用药,以降低输注反应的风险,因其有时难以与真正的过敏反应区分。只有在可以提供药物监测的情况下,才能给予任何前驱用药,否则可能存在忽视ASP失活的风险。
第二次诱导/第一次巩固治疗通常包括环磷酰胺、阿糖胞苷 (AC) 和巯基嘌呤 (MP) 或 HD-甲氨蝶呤 (MTX)/HD-AC 或 HD-AC/伊达比星。2个诱导疗程后未CR的少数患者具有高度耐药性ALL,是替代免疫治疗的候选者(具体取决于方案)。
巩固治疗
CR 患者接受巩固治疗。由 HD-MTX 和HD-AC(也可用作 CNS 渗透剂)、PEG-ASP和其他药物组成的循环多药给药的结局最佳。BFM(Berlin-Frankfurt-Munster)为基础的方案包括延迟的再诱导期。巩固治疗的平均持续时间为6个月或以上,共6-8个疗程。HD-AC、HD-MTX、依托泊苷和环磷酰胺对改善高危亚群和 T-ALL 的结局至关重要。HD-AC(4-8剂,1-3 g/m2)、PEG-ASP和HD-MTX(1-1.5 g/m2,随后为亚叶酸解救治疗)以组(blocks)给药。MTX可使用更高的剂量3-5 g/m2,特别是高危患者和T-ALL;一项随机研究表明,接受 3g/m2与0.5g/m2 MTX巩固治疗的患者相比结局改善,但更低剂量下不常见。在青少年和年轻成人 (AYA) 中进行的一项 II 期研究使用较低的 MTX 剂量和每周剂量调整(Capizzi风格)。儿童研究(≤30岁)显示,Capizzi MTX治疗 T-ALL 的结局优于MTX 5g/m2,但 B-ALL 中未见优势。
考虑到异质性巩固治疗方案、校正患者年龄和风险类别后的结果相当以及缺乏随机比较,目前尚无哪个方案可推荐为 Ph- ALL 的SoC,但P-b方案更受青睐。强烈建议参加(或采用)前瞻性临床试验。研究中心的经验和既定指南对于采用不同的方案也非常重要。
Ph-B系(B-LIN) ALL的一线靶向治疗
鉴于免疫治疗提供的机遇,也对靶向药物的改良方案进行了试验,以增加缓解率、OS,并尽可能降低由于强化化疗和 SCT 导致的高毒性负担,因此识别表面标志物作为免疫治疗靶点是初始诊断的重要部分,具体化合物和作用机制见后文。越来越多的证据表明免疫疗法可提高抗白血病疗效(表1),其中抗 CD20 抗体,双特异性 CD19/CD3抗体贝林妥欧单抗(Blina) 和 CD22抗体-药物偶联物 Inotuzumab Ozogamicin (InO) 已在临床试验中纳入一线和挽救治疗方案。
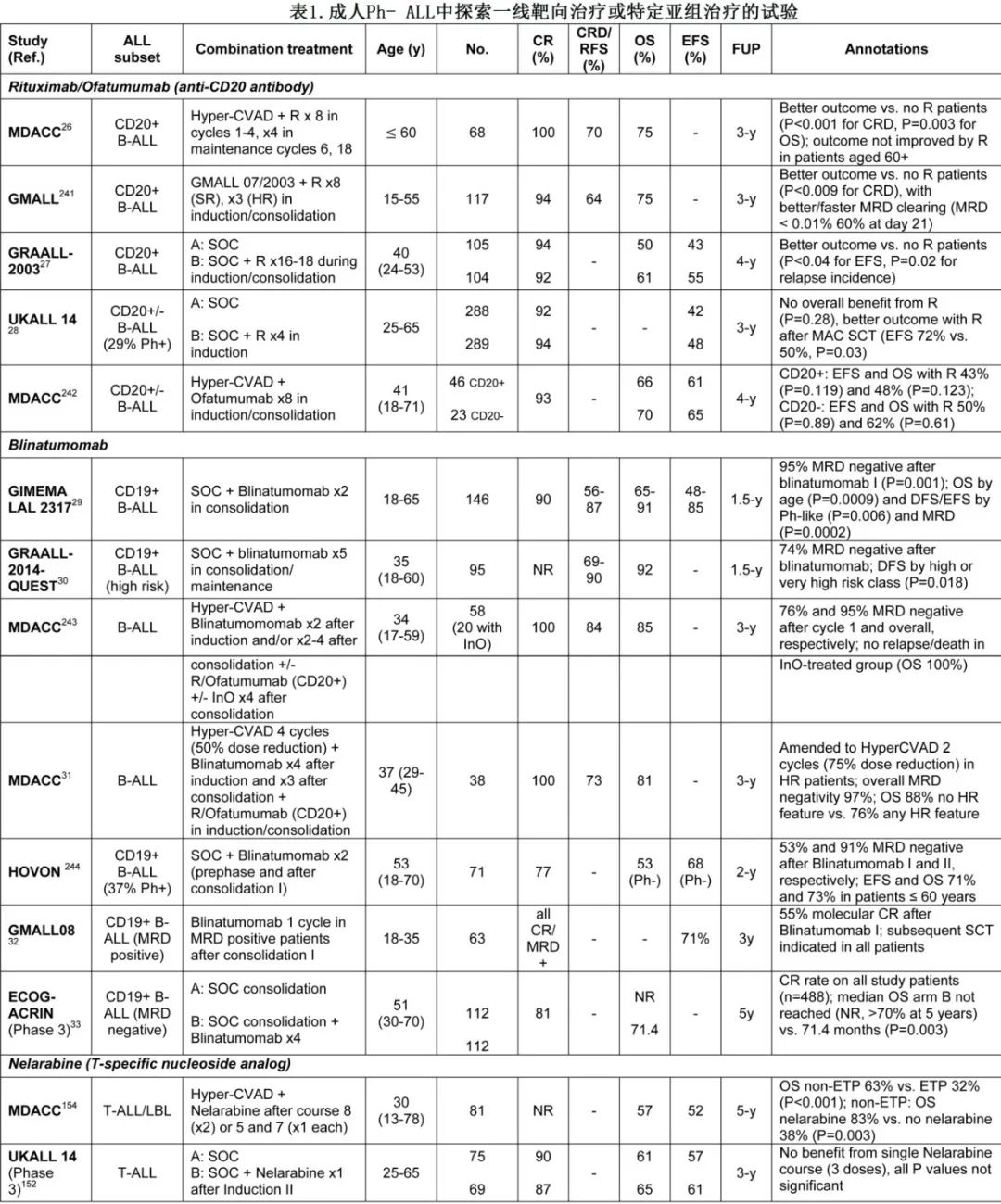
大约40%的成人 B-LIN ALL表达 CD20 抗原(ALL原始细胞中>10-20%),在新发 ALL 中成功评估了抗 CD20 抗体。在一项随机研究中,利妥昔单抗 (Ritux) 显著降低复发风险 (RR),有助于增加 SCT 实现率和改善OS。有趣的是,Ritux治疗患者对 ASP 的过敏反应较少;但早期 MRD 反应并未改善。一项随机研究中,无论CD20 表达如何,给予 Ritux均未显示获益;但该研究仅处方4剂(vs.其他试验中至少8剂)。
Blina 的初步数据(部分与 InO 相关)令人鼓舞,并证实MRD 转阴率较高,RR较低,在1-4年有限随访时 OS 改善。一项随机研究的初步分析显示,在30-70岁 MRD 阴性 ALL 患者的标准基础治疗中加用 Blina 巩固治疗,结果Blina在 OS 方面具有优势。因此,越来越多的证据表明,Blina在MRD 阴性和阳性患者巩固治疗方面可能有益。
总体而言,建议使用 Ritux 治疗CD20+ ALL,至少给药8次。同样,由于在CD22+ 和CD19+ B-ALL中一线 InO 和 Blina 的早期结果有利和期望较高,建议未经治疗的患者参加 InO 和 Blina 试验,直至正在进行的研究出结果。在CD20+ ALL中同时使用抗 CD20 抗体可作为SoC,在分子学失败的情况下使用Blina也是SoC。
维持治疗
强烈建议所有患者接受维持治疗,维持治疗未在随机试验中进行检验,但所有省略维持治疗的尝试均导致结局较差,且维持治疗不充分也导致OS显著恶化。可能需要长期药物暴露来根除MRD。
巯基嘌呤 (MP)和 MTX 是维持治疗的主要药物,而IT 预防也是大多数治疗方案的一部分;部分工作组还纳入其他成分,如 POMP 方案(MP、MTX、泼尼松、长春新碱),但获益仍存在争议。此外,关于长春新碱/类固醇脉冲治疗儿童△IKZF1 患者潜在获益的数据存在争议,在维持治疗中使用 Dexa 代替泼尼松可能导致感染性死亡的发生率增加,因此大多数工作组首选无长春新碱/类固醇脉冲的维持治疗。建议总治疗持续时间为2-2.5年(包括维持治疗),以及维持治疗期间间隔约3个月进行 MRD 检测。
CNS预防
诊断时5-10%的成人发生 CNS 浸润,CNS状态可分为白细胞分类无原始淋巴细胞 (CNS-1)、<5个白细胞/ul (CNS-2)、≥5个白细胞/ul 或颅神经麻痹(CNS-3)。如果 CSF 中可见任何原始细胞,此时均应怀疑CNS 浸润;此时必须进行常规排除,随后通过分析诊断时或诊断后不久获得的 CSF 的细胞离心涂片和/或多色流式细胞术 (MFC) 分析进行监测。部分方案建议等待外周血 (PB) 原始细胞清除或减少到某临界值以下,以防有创操作“播种”CNS的风险。另一方面,延迟腰椎穿刺存在无法检测到初始 CNS 受累的风险,且在白细胞计数 (WBC) 较高的患者中可能更常见。预测初始 CNS 疾病风险较高的因素为T-ALL、高WBC、高危细胞遗传学如Ph+ ALL和T(4;11)。已尝试在CSF中检测MRD,但未成为标准治疗的一部分。
所有患者均需要 CNS 预防。头颅照射、IT化疗和全身治疗中穿过血脑屏障的成分均有应用,但目前很少给予头颅照射作为预防。没有足够的数据来明确解析 CNS 穿透性全身治疗与 IT 预防的相对价值;因此,尽管两者均有建议,但后者最常用作关键组分。
IT化疗
MTX、ARAC和类固醇均可安全通过 IT 给药,均可单独或联合使用,且没有特定 IT 方案显示明显更优。IT药物的给药体积应足以在 CSF 中均匀分布,通常在给药前取出与药物体积相当体积的CSF,并应始终进行 CSF分析;患者应保持卧位至少1小时。传统“切割(cutting)”针具有较高的水囊瘤和硬膜下出血风险,这至关重要,因此建议使用无损伤(atraumatic)针。IT注射的最佳次数尚不确定,但大多数方案推荐总剂量为8-15次。必须密切注意支持治疗,如血液制品支持治疗。在极少数情况下,当腰椎穿刺难以进行时,考虑到手术相关风险和关于充分给药的不确定性,可以认为 Ommaya 储液囊是一种单独的替代方案。IT治疗的实践方面综述见参考文献(Olmos-Jimenez R, Espuny-Miro A, Carceles Rodriguez C, Diaz-Carrasco MS. Practical aspects of the use of intrathecal chemotherapy. Farm Hosp. 2017;41(n01):105-129)。
全身化疗
全身化疗也可能有助于预防 CNS 复发。对43项试验的荟萃分析显示,加用 HD-MTX 在降低 RR 和改善 EFS 方面有益,尽管对 CNS 疾病的影响较小。最近的一项随机试验显示,与0.5g/m2剂量相比,3g/m2剂量在无病生存期 (DFS) 方面具有获益(但对 CNS 复发无影响),且较高剂量无额外毒性。Dexa在降低 CNS RR 方面可能优于泼尼松龙。
基于MRD的治疗调整
鉴于 MRD 缓解对预后的重要影响,大多数工作组建议根据 MRD 改变治疗。基于 MRD 的治疗决策需要适当和标准化的 MRD 检测,且重要的决定因素包括 MRD 的时间点和水平、方法、是否存在其他预后因素(PF)和建议的治疗调整。早期良好的 MRD 缓解与有利结局相关。在一个报道中,12%的标危患者在诱导第11天未检测到MRD,预后极佳。有研究确定首次巩固治疗后的较晚时间点与 RR 最具预后相关性,因此,早期时间点可能适用于确定临床试验中潜在治疗递减的患者,而晚期时间点有助于识别治疗递增的候选者。最适宜的时间点取决于方案,如果主要目标是识别化疗耐药患者,应在进行变更前给予所有相关化疗药物,并谨记 MRD 检测并不代表髓外隔室。在大多数方案中,适宜时间点约为诊断后2-3个月。
确定 MRD最具预测性的水平也很重要,通常考虑阈值为0.01%(即10-4),因为其与 MRD 检测的灵敏度一致。MRD每增加一个对数水平,至后续血液学复发的时间就会缩短;对于 MRD 高于0.01%和0.1%的患者,至血液学复发的中位时间分别为7.6个月和4.9个月。MRD水平较低(即低于0.01%)的患者可能具有中等预后,应考虑在未来进行基于 MRD 的治疗干预。
此外,MRD检测方法也影响治疗决策。因此,克隆免疫球蛋白/T 细胞受体重排 (IG/TR) 的定量聚合酶链反应 (PCR) 测定需要4-6周才能建立适当的试验。MFC可能更快地提供结果,但结果可能不确定,尤其是使用再生(regenerating)骨髓 (BM)时。基于阴性 MRD 状态确认的决定需要严格遵守方法学的先决条件,需要在有经验的参考实验室进行 MRD 评估,且灵敏度至少为0.01%,此外该时间点可用于治疗决策。
大多数关于 MRD 预后影响的试验是在新诊断患者中进行的,在成人 ALL 中,仅有限的数据显示复发性/难治性 (R/R) 背景下新靶向药物治疗后持续 MRD 之间的相关性,但相关性不如一线治疗严格。不管怎么说,对挽救治疗的MRD反应仍可表明抗白血病疗效,且对于患者极有价值。
到目前为止,很少有人尝试减低强度标准治疗。在 MRD 反应良好的标危儿童患者中进行的一项随机试验评价了减低强度再诱导方案的结局,结果DFS 较差,尤其是在10岁以上的儿童中。还需进行进一步的临床试验以评价治疗减低,尤其是免疫治疗时代。
大多数工作组根据 MRD 确定 SCT 的指征,SCT可为 MRD 缓解不佳的患者提供生存优势。但SCT需要时间,在此期间仍有许多患者复发(即使化疗)。此外,SCT前的高 MRD 水平与 SCT 后较高的 RR 相关。SCT前 MRD 的预后价值,与 MRD 检测和移植之间的时间间隔、潜在的过渡治疗、预处理方案和其他移植相关因素相关。
建议对持续或复发性 MRD 患者改变治疗,与化疗相比,具有不同作用机制的药物可能最有前景。到目前为止,Blina是唯一在 MRD 阳性 B-LIN ALL 关键研究中评估的药物,纳入MRD>0.1%的患者(包括首次或后续缓解)。78%的患者达到主要终点,即1个周期后达到完全分子学缓解 (CMR);获得36.5个月的有利中位生存期,且达到 CMR 的患者有显著获益。67%患者桥接SCT,SCT后的 RR 较低。然而,治疗相关死亡率 (TRM) 高于30%,从而影响了OS,该问题可以通过中位年龄较高(42岁)、全预处理和不匹配供者的高发生率来解释。另一方面,大多数无后续 SCT 的患者复发,且除了完全分子学缓解之外未发现预测无 SCT 患者 RR 的因素。未来应在 MRD 持续存在的情况下评价免疫治疗或其他靶向药物。
总体而言,3组(blocks)标准治疗后 MRD 高于0.01%的患者有 SCT 和靶向治疗的指征。到目前为止,没有证据表明可以在临床试验之外建议 MRD 病程有利的患者减少治疗(除了 SCT 外)。是否所有分子学CR患者都可以省略SCT(包括特别高危的亚组),这一问题也应进行研究。使用新化合物(如Blina)从 MRD 阳性状态转换为 MRD 阴性状态后,后续 SCT 仍是具有匹配供者的年轻患者的标准治疗。在 TRM 高风险的老年患者中,应遵循减量预处理移植方案或巩固/维持策略。
干细胞移植
SCT 是一个复杂的多步骤、多因素、高度个体化的治疗概念,因此是预防复发的有效治疗方法,将清髓剂量的化疗和/或放疗与潜在有益的移植物抗白血病反应相结合。但它也与 TRM 的显著发生率相关,在人类白细胞抗原 (HLA) 匹配的同胞供体 (MSD)SCT 后可达13%,在无关供者(URD)SCT 后可达21%。单倍体相合 SCT 与后置环磷酰胺在许多国家越来越多地实施。总体而言,SCT 的指征需要权衡 RR 和 TRM 风险。尽管很多人尝试阐述预后评分,但在许多个体病例中的潜在获益尚不确定。(自体)SCT的价值似乎有疑问,主要受 MRD 状态的影响。近期 SCT 试验的结果总结见表2。

Ph阴性ALL
大多数评价 SCT 作用的前瞻性研究都考虑了 MSD 的可用性。CR1伴 MSD 的患者接受SCT,而缺乏 MSD 的患者接受autoCST 或化疗。大多数试验证明了 MSD-SCT 的有益作用,但这些研究是在 MRD 常规评估时代之前进行的,且使用非 p-b 对照组。目前MRD状态是最重要的PF,可驱动 SCT 指征。在随后的两项试验中,522例≤55岁的 Ph-高危患者准备接受SCT,其中54%在CR1(MSD或URD)接受移植。在诱导后MRD≥10-3的患者中,SCT与较长的 LFS 相关,但在 MRD <10-3的患者中是否SCT并无差异。然而,该观察结果可能不一定适用于减低强度化疗方案,评估 MRD 阴性高危患者 SCT 指征的随机试验正在进行中。
SCT 的指征主要是指55-60岁的年轻成人,但研究组之间存在差异;且关于老年患者尚未达成共识。据报告,研究组和单个中心之间的临床实践存在高度变异性。对于 MRD 阴性的老年患者,不应在前瞻性临床试验之外使用SCT。此外,在 SCT 后继续进行 MRD 监测以确定即将发生的复发也至关重要。
Ph+ ALL
在接受伊马替尼和化疗的患者中,SCT与显著的 OS 获益相关,因此仍是SoC。引入第三代酪氨酸激酶抑制剂 (TKI) 或考虑特定 PF 时可能会限制其指征,但仍需要在随访时间足够长的前瞻性试验中进行验证。在老年患者中进行的第三代 TKI 和免疫治疗的临床试验可能提供无SCT长期生存的相关数据。
SCT 后应进行严格的 MRD 监测。MRD阳性患者应根据 ABL激酶结构域 (KD) 突变状态、MRD复发水平和时间接受 TKI 治疗。早期 MRD 阴性状态的患者可接受预防性(prophylactically)或抢先(pre-emptively)治疗,以获得至少1年的连续分子学CR;一项前瞻性随机试验已证实两种策略均可行。
SCT程序方面
供者类型选择与其他白血病无差异,可考虑所有MSD、URD或半相合供者,但预处理方案的选择可能影响结局。在儿童 ALL 中进行的一项随机试验显示,清髓性全身照射 (TBI)(12 Gray) 为基础的预处理相对于化疗为基础方案有明显获益,主要是由于 RR 降低。在 TBI 可及性有限或无法耐受的患者中,静脉注射白消安或 HD 塞替派为基础的预处理可作为备选方案。成人前瞻性研究的结果表明,白消安/环磷酰胺与 TBI (总剂量为9Gray+环磷酰胺)相比具有非劣效性。对于老年患者,应首选在临床试验中考虑减低强度预处理 (RIC)。最广泛的经验来自一项提供氟达拉滨、美法仑和Alemtuzumab预处理的试验。然而,RIC SCT在老年患者中的作用仍不确定,特别是在有免疫疗法和3 代 TKI 的情况下。
EBMT 最近的两项回顾性研究证实,抗胸腺细胞球蛋白 (ATG)作为预处理一部分时可预防慢性移植物抗宿主病,但与 RR 增加相关,对 OS 无显著影响。G-CSF动员的 PB 干细胞是最常见的干细胞来源。
特定亚组的治疗
青少年和年轻成人
AYA 合并肿瘤是儿童期和成年期过渡的脆弱群体。使用15-39岁来定义基于未修改的儿科方案的治疗策略,同时也认识到15-25岁的患者更容易出现心理社会问题。目前强化 p-b 方案的使用年龄高达55-65岁,但即使在儿童方案的试验中,AYA的结局也低于儿童,相关因素包括疾病生物学的差异、历史上不同的治疗方法和未纳入临床试验,此外心理社会问题可能会降低对持久和复杂方案的依从性。了解这些复杂情况的多学科团队应参与治疗伴ALL的AYA。
AYA的生物学:AYA中 ALL 的发生率低于儿童或老年人,且T-ALL和 LBL 更常见。部分分子学亚型在 AYA 中更常见,如iAMP21、IGH重排、MEF2D重排或 Ph 样ALL。
Ph- ALL:许多历史对照研究阐述了AYA的结局,包括儿童研究或设计用于成人 ALL 的历史研究,并证实儿童治疗策略具有优势。这些观察结果导致不同年龄组的不同策略,包括i)成人患者扩展 p-b 方案,ii)特定 AYA 研究的设置,或iii)儿科研究中年龄上限的扩展;并导致AYA的结局显著改善。目前没有证据表明 AYA 在现代 p-b 方案中的结果劣于未改良的儿科方案。此外,既定方案的任何年龄临界值均应基于明确的依据。
Ph+ ALL:虽然大多数成人组使用减量化疗加TKI,但仍推荐SCT,而儿科医生仍维持强化化疗而减少 SCT 指征,主要是基于早期缓解(包括MRD)。由于该疾病在 AYA 中的罕见性,患者应纳入前瞻性试验。
老年患者(>55-65岁)
许多工作组将未改良的 p-b 方案的年龄上限设定为55岁。最近发表的一篇文章支持这一点,该文章表明,在55-59岁并接受强化 p-b 方案治疗的患者中,CR患者死亡率约为35%。
生物学和临床特征:老年患者通常为B-LIN ALL。不良PF的发生率随年龄增长而增加,如pro-B-ALL(包括 KMT2A 重排ALL)和早期T-ALL),Ph+ ALL (24-51%) 或复杂畸变的发生率较高。老年患者的体能状态经常随着疾病的发作而迅速恶化,合并症也很常见。在一项研究中,通过HCT-CI(造血细胞移植共病评分)评估的任何共病的发生率为76%。早期死亡 (ED) 与共病显著相关。此外,继发性 ALL 在老年人群中更常见。
预后因素:早期死亡风险的潜在 PF包括合并症、年龄和白血病发作前的体能状态。RR的 PF与年轻患者相似。对于减低强度治疗的老年患者中,预期 MRD 持续阳性率较高。因此,有必要对 MRD 进行前瞻性评价,以确定可获益于其他试验性治疗的患者。
治疗:前期治疗可能至关重要,尤其是对于稳定一般状况,其中诱导治疗是治疗的最关键阶段。早期死亡的范围较广 (0-42%)(表3),最常见的原因为感染。即使采用经年龄校正的化疗,仍有超过95%的患者在诱导期间发生Ⅲ~Ⅳ级血液学毒性。瑞典登记研究报告,17%的>55岁患者入住ICU,且强化或姑息治疗的早期死亡相似。
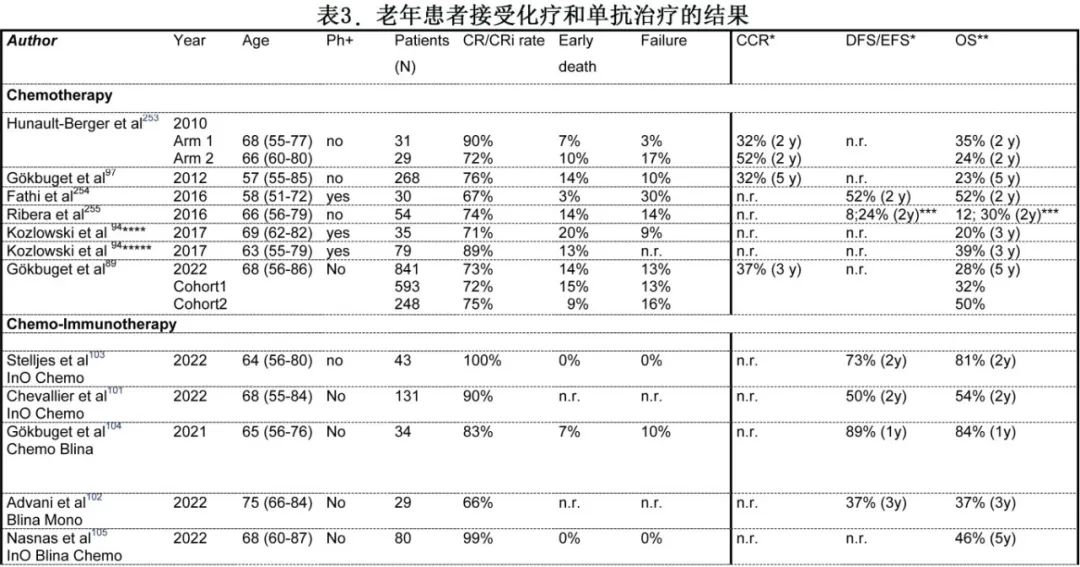
结局:基于人群的研究报告 CR 率为40-70%,OS为6-30%。采用专门为老年 ALL 患者设计的方案,CR 率为43-90%,5年后的OS率低于30-40%(表3)。与年轻患者的方案相同,类固醇和长春新碱是诱导治疗中最重要的药物,但蒽环类药物对 BM 毒性有相当大的贡献,因此核心问题在于,是否必须包括蒽环类药物、哪种类型的蒽环类药物以及哪种剂量强度。一种方法是在诱导中使用伊达比星(具有潜在较低的心脏和肝脏毒性),脂质体蒽环类药物在老年 ALL 中的结果并不令人信服。ASP在老年患者诱导中的耐受性降低,接受强化诱导治疗(包括Dexa、高剂量柔红霉素和2剂PEG-ASP)的60-65岁患者的诱导死亡率为34%,总体而言建议老年患者在巩固治疗后期开始 ASP 治疗。
尽管强化诱导治疗的选择有限,但强化巩固治疗仍有空间。GMALL是目前最大的前瞻性试验,使用 p-b 2期诱导,随后交替巩固周期和维持达2.5年;CD20 阳性 ALL增加8剂Ritux。中位年龄67(55-85) 岁。268例患者 CR 率为76%,早期死亡率为14%,CR死亡率为6%,5年OS 为23%。基于该方案,EWALL定义了老年 ALL 患者的共识治疗方法。Hyper-CVAD方案的 CR 率为88%,CR患者死亡率为31%,5年 OS 为21%。使用最新版本的 GMALL 方案(包括基于 MRD 的免疫治疗),CR 率为75%,早期死亡率为9%,3年OS为50%(表3)。
总体而言,这些标准方案是进一步改善的基础,改善手段包括在巩固治疗中给予适度的时间和剂量强化、考虑RIC SCT和根据 MRD 决定靶向治疗。持续MRD 的B-LIN ALL老年患者应考虑免疫疗法,如Blina;诱导后 PR 或失败的患者也可从 InO 或 Blina 治疗中获益。老年患者也可从化疗基础上加用 Ritux 中获益。
无论 MRD 如何,使用免疫治疗补充或替代化疗均可进一步改善。老年患者对 Blina 和 InO 的耐受性与年轻患者相似。在 InO 联合减量化疗和 Ritux 治疗≥60岁患者的首次经验中,48例可评价患者的 CR 率为98%,78%的患者为 MRD阴性。然而,尽管使用了减量化疗,仍有93%的患者发生 III-V 级感染,17%的患者胆红素或转氨酶升高,81%的患者血小板减少持续时间超过6周,15%的患者发生III-IV 级出血;8%的患者发生静脉闭塞性疾病 (VOD)。然而,CR患者的死亡率为22-25%,3年 OS 为56%。重要的是,试验期间 InO 的剂量共进行了5步调整,且在4个周期InO为基础化疗后,在最新队列中还有进一步调整(增加
Blina)。
在老年患者中,正在进行不同化疗组合的试验以及 Blina 和化疗的序贯试验,并产生了有前景的中期结果。仍需要更长时间的随访,但有趣的是,尽管化疗减少,TRM的风险在部分试验中仍相当高;尤其是>70岁风险细胞遗传学高危患者结局极差。
尽管这些联合治疗方案备受关注,并有望用于老年患者,但与历史数据相比,确定新的标准治疗方案并证明其获益仍具挑战,该获益不仅是获得一线免疫治疗上市许可的必要条件,也是获得不同医疗保健系统报销的必要条件。
Ph/BCR::ABL1阳性(Ph+) ALL
诊断和分子学特征:临床表现和诊断与 Ph- ALL 相当。由于 TKI 的安全性特征,心血管评估尤为重要,并且应关注超声心动图,因为部分 TKI 可能导致 QT 间期延长。Ph+ ALL的确认依赖于核型分析和/或分子遗传学,此外其他染色体畸变也与结局较差相关。BCR::ABL1的 PCR 分析不应是唯一的诊断检查,因为可能遗漏非典型BCR::ABL1转录本,但确定BCR::ABL1亚型对于后续 MRD 分析也很重要。在三分之一的患者中,与 p210 断裂点相比,更常见的 p190 亚型的预后相关性并无明确数据。
治疗原则:TKI可在90-95%的患者中诱导CR,显示低毒性,使更大比例的患者能够接受SCT。应尽早开始 TKI 治疗,因为诱导期间的延迟会降低其疗效。诱导期间可仅依靠 TKI 达到CR,但在实践中,TKI通常与类固醇和长春新碱联合使用;TKI与大多数化疗药物同时给药是可行的。此外CNS预防是强制性的。
诱导和缓解后化疗:前瞻性研究评估了伊马替尼联合非强化诱导,结果显示 CR 率更高、诱导死亡率更低且不影响OS。诱导治疗期间的化疗降级适用于所有年龄组,但尚未普遍采用。由于少数患者可在仅 TKI 诱导后达到深度分子学缓解,因此需要额外的抗白血病治疗作为缓解后治疗(表3)。缓解后治疗通常以1个或2个巩固周期开始,TKI联合更强化的化疗,类似于 Ph-患者的治疗;部分研究小组不鼓励使用ASP。根据合并症、移植风险、年龄、患者偏好和 MRD 水平,进一步的缓解后治疗可包括SCT、继续巩固和维持治疗,或如果认为缓解不满意则转换为替代治疗。巩固治疗后,根据耐受性和疗效,使用初始或其他 TKI 进行维持治疗。不建议非移植患者停用TKI,即使是长期MRD阴性患者。
MRD:Ph+ ALL的 MRD 监测应依赖于 BCR-ABL1 测量,但辅以另一种方法。
激酶结构域 (KD) 突变:BCR::ABL1的KD点突变导致 TKI 治疗期间的大多数复发。BCR::ABL1转录本增加应提示进行突变分析,因为突变类型可提示转换至哪种TKI。大多数情况下ponatinib是 TKI 的首选药物。在明显血液学复发的情况下,即使转换为最合适的 TKI 也很少可诱导长期缓解。灵敏度为1-5%的 NGS 是在 MRD 环境中检测演化突变克隆的首选方法。诊断时低水平突变的临床相关性仍不清楚。
选择TKI:化疗联合伊马替尼或二代 TKI 方案的CR持续时间和 OS 相当,这在一定程度上可归因于 SCT 作为混杂因素。与之相反,一项在儿童患者中进行的随机研究显示,当联合强化化疗时,达沙替尼优于伊马替尼;但研究中伊马替尼剂量低于儿童 ALL 的典型处方剂量。不依赖于 SCT 或联合强化化疗的治疗策略可能从二代和三代 TKI 中获益。因此,一线ponatinib联合 hyperCVAD 具有较高的 CR 率和分子 CR 率,5年 OS(71%) 优于历史对照。在一项纳入新诊断Ph+ ALL患者给予ponatinib联合标准诱导和巩固化疗的2期试验中,3年 EFS 和 OS 率分别为70%和96%(表4)。在245例患者中进行的一项ponatinib与伊马替尼联合减量化疗的随机试验的临床前数据显示,ponatinib的 MRD 缓解率显著更高 (34% vs 17%),而 OS 无差异。
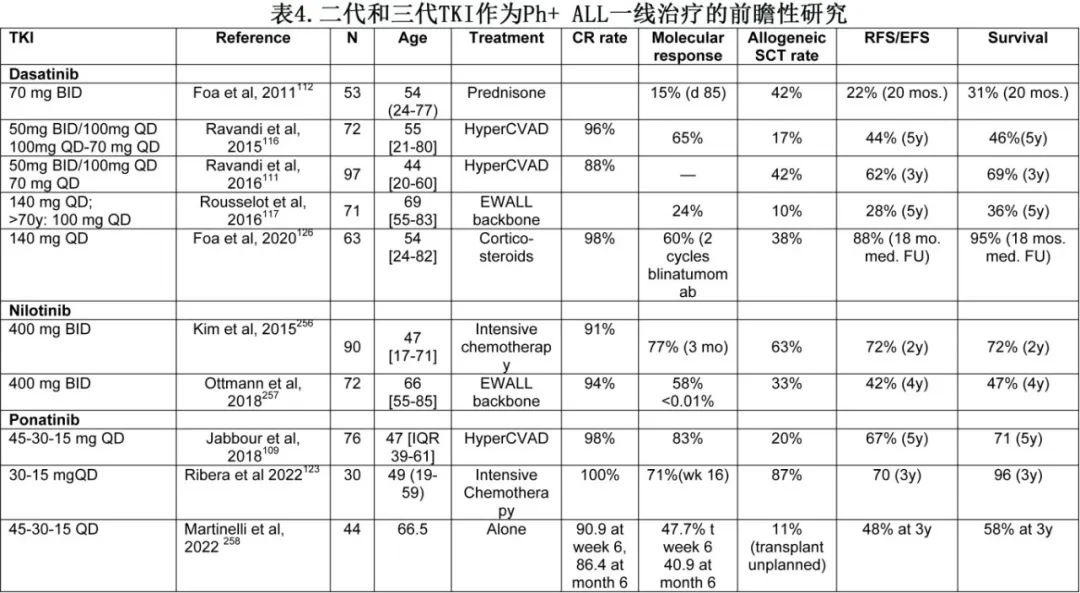
所有TKI均需考虑剂量。对于伊马替尼,维持较高的初始剂量(800mg/天,6-8周)与更好的结局相关。Ponatinib(45mg/天)和尼洛替尼与心血管不良事件有关,达到 CR 时将Ponatinib剂量降低到30 mg/天可降低动脉闭塞事件风险而不会影响疗效;但药代动力学数据不鼓励使用低于 15mg/天 (QD) 的Ponatinib剂量。严密关注血压、血葡萄糖和脂肪的正常化至关重要,需要考虑的其他合并症包括肺部疾病(达沙替尼)和糖尿病(尼洛替尼)。尼洛替尼和Ponatinib可引起临床症状性胰腺炎,特别是在有胰腺炎病史的患者中。选择 TKI 作为一线治疗还取决于治疗方案、合并症和不同医疗保健系统的药物批准。
免疫治疗:TKI联合免疫治疗可增强抗白血病活性,但尚未确定加用 Ritux 是否可增强 Ph-ALL 的疗效。Blina在缓解后治疗时联合达沙替尼高度有效。在这项试验中,除1例患者外所有患者均在达沙替尼治疗后达到CR (98%),两个周期 Blina 治疗后,高达60%的患者获得通过BCR:: ABL1 MRD测量的分子学反应;中位随访18个月时DFS为88%。鉴于发生多次CNS 复发,从而强调了强化 CNS预防的必要性,但SCT的作用仍有待确定,因为约50%的患者根据研究者的选择接受了SCT。几项试验正在评价 TKI 联合 Blina 作为老年Ph+ ALL患者的一线治疗。此外,SCT的作用或可在进行中的随机试验中定义 (NCT06061094)。
CNS预防:达沙替尼可穿过血脑屏障,但 CSF 渗透 TKI 的临床相关性尚未充分描述。因此,预防 CNS 复发是所有TKI方案的重要部分,通常依赖于强化和长期应用 IT 预防。
挽救治疗:除 TKI 外,其他治疗方式与其他 B-LIN ALL 相同;大多数患者会发生 KD 突变。二代和三代 TKI 的缓解率为16-46%,OS为6-9个月;即使接受 SCT 的患者OS也较差。与 SoC 相比,InO治疗R/R Ph+ ALL时观察到缓解率更高、PFS更长和 SCT 率更高,但 OS 无获益。单药 Blina 在R/R Ph + ALL患者中诱导CR/CRh率为36%,包括 T315I 突变患者;中位 RFS 和 OS 分别为6.7个月和7.1个月。在R/R Ph + ALL中同时使用 Blina 和ponatinib获得显著较高的 CR 率 (96%) 和令人鼓舞的OS(中位20个月),且耐受性可接受。CAR-T细胞疗法在Ph+ ALL治疗中的最佳定位仍有待确定。避免复发至关重要,因为挽救治疗疗效仍不佳。除免疫疗法外,BH3抑制剂和新型变构激酶抑制剂 ABL001(asciminib) 也是值得关注的药物;两者均具有良好的毒性特征,并且与Ph+ ALL中可用的治疗方式具有协同作用。
Ph样ALL
约10-30%的 B-LIN ALL 病例具有与Ph+ ALL相似的基因表达谱特征,因此将其命名为BCR::ABL1样或 Ph 样ALL。
诊断:Ph 样ALL首次在成人 ALL 中描述。儿童 ALL 中的一个签名(signature),即BCR::ABL1样,是基于110个基因探针组的分层聚类;257个基因探针组的另一个签名命名为 Ph 样,是基于微阵列 (PAM) 分类器的预测分析。两种分类器的比较发现重叠程度相对较小,只有18%的患者一致分类,但均确定了结局较差的患者和酪氨酸激酶融合基因。两个列表之间只有9个探针组重叠,可能是归因于不同的方法、算法和患者人口统计学。
Ph 样 ALL 的鉴别仍然具有挑战性,并无SoC。15基因 LFS(LDA) 基因表达卡可用于使用定量 RT-PCR 结合数学算法的临床诊断。LDA卡包括 Ph 样 ALL 中最常见酪氨酸激酶基因组病变的基因探针。LDA卡与 PAM 法的一致率为87%。另一种方法为“BCR::ABL1样预测因子”,基于9个特异性过表达基因的 RQ-PCR 定量。为了临床试验的可比性,应明确描述鉴别 Ph 样 ALL 的方法。但没有足够的证据表明需要在临床试验以外的所有患者中预先将 Ph 样 ALL 作为一个整体亚组。
分子学特征:基因组筛查和 NGS 显示其具有高度多样化的畸变,其中包括许多新的融合基因,包括 ABL1 类和 JAK 类融合基因。Ph样 ALL 畸变可分为5个主要亚类。由于大多数研究是在儿童和年轻人中进行的,老年人基因组病变的类型知之甚少,可能存在差异。
发病率:Ph样 ALL 的发病率因地理区域、年龄、参比组和识别方法而异。使用 PAM 分类器,美国队列中青少年和老年人(>39岁)的 Ph 样患者发生率为20-24%,年轻人(21-39岁)的发生率较高,为28%(表5)。但必须注意的问题在于,应指出该发病率是指 B-LIN 作为一个整体还是指命名为 B-其他的组,即无明显细胞遗传学/分子学畸变的组。
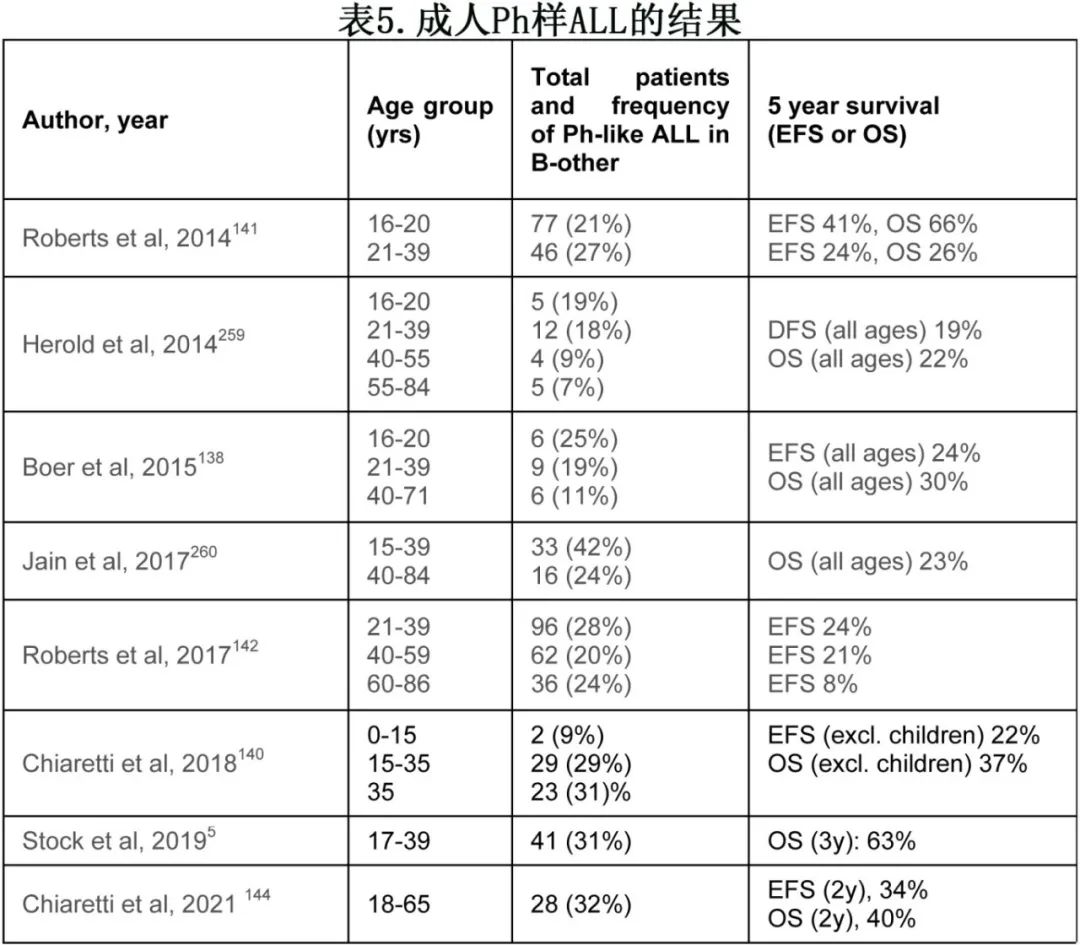
MRD缓解和预后意义:Ph样 ALL 成人患者在诱导治疗后的 MRD 阳性率更高,且与无事件生存期 (EFS) 和 OS 较差相关,70%的 Ph 样 ALL 患者保持 MRD 阳性,这在其他成年人群中也得到证实。关于 MRD 缓解对 Ph 样 ALL 影响的数据相互矛盾,高 RR 并不总是与 MRD 缓解相关。另一方面,标准治疗后 Ph 样 ALL 和阴性 MRD 状态的儿童患者的结局并不差。因此对于该亚组患者,MRD阴性仍存在预后意义。
治疗:新型免疫治疗如 Blina 和 InO 正在研究中,根据治疗成功的阳极报告,似乎有效。大多数工作组依赖于基于 MRD 的方法,如果MRD 反应较差则给予 SCT 和/或靶向治疗。尚无研究证实 SCT 可克服该亚组中较高的RR。
考虑到 Ph 样 ALL 的遗传异质性,该亚型转化至有用的治疗算法仍有挑战。ABL 类融合(通常通过荧光原位杂交鉴定)对SRC/ABL TKI(如伊马替尼和达沙替尼)敏感,并且有几份轶事临床报告。在临床前研究中,JAK2融合、EPOR重排和激活 JAK-STAT 突变对 JAK2 抑制剂芦可替尼高度敏感。另一种方法可能是使用ponatinib。对于临床实践,识别 ABL 融合和基于 MRD 的治疗调整至关重要。
T-ALL
T-ALL 占成人 ALL 的25%,治疗与 B-LIN ALL 相似,标准诱导后通常为含环磷酰胺和阿糖胞苷(AC)的强化期。儿童 T-ALL中强化使用 ASP 高度有效。尚不清楚nelarabine作为巩固治疗是否可改善成人结局。当与 hyper-CVAD 方案联合用于新诊断 T-ALL/LBL 成人时,与历史数据相比,加用nelarabine无 OS 获益。一项随机儿科试验评价了nelarabine治疗新诊断T-ALL/LBL,nelarabine组的5年 DFS 为88%,而非nelarabine组为82%,毒性可接受;OS方面则nelarabine无获益。值得注意的是,nelarabine组的孤立性和合并 CNS 复发率降低。在成人 ALL 中,最近的一项试验未显示一个疗程nelarabine(诱导治疗第二阶段后给药,1.5 g/m2,D1、3、5,共3次给药)具有获益。GMALL 08/2013试验在标危 ALL 中增加了2个周期的nelarabine,并报告了极佳的结局;但nelarabine在该强化 p-b 方案中的确切作用仍有待确定。另一方面,nelarabine在 MRD 阳性未成熟 T-ALL 中的疗效有限(表1)。MDACC报告,与回顾性对照相比,nelarabine治疗患者的 OS 改善,但 ETP ALL 除外,其改善较差。所有成人试验均未发现特定安全性问题。建议尽可能参加基于nelarabine的试验,直至获得更稳健的数据。
对于B-LIN,ALL MRD检测极为重要,并为 SCT 指征提供指导。ETP ALL似乎在化疗后预后较差,不良肿瘤遗传学也应考虑 SCT。老年高危 T-ALL 患者如果有匹配良好的供者,或可从 RIC 中获益。
淋巴母细胞淋巴瘤 (LBL)
LBL 是一种罕见疾病,占NHL的1-3% NHL,其中80-90%为 T 细胞 (T-LBL)。LBL和 ALL 可通过 25% BM 浸润的临界点进行分离。GEP和 SNP 分析显示 T-ALL 和 T-LBL 之间存在差异。T-LBL显示70%的胸腺亚型具有良好结局,而早期 T 型为18%,成熟 T 型为9%。
患者特征和PF:T-LBL以男性为主,最常表现为晚期 III-IV 期,90%的 T-LBL 患者有纵隔巨大肿块,有时伴有胸膜和心包积液。CNS受累占5-10%,淋巴结或其他器官受累占70%且多数 LDH 值增高。与 T-ALL 不同,PB值通常正常。没有广泛接受的不良PF,且在各种试验中存在差异,如 LDH 升高、CNS受累;在一项研究中,基因分类器具有预后性。
治疗:罕见肿瘤溶解综合征,在某些情况下,胸部压迫需要立即使用皮质类固醇进行治疗干预。其治疗应基于 ALL 方案。大多数研究中的 CR 率为70-90%,5年EFS 为60-70%,OS范围也在60-70%之间。CNS预防给药与 ALL 相同。
在早期的研究中,即使残留肿瘤给予24-36 Gy纵隔照射,纵隔复发率仍较高,现在可通过更强化的全身化疗进行弥补。PET 理论上可指导残留病灶的治疗,但确切时间、预测作用和PET阳性后的治疗后果尚未确定。BM或 PB 中的 MRD 可能有助于评价缓解。与单独化疗相比,SCT获得相同的 OS 结果 (70%);但必须考虑 SCT 的已知选择偏倚。因此,SCT适用于第二次 CR 或难治性T-LBL 患者。
复发/难治性 (R/R)ALL
常规化疗挽救治疗
根据方案和亚型,5-10%的患者为原发性难治,另外30-60%的患者会复发。尽管 BM 是最常见的复发部位,但也可发生髓外复发,随着免疫治疗的更广泛使用,发生率甚至可能增加。R/R ALL成人患者接受挽救化疗后的预后较差,根据治疗线的不同,20-40%的患者可获得新的CR,但即使随后进行SCT,缓解也通常并不持久,仅约10-15%的患者实现长期无病生存(DFS) 和治愈,一项包含1706例 R/R Ph-B-LIN ALL 患者的国际研究报告中,3年 OS 率仅为10%。结局的预测因素包括年龄、首次缓解持续时间、对初始挽救治疗的反应和是否适合SCT。对于适合挽救治疗的患者,需根据患者年龄和合并症、疾病特征(例如免疫表型、遗传特征、髓外受累等)、既往治疗类型(包括SCT)和既往缓解持续时间选择治疗方案。R/R ALL是急症,应将患者转诊至有经验的中心以制定综合管理计划,因为挽救治疗的顺序和时间对结局至关重要。所有 R/R ALL患者均应考虑 SCT。
髓外复发的治疗
CNS 是髓外复发的最常见部位。须先进行 CNS 治疗,然后联合全身治疗。CNS内复发通常与全身复发同时发生或可预测全身复发,因此建议立即进行 MRD 检测。尽管静脉或口服 Dexa 通常可快速改善神经系统症状和体征,但应及时开始 IT 治疗,每周两次,直至 CSF 阴性。全身再诱导治疗应包括能够通过血脑屏障的药物,如 HD-MTX 或HD-AC。孤立性或合并 CNS 复发的患者适合SCT,尽管没有数据支持哪种预处理方案,但首选 TBI 方案。在接受TBI为基础预处理的成人中,6 Gy的头颅增强可以耐受。尚无移植后给予额外 IT 治疗的潜在获益或危害的随机数据,具体实践因机构而异。CSF中 MRD 检测可能有助于指导治疗。关于免疫治疗,在接受 CD19 CAR-T 细胞治疗的患者中有报道 CNS 白血病消除。根据部位,其他髓外复发的治疗较个体化,通常尝试化疗或局部治疗(例如放疗),因为免疫治疗的疗效尚不明确。
新的化疗和靶向药物
开发长春新碱脂质体的目的是增加长春新碱在白血病细胞中的药物暴露量,同时将剂量限制性神经毒性降至最低。总缓解率(CR、CRi、PR)为32%,中位缓解持续时间为23周,中位 OS 为4.6个月。25%的患者发生3-4级神经病变。
氯法拉滨是一种获批用于 R/R ALL 儿童的核苷类似物,单药治疗在成人中的缓解率仅为12%。对联合方案(依托泊苷/米托蒽醌、环磷酰胺或阿糖胞苷)的反应范围为17%-36%,但这些方案的毒性较高,妨碍了在大多数患者中使用后续SCT。
Nelarabine获批用于R/R T-ALL/LBL。第一项研究显示,26例成人 R/R 患者的 CR 率为23%。一项包括126例多限治疗的 R/R 成人患者(年龄18-81岁)的大型 II 期研究显示 CR 率为36%,PR率为10%,80%的 CR 患者桥接SCT。约10%的患者发生显著的神经毒性。目前尚不清楚联合治疗是否会产生更高的缓解,随着Nelarabine在一线治疗中的使用增加(见上文),R/R ALL的治疗选择可能更加有限。
免疫疗法
ALL 细胞表面表达的抗原 (CD19、CD20、CD22、CD52) 是单克隆抗体 (MoAb) 的适当靶点,可单药使用或联合化疗,因此开发了 MoAb 和 CAR-T 细胞,并证明它们在主要靶向 B 系 CD19 和 CD22 表面抗原时的高抗白血病活性(表6)。上文已经讨论了一线治疗的数据。在 T-ALL 患者中更难开发抗原靶向性,但目前正在研究靶向CD38、CD3、CD5、CD7、CD1a和 CCR9 的潜力。

Inotuzumab:InO是一种与刺孢霉素(一种细胞毒性抗生素)结合的抗 CD22 抗体,已基于一项随机研究获批用于治疗 R/R CD22 阳性ALL,InO治疗后的 CR/CRi 率为81%,而标准挽救化疗后为33%。在缓解者中,InO组的 MRD 阴性率为78%,对照组为28%;中位 OS 分别为7.7 和6.7个月。InO组中肝脏相关不良事件 (AE) 更常见,静脉闭塞性疾病 (VOD) 的发生率为11% vs 1%。在长期随访中也证实该结果。InO联合化疗能否进一步改善 R/R ALL 的疗效尚不明确。为了降低 VOD 风险,建议在 SCT 前仅给予最多2个周期的InO,避免在预处理中使用双烷化剂,并在 SCT 后严格监测患者的 VOD 体征。InO在高度增殖复发患者中也有效,且在髓外复发中显示出一定的有效性。建议密切监测肝功能检查。
Blinatumomab(Blina):Blina是一种双特异性 T 细胞衔接抗体构建体,能够靶向清除自体 CD3 阳性 T 细胞中的 CD19 阳性 B 细胞,包括 B-LIN 原始细胞。基于一项随机化研究,Blina已获批用于治疗R/R ALL,Blina的 CR/CRi 率为44%,标准挽救化疗为25%;Blina组的 MRD 阴性率为76%,对照组为48%,中位 OS 分别为7.7 和4.4个月。在接受 Blina 作为首次挽救治疗的患者和 BM 浸润低于50%的患者中,获益更明显。关注的 AE包括可管理的细胞因子释放综合征 (CRS) 和一过性神经系统事件。如上所述,在 MRD 阳性 ALL 中观察到Blina 的更有利结果。最近的两项儿科随机研究也研究了 Blina 作为 MRD 首次复发再诱导后治疗和移植桥接的使用。这些研究表明,Blina组的毒性反应较少,MRD缓解率较高,进行 SCT 的可能性更大,DFS和 OS 改善。
基因工程 T 细胞 (CAR-T):靶向 CD19 抗原的 CAR-T 在儿童和成人 R/R ALL 患者中产生了有前景的结果。迄今为止发表的最大型非对照 CAR-T 研究的特征和结果详见表6,中位年龄相对较低,输注患者的总缓解率范围为67-97%,大多数缓解者达到MFC 评估的完全 MRD 缓解。多数患者患有非常晚期的疾病,相当大比例的患者在既往 SCT 后复发。为了使结果与 R/R ALL 的其他方案具有可比性,必须对意向治疗人群进行评价,因为归咎于桥接期间复发或死亡或毒性,并非所有患者均接受预期的 CAR-T 细胞治疗。在主要是儿科 ELIANA 试验中评价了其的总体适用性,筛选的92例患者中有75例 (81%) 接受输注,试验中年龄上限为25岁的依据尚不清楚。该试验导致 tisagenlecleucel 获批用于1-25岁 R/R ALL 患者。
CAR-T治疗成人 ALL 的数据仍有限,临床试验和现实世界的数据表明,其对完全细胞学复发的疗效较差。Zuma-3试验在55例既往多线治疗的成人 R/R ALL 患者中产生了有前景的结果,中位年龄为40(28-52) 岁。共入组71例患者,62%的治疗患者在输注时 BM 浸润>25%。输注患者的 CR/CRi 率为71%,所有患者的 CR/CRi 率为54%;治疗患者的中位 OS 为18个月,中位 RFS 为11.6月。该试验使 Brexucaptagene Autoleucel 获得上市。
与 Blina 相比,CAR-T的 CRS 和神经毒性更常见且更严重,可能是由于大量诱导的 CAR-T 扩增/活化和内皮活化,因此 CAR-T疗法应在具有经过培训的重症监护室的专科中心给药。尚有许多问题仍需阐明,包括 CAR-T 亚群和持久性的影响,既往 alloSCT 和输注时疾病负荷对 CAR-T 疗效的作用,以及是否需要后续 SCT。基因工程“现成”的异基因CAR-T旨在增加程序的适用性和快速性,正在临床开发中。由于 CD19 阴性 ALL 的复发率相对较高,因此还研究了使用双重或双特异性 CAR-T 结合 CD19 和 CD22 靶向的策略。
在所有选项均可及的国家和地区,Blina、InO和 CAR-T 在 R/R B-LIN ALL 中的选择和排序存在争议,尚无明确的建议,因为迄今为止尚未进行对照研究;此外CAR-T细胞的可及性有限。有人可能建议在疾病负荷相对较低且 T 细胞功能保留的患者中支持Blina,而 InO 可用于降低高疾病负荷,尽管试验仅限于外周原始细胞低于 10000/ul 的患者。两种药物的序贯使用(InO 后Blina)也值得关注。CAR-T可能适用于治疗更晚期的疾病,尤其是 SCT 后复发。大多数接受CAR-T治疗的患者都将其作为桥接移植,但CAR-T能否在未来取代 SCT 的问题也具有重要的临床意义。CAR-T输注前 Blina 或 InO 治疗失败的潜在负面影响也需要更大研究评价。尚不清楚既往失败是不良疾病生物学的选择还是存在特定的潜在机制。
其他试验用药物
最有前景的靶向药物是靶向控制细胞增殖和凋亡反应的主要分子学通路的药物(例如多种激酶和BCL-2、TP53、RAS、mTOR/PI3K、前 B/B 细胞受体和 NOTCH 网络)。各种精准医学方法正在研究中,尽管通常仅基于疾病生物学和轶事病例。在前瞻性临床试验中进行进一步研究仍有挑战。使用 FLT3 抑制剂、JAK抑制剂(活化 IL7R 通路病例)、伊马替尼或达沙替尼(NUP214-ABL1突变病例)报告了一些轶事缓解。靶向治疗在 T-ALL 中的发展较少。CD38抗原是 T-ALL 的潜在靶点,已经探索了 CD38 靶向治疗与常规复发治疗的联合治疗。目前正在临床试验中测试用 BCL-2 抑制剂靶向凋亡途径,在47例复发性 T 细胞和 B 细胞疾病患者中评价了选择性 BCL-2 抑制剂联合低剂量navitoclax(BCL-XL/BCL-2 抑制剂),CR率达到60%,28%可继续进行潜在治愈性治疗。通过 NOTCH1 或 FBXW7 基因突变可频繁激活 T-ALL/LBL 中的 NOTCH 通路,导致开发了靶向NOTCH药物,如γ-分泌酶抑制剂 (GSIs) 或 NOTCH 抑制抗体。几个研究组正在尝试开发用于复发性 T 细胞疾病的 CAR-T 细胞,以避免自相残杀(fratricide)和长期 T 细胞再生障碍的问题。来自中国的供者来源 CAR-T 细胞在20例患者中的首次人体试验取得重大进展,疗效高且毒性可接受。
晚期效应
随着成人 ALL 治愈率的提高,晚期效应、生活质量和晚期 AE 预后因素的研究也越来越重要。与健康亲属和一般人群相比,儿童ALL患者的死亡率更高,慢性疾病更多,总体和心理健康受损,功能损害,社会参数更差。GMALL小组最近总结了538例 ALL 治疗长期存活者的医疗状况,66%的患者无合并症,最常见的诊断为感染 (12%)、疲乏 (13%) 和GvHD(15%),而最常受累的器官类别为内分泌(17%男性,24%女性)、神经系统 (27%) 和皮肤 (18%)。晚期效应可能包括一般性激素缺乏、甲状腺疾病、过早绝经、不育、、骨坏死和骨质疏松症、、心脏毒性、神经心理障碍、疲乏和继发恶性肿瘤。SCT患者的晚期效应发生率高于未移植患者,并且可能发生其他晚期效应,如慢性 GvHD 背景下的皮肤疾病、干燥综合征、限制性和阻塞性肺病以及白内障。虽然患者在化疗后可以维持生育能力,但几乎在所有移植患者中均观察到不孕。
缺血性骨坏死也是临床相关问题,尤其是AYA中,类固醇强化治疗是风险因素,而门冬酰胺酶或 HD-MTX 可增强作用。在一项诱导后地塞米松或泼尼松脉冲治疗的儿童研究中,骨骼毒性的总体发生率为13%(11%骨折,4%骨坏死),且接受 Dexa 脉冲治疗的大龄儿童(>10岁 vs <10岁)中发生率较高 (25% vs 11%)。与之不同,UKALL/ECOG2993成人 ALL 研究发现骨坏死的总发生率为4%,年轻(<20岁)患者的发生率高于老年患者。近半数儿童骨坏死患者需接受外科手术。凝血功能紊乱与骨坏死可能存在相关性,PAI-1基因多态性(与血栓形成风险相关)也与儿童 ALL 的骨坏死相关,高甘油三酯血症(ASP的副作用)与骨坏死之间也有潜在相关性。ALL患者中的大多数骨坏死病例发生于治疗的前3年内,髋关节和膝关节是最常见的部位。最敏感的诊断方法是磁共振成像 (MRI),部分作者建议在治疗结束时至少对高危人群进行定期髋关节和膝关节MRI。骨坏死的早期发现、预防和管理是儿童和成人血液科医生面临的主要共同挑战。
心脏毒性,特别是心肌病、心包炎或充血性心力衰竭,多归咎于蒽环类药物,其风险似乎与总药物剂量相关,但也可能较为独特,在较少给药后发生。纵隔照射、感染或联合使用不同的心脏毒性药物等因素可能会增加风险。对于蒽环类药物累积剂量较高的患者,可以选择使用dexroxazone进行心脏保护。心脏毒性,例如表现为射血分数降低的心脏毒性,可能在治疗后数年才表现出来,因此,心血管检查应作为治疗后护理的一部分。
在成人 ALL 患者常见非特异性神经心理障碍,包括关于认知障碍的主诉。对于这种被称为“化疗脑(chemobrain)”的现象,生理学相关性尚不清楚。治愈的 ALL 患者中有相当数量出现疲乏,但疲劳可能在治疗后诊断不足,应通过特定问卷进行检测。
ALL 存活者有较高的癌症发生风险。继发恶性肿瘤的 PF可能包括烷化剂、表鬼臼毒素、CNS照射、SCT前 TBI 预处理以及不同的基因畸变。在成人 ALL 存活者中,最常见的继发恶性肿瘤是造血系统肿瘤,主要发生于化疗结束后的前5-10年内;也观察到多种实体瘤,如乳腺、甲状腺、胃肠道、肺、皮肤、泌尿生殖系统、脑或肉瘤。
对于参与治疗的医生,提供足够的关于治疗和治疗后相关方面的信息非常重要。对已治愈的 ALL 患者的长期观察是正在进行和未来临床试验的重要部分,也是在学术团体财政资源有限的环境中的重大挑战。根据不同的医疗保健系统,专门的晚期效应门诊可以结合儿科和成人血液学团队。
特殊情况的管理
妊娠期ALL
据估计,每10万例妊娠中就有2例发生急性白血病。目前的治疗选择通常基于病例报告和回顾性分析,在很大程度上取决于个人和社会考虑以及胎龄、疾病生物学和患者临床状态的医学考虑。15例在孕期接受治疗的女性与330例非妊娠对照进行比较,证实妊娠不一定影响 ALL 总体结局。患有 ALL 的妊娠女性须在有经验的中心进行管理,并与产科和胎儿医学团队密切合作。治疗手段取决于孕期(三个月)。在孕早期,终止妊娠是强烈考虑因素,因为胎儿安全性会妨碍标准 ALL 治疗的实施;对于后续孕期,许多化疗药物可以安全地给药以达到母体CR,但孕期的任何时间均应避免使用全身性抗叶酸药物。ASP在孕后期的潜在应用存在争议,特别是由于其对凝血的影响,应根据风险-获益比,推迟至分娩后。应考虑使用特异性类固醇促胎肺成熟。分娩应控制在可实现胎儿存活的时间,并在母体造血功能充分的情况下进行。
混合表型急性白血病 (MPAL)
谱系起源不明确的白血病对于诊断和治疗都有困难。在儿科 MPAL 中,建议使用以 ALL 为方向的方案进行初始治疗,缺乏反应时应转换为 AML 方向方案。对成人采用类似的策略也是合理的。对于MPAL,其是CR1期SCT 的一般指征,还是仅在持续性 MRD 病例中SCT的指征,仍存在争议。
继发性 ALL
ALL 作为第二恶性肿瘤(伴或不伴既往恶性肿瘤的细胞毒治疗)越来越被认识。继发性 ALL 发生在多种前期诊断之后,包括乳腺癌、淋巴瘤、骨髓瘤、肉瘤和神经母细胞瘤。如果既往未接受过细胞毒治疗,应怀疑肿瘤抑制基因或癌基因如TP53(Li-Fraumeni综合征)或不匹配的修复基因(MSH2、MLH1、MSH6和PMS2)发生遗传性生殖系突变。对于既往细胞毒治疗后的ALL,美国 SEER 登记研究数据显示,与新发 ALL 相比,中位潜伏期为60个月,中位5年生存期显著更短。来那度胺治疗后发生 ALL 可能是特定的生物学相关性。一般而言,治疗策略与新诊断ALL 相似,但预期毒性风险可能更高。
ALL和唐氏综合征
唐氏综合征 (DS) 患者发生 ALL 的风险增加10-20倍,ALL通常发生在儿童期,与遗传易感性相关,在儿童患者中已充分描述与 DS 相关的ALL。最近描述了 DS-ALL 中发生率更高的三种不同分子亚型(CRLF2重排、C/EBP改变和IGH::IGF2BP1重排)。DS-ALL儿童患者 RR 和 TRM 增加,主要是由于感染。尽管给予 DS-ALL 患者标准治疗,但建议进行一些调整,如减少蒽环类药物和大剂量甲氨蝶呤。强化预防和监测感染是必须的。在临床试验中评估了用免疫疗法替代毒性化疗。DS-ALL成人应参照儿童管理。
支持治疗
EWALL的支持治疗建议已发表(Recommendations of the European Working Group for Adult ALL: UNI-MED Verlag AG, D-28323 Bremen, International Medical Publishers (London,Boston); 2011.)。下文中仅涉及ALL 管理的特定方面。
高WBC:患者出现非常高的 WBC 时,白细胞淤滞和由此导致的组织损伤可能发生于易损毛细血管区域,导致器官受损。可根据出现不明原因的缺氧、神经系统症状、肾衰竭、心肌缺血、阴茎异常勃起或重度视网膜病变诊断为白细胞淤滞。症状性白细胞淤滞的管理是医学急症,可采用白细胞分离术治疗,但不应将其视为促使开始 ALL 治疗(如类固醇预治疗)的替代方法。
肿瘤溶解综合征 (TLS):TLS 风险高的患者(WBC> 100x109/L,高肿瘤负荷)应增加补水 (3l/m²/d),除非有肾功能不全和少尿的证据,以及给予拉布立酶预防治疗。不再推荐尿碱化。难治性液体超负荷、高钾血症、高尿酸血症、高磷血症或低钙血症是肾透析的指征。
抗感染预防治疗:鉴于感染仍然是 CR 死亡的主要原因,抗菌、抗真菌和抗病毒预防以及积极管理感染至关重要。应根据各自的指南进行管理。
生长因子:在 ALL 中预防性给予 G-CSF 可缩短中性粒细胞减少症的持续时间,提高对化疗方案的依从性,在一项研究中降低了感染的发生率。基于这些数据,几十年来,大多数欧洲研究组在其基于儿童的方案中实施G-CSF 的预防性使用。对来自5项欧洲临床试验的长期随访数据进行联合分析,发现 G-CSF 组具有生存优势,尤其是 T-ALL 的DFS(5年DFS 38% vs 24%)和OS(5年51% vs 29%),可能是由于提高了化疗疗程的剂量密集给药及降低8周死亡率(但无统计学意义)。
经期预防:为了在血小板减少期间抑制月经过多并避免化疗期间意外妊娠,孕激素药物连续给药优于联合口服避孕药,尤其是在 ASP 治疗期间及其血栓前状态。对于炔诺酮,暴露于较高剂量与血栓栓塞风险之间无显著相关性;醋酸甲羟孕酮是静脉栓塞高风险患者的首选。使用孕激素药物不应超过6个月,以预防发生脑膜瘤。
保留生育力:作为 ALL 治疗前知情同意的一部分,血液科医生应告知生育期接受治疗的患者发生不育的可能性,讨论生育力保留,并将所有患者转诊至适当的生殖专科医生。在化疗开始前,应建议所有男性进行精子冷冻保存;在女性中,卵巢组织冷冻保存是 SCT 前需要考虑的选择。为控制卵巢组织移植后疾病再引入的风险,正在探索卵巢 MRD 的定量,以决定卵巢再植入。到目前为止,尚未明确推荐使用 GnRH 激动剂 (GnRHa) 保留生育力,特别是由于关于其对卵巢功能不全风险和后期妊娠可能性影响的数据相互矛盾。患者应有机会就不同的可用选择进行咨询,可根据个体考虑使用GnRHa。建议完成化疗后重新评价卵巢功能(AMH、窦卵泡计数)。
总结和展望
充分管理 ALL 的基础是应用综合诊断工具,识别预后因素,包括持续监测MRD。作为前瞻性治疗优化试验的一部分,ALL的标准治疗通常由国家研究组和国际联盟定义。此外,研究组的临床数据库通常包括生物学标志物的综合数据,也是可靠的真实世界数据的来源。
目前标准p-b化疗方案在年轻患者中取得良好的疗效,为了降低发病率和死亡率负担,低毒方案也是重要目标。医疗系统之间的差距正在扩大。在美国,根据NCCN指南,许多新化合物可用于一线治疗,而在大多数欧洲国家还需要特定的上市许可和报销决策。
使用抗体的免疫疗法是R/R ALL的标准治疗,但CAR-T治疗成人ALL的可及性和数据仍有限,治疗手段的排序仍存在挑战。CAR-T治疗SCT后复发的指征已被普遍接受,如果可能的话,也可在MRD复发的情况下。在R/R ALL中,定义充分桥接治疗和决定是否需要后续(第二次)SCT的标准必不可少。
对于Ph+ ALL, TKI的选择、非化疗方案的疗效、TKI改变的指征、不同方法检测的MRD的影响、免疫治疗和HSCT的作用是重要的研究问题。
目前T-ALL预后分型的研究进展较少,且鲜有有前景的新药。尽管T-ALL总体预后良好,但由于复发后生存极差,因此对于预后不良的亚组迫切需要新的治疗方法。
治疗的晚期效应(如骨坏死)与ALL生存率的改善越来越相关,需要儿科和成人研究组的共同努力,以更好地了解生物学,改善监测,并确定潜在的治疗调整。
许多新的治疗方法仅适用于ALL的小亚组,从而对成功的临床试验提出挑战,这也适用于需要整合分子和免疫靶点以及体外反应数据的更个体化复发治疗。这些策略需要国际合作,包括儿科和成人研究组的联合力量。
关于采用复杂联合疗法治疗的 ALL 新药的上市许可和报销,监管先决条件正在扩大。在 ALL 罕见分子亚组中评价新药需要与欧洲药品管理局的欧洲水平合作和组间数据共享,如 Harmony IMI 倡议。临床试验设计的新策略必须与患者代表合作制定,迫切需要通过资助项目支持和维持独立学术研究组的成功基础设施。
在未来几年,随着新的单克隆抗体和细胞疗法整合到一线,这些挑战将变得明显。欧洲和全球正在进行几项临床试验,需要协调以便将来进行荟萃分析。一线治疗不会解决单一药物的影响,而是对新的联合策略、风险分层和 SCT 等方法的影响。有一个主要的研究问题,必将集中于 SCT 在成人和儿童 ALL 中的未来作用。
随着免疫治疗的实施越来越多,未来的 ALL 治疗将基于非常成功的标准,其目标是改善高危患者的预后,但也显著降低所有年龄患者的治疗相关发病率和死亡率。
参考文献
Gökbuget N,et al.Management of ALL in Adults: 2023 ELN Recommendations from a European Expert Panel.Blood . 2024 Feb 2:blood.2023023568. doi: 10.1182/blood.2023023568.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















。ALL在成人肿瘤中相对罕见
25
#指南# #ALL#
29