FDA批准辉瑞Prevnar13肺炎球菌疫苗扩大适用范围
12月30日,FDA批准将辉瑞(Pfizer Inc., PFE)旗下Prevnar 13肺炎球菌疫苗的适用范围扩展至50岁及以上的成年人,以防止肺炎球菌疾病的蔓延,此前FDA已经批准Prevnar 13FDA依照其严重及威胁生命疾病治疗的审批程序,批准了最新的药物使用范围。FDA审查小组在11月份曾经表示,临床资料支持Prevnar 13肺炎球菌疫苗的使用范围扩展,这一疫苗在2
辉瑞,Prevnar13,疫苗,肺炎球菌 - 2012-01-01
FDA批准用于多发性硬化的外骨骼机器人
6月13日,Ekso Bionics公司宣布其外骨骼机器人设备EksoNR获得美国FDA批准,可用于有行走困难的多发性硬化(MS)患者的康复。这是FDA批准的首个用于MS患者康复的外骨骼机器人。
网络 - 多发性硬化症 - 2022-06-17
FDA批准首个急性髓性白血病(AML)靶向新药midostaurin
FDA 4月28日批准诺华Rydapt (midostaurin),用于联合化疗一线治疗携带FLT3突变的新确诊成人急性髓性白血病。FDA同时批准了Invivoscribe Technologies公司的伴随诊断试剂盒LeukoStrat CDx FLT3。
医药魔方 - AML,FDA - 2017-04-30
FDA批准大冢tolvaptan用于治疗常染色体显性多囊肾病
大冢(Otsuka Pharma)公司的托伐普坦(tolvaptan)获FDA批准用于治疗常染色体显性多囊肾病(ADPKD),成为美国第一款ADPKD药物。
MedSci原创 - 常染色体显性多囊肾病,Tolvaptan,血管加压素V2受体拮抗剂 - 2018-04-25
FDA批准诺华脑膜炎疫苗Menveo用于2月大婴儿
诺华(Novartis)8月1日宣布,脑膜炎双球菌疫苗Menveo扩大适应症申请获得了FDA的批准。FDA批准将Menveo用于2个月以上的婴幼儿,预防4株脑膜炎奈瑟菌(血清型A,C,Y和W-135)导致的脑膜炎球菌病。 随着这一扩大适应症的获批,Menveo在美国提供了最为全面的年龄覆盖面。
生物谷 - 新药,FDA - 2013-08-02
FDA批准Shionogi的Mulpleta治疗慢性肝病引起的血小板减少症
美国食品和药物管理局(FDA)近日宣布批准Shionogi的Mulpleta(lusutrombopag)用于治疗慢性肝病引起的成人血小板减少症。FDA于今年2月份接受了血小板生成素受体激动剂Mulpleta的申请,并授予其优先审查资格。
MedSci原创 - Shionogi,Mulpleta,血小板减少症 - 2018-08-01
FDA批准安进/优时比的抗骨质疏松新药Evenity上市
FDA专家组近日通过投票,批准安进Amgen和优时比UCB联合开发的骨质疏松新药Evenity上市。
MedSci原创 - 骨质疏松,骨折,抗硬化蛋白抗体 - 2019-01-26
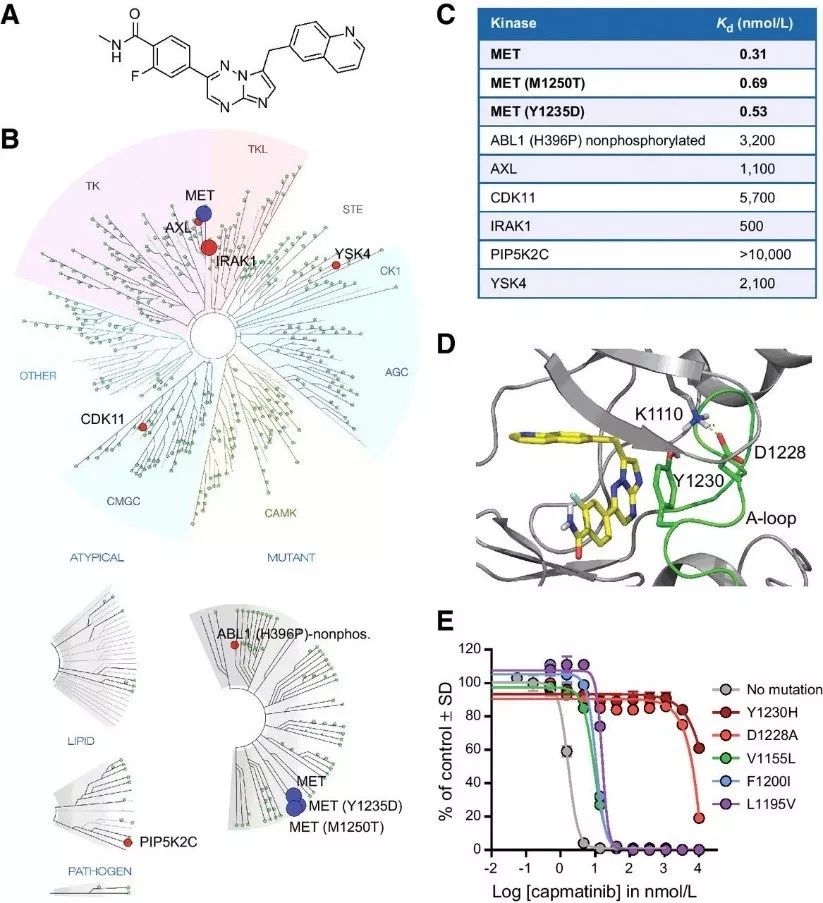
FDA:批准MET抑制剂capmatinib上市用于MET突变NSCLC的治疗
诺华(Novartis)公司宣布,美国FDA批准其MET抑制剂Tabrecta(capmatinib)上市,治疗携带MET基因外显子14跳跃突变的晚期非小细胞肺癌(NSCLC)患者。这些患者的基因突变
MedSci原创 - NSCLC,Capmatinib - 2020-05-07
FDA:2020年一季度批准11款新药信息汇总
2020年第一季度,FDA共批准11个新药上市,其中1月份3个,2月份5个,3月有3个(此处所列新药,主要指FDA批准的新分子实体(NME)、新生物制品、细胞疗法、基因疗法,不包括疫苗)
MedSci原创 - FDA,新药 - 2020-04-04
FDA批准Renovis公司3D打印颈椎间融合系统上市
2016年3月30日,医疗植入物生产商Renovis Surgical Technologies公司宣布,该公司的3D打印TeseraSC——多孔钛颈椎椎间融合系统——已经获得美国食品药品管理局(FDA
MedSci原创 - 椎间融合,颈椎,3D打印 - 2016-04-03
FDA批准Seattle Genetics的Adcetris治疗外周T细胞淋巴瘤
Seattle Genetics公司近日宣布,其Adcetris(brentuximab vedotin)与化学疗法相结合的方案,获得了美国的批准,以治疗患有先前未治疗的全身性间变性大细胞淋巴瘤(sALCL
MedSci原创 - Seattle,Genetics,Adcetris,外周T细胞淋巴瘤 - 2018-11-18
最畅销艾滋病药Truvada首个仿制药获FDA批准上市
近日,美国FDA批准了梯瓦制药(Teva)生产的防止版Truvada(主要含200mg恩曲他滨和300mg富马酸替诺福韦二吡呋酯)上市,用于联合其他抗逆转录病毒药物治疗成人及儿童HIV- 1感染以及成人高危人群的
医谷 - Truvada - 2017-06-15
礼来旗下来得时仿制药Basaglar获FDA暂时批准
礼来为其赛诺菲来得时仿制药获得“暂时性”FDA批准,但近期在药房中还找不到这款药。据礼来称,FDA认为Basaglar达到了赢得上市批准的条件,但在2016年中期之前,赛诺菲却把握着这款产品上市的关键,
dxy - 仿制药,礼来 - 2014-08-25
FDA批准Ofev对于特发性肺纤维化的治疗
美国食品和药物管理局于10月15日批准了Ofev(nintedanib)对于特发性肺纤维化(IPE)的治疗。 特发性肺纤维化是一种肺部随时间逐步瘢痕化的疾病。“今天对于Ofev的批准增加了患有特发性肺纤维化这种严重慢性疾病的患者的可用治疗选择”,FDA药物评价
医学论坛网 - Ofev,特发性肺纤维化,FDA - 2014-10-28
FDA批准首款脑膜炎球菌血清群B疫苗Trumenba
10月29日,美国食品与药物管理局(FDA)宣布,通过加速审批通道批准了首款用于预防脑膜炎奈瑟球菌血清群B引起的侵袭性脑膜炎球菌病的疫苗Trumenba,该疫苗适用于10至25岁人群。
医学论坛网 - 脑膜炎球菌,血清群B,疫苗,Trumenba - 2014-11-05
为您找到相关结果约500个