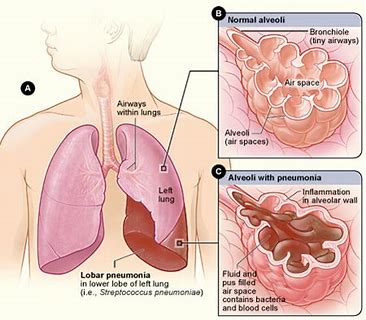
RECARBRIO(亚胺培南、西司他丁和雷巴坦)或能“力克”呼吸机相关细菌性肺炎
RESTORE-IMI 2是一项随机、对照、双盲的III期临床试验,旨在评估RECARBRIO治疗成人医院获得性或呼吸相关细菌性肺炎。
MedSci原创 - 细菌性肺炎,Recarbrio,亚胺培南 - 2020-05-06
FDA 指导文件:在 ANDA 中提交的外用药物产品的体外释放试验研究
本指南旨在帮助申请者提交适用于皮肤的液体和/或其他半固体产品的简化新药申请 (ANDA),包括外皮和黏膜(如阴道)膜,以下称为
FDA - 外用药物,体外释放试验研究 - 2022-11-10
TREAKISYM获批成为低度B细胞非霍奇金淋巴瘤和套细胞淋巴瘤抗癌剂
®(通用名:盐酸苯达莫司汀)已在日本获得批准,作为低度B细胞非霍奇金淋巴瘤和套细胞淋巴瘤(MCL)的一线抗癌剂。 /* Style Definitions */ span.prnews_span { font-size:8pt; font-family:"Arial"; color:
卫材(中国)药业有限公司 - 美通社,白血病 - 2017-01-19
FDA指南:生物相似性和可互换性:关于生物仿制药开发和BPCI法案(修订版1)的附加问答草案
本指导文件草案修订了2020年11月发布的题为“生物相似性和可互换性:关于生物仿制药开发和BPCI法案的补充问答草案”的指导文件草案,以保留草案中的适当问答。
FDA官网 - 生物相似性 - 2023-11-30
又一省发文,未过一致性评价不采购
10月10日,湖南省卫计委发布《关于做好新药和通过仿制药质量和疗效一致性评价品种供应保障工作的通知》。
赛柏蓝 - 一致性评价,仿制药,湖南 - 2018-10-12
女性滴虫病的治疗:Solosec®(secnidazole)的III期临床取得积极结果
Lupin制药公司今天公布了其关键III期临床试验的顶线结果,该试验评估了单剂量Solosec®(secnidazole)治疗女性滴虫病的有效性和安全性。
MedSci原创 - secnidazole,滴虫病 - 2020-05-04
报告称:糖尿病患病率升高 降糖药市场多年保持增长
广州4月21日电 (蔡敏婕)医药健康领域的数据信息服务平台米内网21日发布消息称,内地公立医院渠道的降糖药市场连续多年来保持增长,目前已经突破510亿元。
中新网 - 糖尿病,降糖药 - 2020-04-22
再鼎医药的PARP抑制剂Niraparib用于卵巢癌维持治疗,获得NMPA授予优先审查
再鼎医药宣布,国家药品监督管理局(NMPA)为其PARP抑制剂Niraparib的补充新药申请(sNDA)授予优先审查地位。
MedSci原创 - 卵巢癌,NMPA授予优先审查,PARP抑制剂Niraparib - 2020-04-18
雾化Ensifentrine治疗慢性阻塞性肺疾病(COPD):即将开展III期临床试验
Verona Pharma已启动一项III期临床试验(ENHANCE研究),以评估雾化Ensifentrine治疗中度至重度慢性阻塞性肺疾病(COPD)的安全性和有效性。
MedSci原创 - COPD,COPD药物,雾化吸入治疗,ensifentrine,慢性阻塞性肺疾病与肺心病 - 2020-09-28
奥希替尼新适应症上市申请获FDA优先审评资格
阿斯利康宣布FDA接受其提交的奥希替尼补充新药申请(sNDA),并授予优先审评资格,用于对接受过完全肿瘤切除术的早期(IB、II和IIIA期)表皮生长因子受体突变(EGFRm)非小细胞肺癌(NSCLC
医药魔方 - FDA,中枢神经系统,优先审评 - 2020-11-04
罗沙司他全球III期临床研究证实其心血管安全性
近日,阿斯利康公布其罗沙司他全球III期临床研究心血管(CV)安全性汇总分析结果。罗沙司他是全球首个低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI),也是首个在中国获批上市的肾性贫血口服新药,已于2018年12月获得国家药品监督管理局(NMPA)的上市批准,用于慢性肾脏病透析患者的贫血治疗
生物谷 - 罗沙司他,心血管 - 2019-05-17
发展植物提取物产业 推动中药现代化进程
医药品市场巨大,但一直以来,制药业却因为创新药物甚少而举足不前,行业需要寻求新的发展方向。中药便成了探索之一,在中国相传数千年的中药,如今日渐成为西方制药公司提取有效成分的药材。
会议 - 2008-09-08
FDA使用说明 — 人用处方药和生物制品的患者标签 — 内容和格式
本指南为开发人用处方药和生物制品以及根据新药申请 (NDA) 提交的药物主导或生物主导组合产品的患者使用说明 (IFU) 文件的内容和格式提供了建议,或 生物制品许可申请 (BLA)。
FDA - 药品标签 - 2022-08-09
FDA 表格3926:个体病人扩展用药计划(EAP)申请
本指南描述了来自 FDA 3926(个体患者扩展用药 - 研究性新药申请 (IND)),该指南可供获得许可的医生用于针对个体患者 IND 的扩展访问请求。在使用研究药物治疗患者的情况下,偶尔也会使用同
FDA - EAP临床试验 - 2021-11-26
为您找到相关结果约500个