Annamycin治疗软组织肉瘤,已获得FDA“孤儿药称号”
肉瘤是一类间充质细胞来源的罕见异质性恶性肿瘤,占所有成人恶性肿瘤的不到1%,占儿科癌症的12%。约80%的新发肉瘤来源于软组织,其余来源于骨。
MedSci原创 - 软组织肉瘤,孤儿药称号,FDA孤儿药称号,Annamycin - 2020-12-30
君实生物特瑞普利单抗治疗小细胞肺癌获得美国FDA孤儿药资格认定
这是特瑞普利单抗获得的第五项孤儿药资格认定,此前特瑞普利单抗治疗黏膜黑色素瘤、鼻咽癌、软组织肉瘤及食管癌已分别获得FDA孤儿药资格认定。
网络 - 小细胞肺癌,君实生物,FDA孤儿药,特瑞普利单抗注射液(拓益®) - 2022-04-14
阿斯利康承认子公司抗癌药临床数据造假,刚获突破性疗法认定
欧洲制药巨头阿斯利康(AstraZeneca)近日承认,其旗下一家子公司在一个突破性抗癌药的临床研发中数据造假。据制药行业专业媒体Pharmafile报道,阿斯利康发现,其控股公司Acerta Pharma在研发新型实验性抗癌药物Acalabrutinib的过程中伪造了部分临床有效性数据。该药物在今年8月刚刚被美国食品药品管理局(FDA)授予了突破性疗法认定。目前阿斯利康正在调查该药物的表现,涉及
澎湃新闻 - 阿斯利康,抗癌药,FDA,临床数据造假 - 2017-10-18
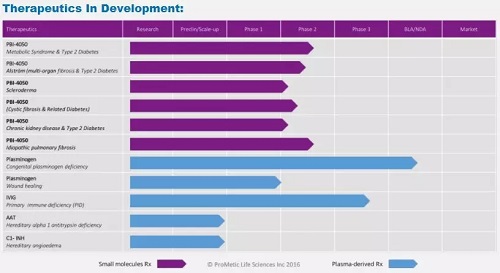
新疗法获FDA两大认证
近日,总部位于加拿大魁北克省的Prometic Life Sciences公司宣布,其针对坏死性小肠结肠炎(necrotizing enterocolitis,NEC)的疗法Inter-Alpha-Inhibitor-Proteins(IAIP)获得美国FDA颁发的儿科罕见病认证(Rare Pediatric Disease Designation)。FDA儿科罕见病认证旨在帮助医药公司开发用于1
药明康德 - 早产新生儿,FDA,孤儿药 - 2018-03-08
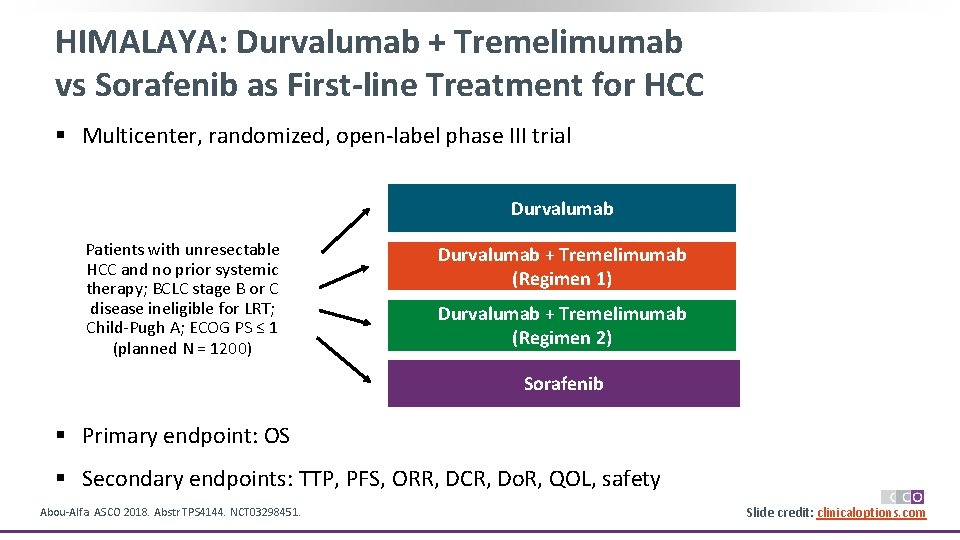
Imfinzi联合tremelimumab治疗肝癌,III期试验显示可提高总体生存率
阿斯利康的药物组合Imfinzi联合tremelimumab已被证明可显著提高一线不可切除肝癌患者的总生存期。
MedSci原创 - Tremelimumab,Imfinzi,PD-L1单抗Imfinzi - 2021-10-15
瑞德西韦获得FDA孤儿药认定
根据美国《金融邮报》的报道,FDA已授予吉列德科学(Gilead)公司的实验性药物瑞德西韦(remdesivir)孤儿药认定,以作为COVID-19的潜在治疗药物。
MedSci原创 - 瑞德西韦,Covid-19,COVID-19肺炎,孤儿药 - 2020-03-24
α-1抗胰蛋白酶(A1AT)缺乏症治疗或取得重大突破:DCR-A1AT获得孤儿药认定
Dicerna Pharmaceuticals致力于核糖核酸干扰(RNAi)药物的开发,近日宣布,美国食品药品监督管理局(FDA)已授予RNAi候选药物DCR-A1AT孤儿药认定。
MedSci原创 - α-1抗胰蛋白酶,α-1抗胰蛋白酶缺乏,DCR-A1AT - 2020-03-19
囊性纤维化候选药物SNSP113获得欧盟孤儿药物认定
Synspira Therapeutics近日宣布,欧洲药品管理局(EMA)孤儿药品委员会(COMP)已授予该公司的SNSP113以孤儿药物认定。
网络 - SNSP113,囊性纤维化,孤儿药物认定 - 2019-04-11
第十届中国罕见病高峰论坛在杭举行,真实世界数据研究在罕见病中应用渐入佳境
2021年9月10日-12日,第十届中国罕见病高峰论坛在杭州隆重召开。会议以“罕路同行 十载与共”为主题,由蔻德罕见病中心(CORD)、浙江大学医学院、浙江大学医学院附属第二医
MedSci原创 - 真实世界,真实世界证据,真实世界数据,真实世界研究,真实世界管理 - 2021-09-13
君实“特瑞普利单抗”:首个获得FDA突破性疗法认定的国产PD-1
今日,君实生物发布公告称,其“特瑞普利单抗注射液”用于鼻咽癌的治疗获得FDA突破性疗法认定,特瑞普利单抗成为首个获得FDA突破性疗法认定的国产抗PD-1单抗,这是继2020年5
亿欧 - PD-1,特瑞普利单抗,FDA突破性疗法指定 - 2020-09-10
NEJM:局部应用基因治疗营养不良性大疱性表皮松解症
营养不良性大疱性表皮松解症,也称大疱性表皮松解症(DEB)是一种罕见的严重疾病,影响皮肤和粘膜组织。该病是由COL7A1基因中的一个或多个突变引起,该基因负责产生VII型胶原蛋白(COL7),形成将真
MedSci原创 - 基因治疗,营养不良性大疱性表皮松解症 - 2022-12-20
FDA:合格传染病产品指定问答
本指南向申办者提供有关 FDA 实施食品和药物管理局安全与创新法案 (FDASIA) 标题为“立即产生抗生素激励措施 (GAIN)”的第八章的信息。 GAIN 条款为开发治疗严
FDA - 传染病 - 2021-10-22
FDA批准高三尖杉酯碱皮下注射剂上市
10月26日,美国食品与药物管理局(FDA)通过加速审批程序批准了“孤儿药”高三尖杉酯碱(omacetaxine mepesuccinate)用于治疗成人慢性髓性白血病(CML)。Synribo预期用于那些至少用2种酪氨酸激酶抑制剂药物(TKIs)治疗后疾病仍有进展的患者。 该药为皮下注射剂,2次/天,连续注射14天,28天为一疗程直至白细胞计数正常。
FDA - 慢性髓性白血病,高三尖杉酯碱,酪氨酸激酶抑制剂 - 2012-10-30
强生单抗药Sylvant获FDA批准
强生(JNJ)旗下杨森研发单元(Janssen)4月23日宣布,FDA已批准单抗药物Sylvant(siltuximab),用于HIV阴性和人类疱疹病毒-8(HHV-8)阴性的多中心型巨大淋巴结增生症(multicentric Castleman's disease,MCD)患者的治疗。此前,siltuximab已被授予孤儿药地位。 Sylvant是一种单克隆抗体,是IL-6拮抗剂,通过静脉输注
生物谷 - 新药,FDA - 2014-05-12
为您找到相关结果约500个