FDA授予Prevail公司的帕金森基因疗法快速通道指定
美国食品和药物管理局(FDA)已授予Prevail Therapeutics公司的帕金森病候选药物PR001 快速通道指定,用于GBA1突变的患者,该类患者占帕金森病患者的7%至10%。
MedSci原创 - 帕金森,基因疗法,快速通道指定 - 2019-07-13
GRANITE-001获得FDA快速通道指定用于治疗结直肠癌
Gritstone Oncology是一家临床阶段生物技术公司,致力于开发下一代癌症免疫疗法以对抗多种癌症,近日宣布GRANITE-001已经获得FDA快速通道指定用于治疗结直肠癌。
MedSci原创 - GRANITE-001,FDA,快速通道指定 - 2018-12-22
DiscGenics用于治疗椎间盘退变的细胞疗法,获得FDA快速通道指定
DiscGenics,一家临床阶段生物技术公司,专注于开发基于再生细胞的疗法,可缓解脊柱退行性疾病患者的疼痛和恢复功能,今天宣布美国食品和药物管理局(FDA)已批准其研究性细胞疗法IDCT的快速通道指定
MedSci原创 - DiscGenics,椎间盘退变,细胞疗法,FDA快速通道指定 - 2019-08-27
Alnylam的RNAi疗法Vutrisiran获得FDA快速通道指定,治疗hATTR淀粉样变性
RNAi疗法vutrisiran靶向和沉默特定的信使RNA,从而阻止野生型和突变型甲状腺素转运蛋白(TTR)的产生。
MedSci原创 - hATTR淀粉样变性,FDA快速通道指定,RNAi疗法vutrisiran - 2020-04-15
Moderna的mRNA纳米药物(mRNA-3927)治疗丙酸血症,获得FDA快速通道指定
Moderna公司宣布美国食品药品监督管理局(FDA)授予在研的mRNA治疗药物mRNA-3927快速通道称号,用于治疗丙酸血症(PA)。
MedSci原创 - Moderna,mRNA纳米药物,mRNA-3927,丙酸血症,FDA快速通道指定 - 2019-10-23
非酒精性脂肪性肝炎新药HM15211,获得FDA快速通道指定
Hanmi Pharmaceutical表示,其HM15211治疗非酒精性脂肪性肝炎获得FDA的快速通道指定。
MedSci原创 - 非酒精性脂肪性肝炎(NASH),FDA快速通道指定,HM15211 - 2020-07-17
Agenus的PD-1单抗Balstilimab治疗晚期宫颈癌,获得FDA的快速通道指定
Agenus公司宣布,美国食品和药品管理局(FDA)已为其PD-1单抗balstilimab用于治疗宫颈癌,授予了快速通道指定。
MedSci原创 - 转移性宫颈癌,PD-1单抗Balstilimab,抗CTLA-4单抗zalifrelimab - 2020-04-08
FDA授予ADC药物sacituzumab govitecan快速通道指定,用于治疗转移性尿路上皮癌
Sacituzumab govitecan是一种新型的抗体药物偶联物(ADC),由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。
MedSci原创 - 抗体药物偶联物,局部晚期或转移性尿路上皮癌,Sacituzumab govitecan - 2020-04-08
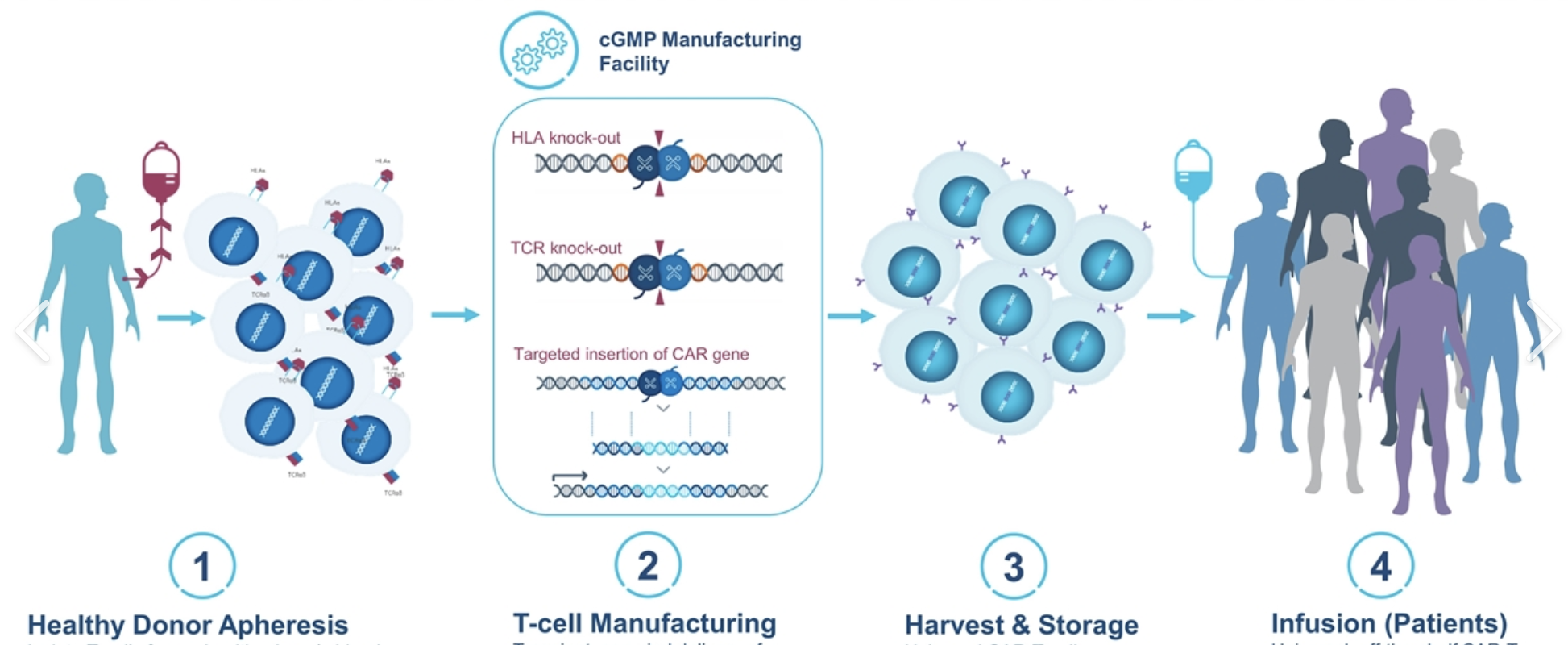
同种异体CAR-T细胞疗法治疗白血病,获得FDA的快速通道指定
同种异体嵌合抗原受体(CAR-T)细胞疗法PBCAR0191治疗晚期前体B细胞急性淋巴细胞白血病,获得FDA快速通道指定。
MedSci原创 - 白血病,FDA快速通道指定,同种异体CAR-T细胞疗法 - 2020-08-20
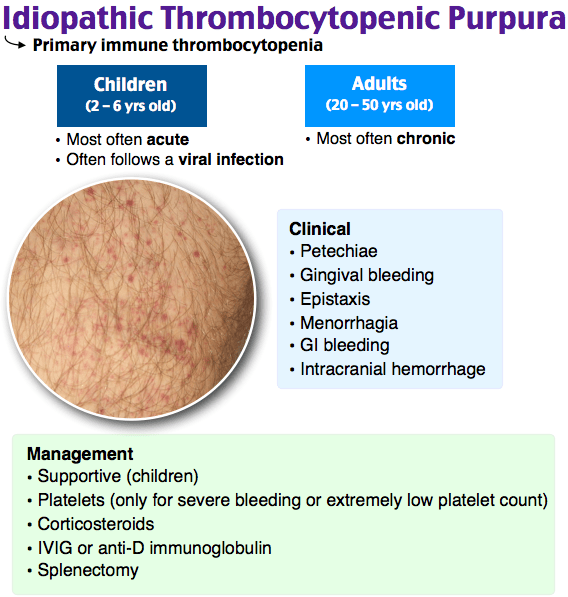
BTK抑制剂Rilzabrutinib治疗免疫性血小板减少症:被授予FDA快速通道指定
Rilzabrutinib很可能成为治疗免疫性血小板减少症(ITP)的首款BTK抑制剂。
MedSci原创 - 免疫性血小板减少症,BTK抑制剂Rilzabrutinib - 2020-11-19
Themis Bioscience公司的基孔肯雅热预防疫苗获得了FDA快速通道指定
专注于传染病和癌症免疫调节疗法的生物制药公司Themis Bioscience今天宣布,美国食品和药物管理局(FDA)已授予其预防基孔肯雅病的候选疫苗( MV-CHIK)快速指定。
MedSci原创 - 基孔肯雅热,疫苗,预防,快速通道指定 - 2019-02-25
非阿片类镇痛药EC5026治疗神经性疼痛:获得FDA授予快速通道指定
EC5026是一种口服小分子,可抑制sEH,而EH是内源性抗炎脂肪酸代谢的关键调节酶。抑制sEH可通过阻止这些天然止痛和抗炎脂肪酸的分解,引起脂肪酸在细胞内的累积进而治疗疼痛。
MedSci原创 - 神经性疼痛,FDA授予快速通道指定,非阿片类镇痛药EC5026 - 2020-04-10
Immunocore的tebentafusp治疗转移性葡萄膜黑色素瘤被FDA授予快速通道指定
T细胞受体(TCR)生物技术公司Immunocore的候选药物tebentafusp(IMCgp100)获得FDA快速通道指定治疗转移性葡萄膜黑色素瘤(mUM)。
MedSci原创 - tebentafusp,转移性葡萄膜黑色素瘤,快速通道指定 - 2019-04-04
上周获批II期临床后,Moderna新冠病毒mRNA疫苗又获得FDA授予的快速通道指定
Moderna公司宣布其针对新型冠状病毒(SARS-CoV-2)的mRNA疫苗候选物(mRNA-1273),获得了FDA授予的快速通道指定。
MedSci原创 - 新型冠状病毒,mRNA疫苗 - 2020-05-13
Orphazyme的热休克蛋白疗法Arimoclomol治疗肌萎缩性侧索硬化症,获得美国快速通道指定
Arimoclomol通过增加热休克蛋白的产生,帮助挽救错误折叠的蛋白,清除蛋白聚集体来治疗肌萎缩性侧索硬化症。
MedSci原创 - 肌萎缩性侧索硬化症,热休克蛋白疗法,Arimoclomol - 2020-06-03
为您找到相关结果约500个