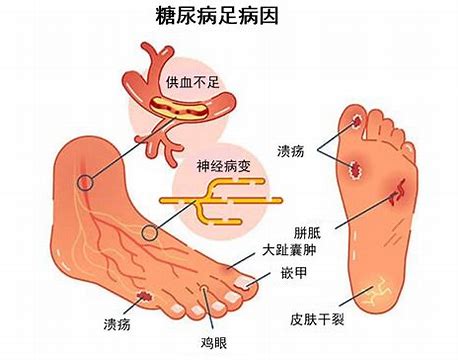
FDA“糖尿病足感染:开发治疗药物的供企业用的指导原则草案”介绍
美国食品药品监督管理局(FDA)于2023年11月发布了“糖尿病足感染:开发治疗药物的供企业用的指导原则(草案)”。该指导原则草案提出了糖尿病足感染治疗药物临床开发的建议,包括
药物评价研究 - 糖尿病足 - 2024-04-07
FDA 行业指南:《药品供应链安全法》行业指南下可疑产品和非法产品的验证义务定义
药品供应链安全法 (DSCSA)(公法 113-54 标题 II)修订了联邦食品、药品和化妆品法(FD&C 法),以建立对某些药品的产品追踪、验证和产品标识的要求分布于美国。FD&C
FDA - 药品供应链安全法 - 2023-03-25
FDA 指导文件:艰难梭菌感染的开发治疗药物、减少复发和预防
美国食品和药物管理局(FDA 或机构)宣布推出题为“艰难梭菌感染:开发用于治疗、减少复发和预防的药物”的行业指南草案。本指南草案的目的是协助申办者临床开发治疗艰难梭菌感染(CD
FDA - 艰难梭菌,艰难梭菌感染 - 2022-11-09
FDA指南:研究数据技术一致性指南 - 技术规格文档
本技术规范文件代表了美国食品和药物管理局(FDA)目前对这一主题的看法。它不会为任何人创造或授予任何权利,也不会对FDA或公众产生约束力。
FDA官网 - 研究数据 - 2023-12-06
中药配方颗粒调剂技术规范专家共识(2022年版)
中药配方颗粒自2001年7月国家食品药品监督管理局发布《中药配方颗粒管理暂行规定》(国药监注[2001]325号)中被正式命名;2001年12月1日起纳入中药饮片管理范畴,并陆续批准企业试点生产。中药
医药导报 - 中药配方颗粒调剂 - 2022-08-13
FDA官网:根据FD&C法案第506C条,通知FDA成品或活性药物成分的生产中止或中断
美国食品和药物管理局(FDA)宣布推出一份名为“根据FD&C法案第506C条永久停止或中断生产的通知”的行业指南草案。该指南草案旨在帮助申请人和制造商及时向FDA提供关
国家药品监督管理局官网 - 活性药物 - 2024-02-08
国家药监局锝标记及正电子类放射性药品检验机构评定程序
国家药监局组织制定了锝标记及正电子类放射性药品检验机构评定程序,现予发布,自发布之日起施行。
国家药品监督管理局官网 - 放射性药品 - 2024-03-15
脊髓电刺激治疗慢性疼痛专家共识
慢性疼痛(chronic pain)原因及发病机制复杂,持续时间长,治疗方法手段多样,临床疗效不尽如人意,成为广受关注的医疗和社会问题。近年来,采用以脊髓电刺激(spinal cord stimula
中国疼痛医学杂志. 2021,27(06 - 慢性疼痛 - 2021-07-15
2023 ACIP建议:应用Nirsevimab预防婴幼儿呼吸道合胞病毒疾病
本文主要针对Nirsevimab在预防婴幼儿呼吸道合胞病毒疾病中的应用提供指导建议。
MMWR Morb Mortal Wkly Rep - 呼吸道合胞病毒,Nirsevimab - 2023-08-25
2024 FDA指南:考虑在第564条宣布的紧急状态期间进行测试的执行政策
FDA发布本指南草案,以描述我们在决定根据《联邦食品、药品和化妆品法》(FD&C Act)第564条在未来宣布的紧急情况下发布有关测试制造商提供某些未经批准的测试的执行政策时打算评估的因素。
FDA官网 - 公共卫生 - 2024-05-05
FDA 行业指南:慢性鼻窦炎伴鼻息肉的开发治疗药物
本指南阐述了 FDA 目前对正在开发的用于治疗 CRSwNP 的药物的试验人群和设计、有效性、统计分析和安全性的想法。
FDA官网 - 慢性鼻窦炎,慢性鼻窦炎鼻息肉 - 2023-06-30
FDA 指南:长效局部麻醉药品的开发
美国食品药品监督管理局(FDA 或 Agency)宣布提供一份名为“开发具有延长作用持续时间的局部麻醉药物产品”的行业指南草案。
FDA - 长效局部麻醉药品 - 2023-03-25
FDA提供电子和非电子格式的监管提交——人用处方药的促销标签和广告材料
本指南适用于由制造商、包装商和分销商(公司)向食品药品监督管理局(FDA 或机构)提交的人用处方药(药品)宣传材料,无论是申请人还是代表申请人行事的实体 . 具体而言,本指南适用于向药物评估和研究中心
FDA - eCTD - 2022-08-05
FDA急性疼痛非阿片类镇痛药的开发(草案)
本指南是根据《促进患者和社区的阿片类药物恢复和治疗 (SUPPORT) 法案》第 3001(b) 节的法定要求编写的,该法案指示食品和药物管理局 (FDA) 发布 或更新现有指南,以帮助解决开发非成瘾
FDA - 疼痛,镇痛,非阿片类药物,非阿片类 - 2022-08-05
为您找到相关结果约500个