【Leukemia】小剂量阿糖胞苷治疗新诊断成人朗格汉斯细胞组织细胞增生症的中国2期研究结果
2024-02-25 聊聊血液 聊聊血液 发表于上海
北京协和医院开展一项2期、前瞻性、单中心研究,旨在评估小剂量阿糖胞苷方案在初诊MS或SS-M LCH成人患者中的疗效和安全性。
阿糖胞苷治疗成人LCH
朗格汉斯细胞组织细胞增生症(Langerhans cell histiocytosis, LCH)是一种罕见的异质性组织细胞疾病,可发生于所有年龄,但最常见于10岁以下儿童,高峰为1-3岁,因此成人误诊率较高。LCH根据受累部位和范围可分为单病灶、单系统肺、单系统多灶(SS-M)和多系统(MS)疾病。2010年首次在57%的LCH样本中发现了反复激活的BRAFV600E突变,此后又发现了MAPK通路的其他激活突变,因此LCH重新分类为髓系肿瘤。LCH的年发病率估计为0.5/100000~5.4/100000,男性稍多,成人LCH发病率低。
由于缺乏前瞻性研究数据,成人SS-M和MS LCH患者的最佳治疗策略尚不明确,包括手 术治疗、放疗、化疗,或几种方法的联合治疗。回顾性研究采用从儿科经验推断出的化疗方案,显示复发率较高。克拉屈滨在初诊和复发难治患者中显示出较高的总缓解率(ORR)和长期缓解的潜力,但不良事件比例高且患者数量有限。对于一线治疗难治性或有终末器官功能障碍的LCH,推荐使用靶向治疗(BRAF或MEK抑制剂),但持续时间未明确。长春新碱联合糖皮质激素治疗成人LCH的复发率为71.0~78.6%。前瞻性研究使用甲氨蝶呤和阿糖胞苷联合治疗83例初诊成人患者,有效率为87%,但94.0%发生3~4级中性粒细胞减少,近半数发生发热性中性粒细胞减少。
北京协和医院开展一项2期、前瞻性、单中心研究,旨在评估小剂量阿糖胞苷方案在初诊MS或SS-M LCH成人患者中的疗效和安全性。研究结果近日发表于《Leukemia》,通讯作者为曹欣欣教授。

研究方法
该2期、单中心、单臂研究纳入年龄≥18岁LCH患者,具体标准包括:(1) 根据WHO分类标准组织学诊断为LCH,由两名独立的病理学家确诊;(2) 新诊断或既往未接受过 LCH 全身治疗(允许既往单纯放疗);(3)MS 或SS-M LCH(排除单系统肺LCH)。
给予小剂量阿糖胞苷皮下注射,剂量为100 mg/m2体表面积,1次/d,连续5d,35d/周期,共12个周期。支持治疗包括抗生素、血小板输注和必要时的粒细胞集落刺激因子(G-CSF)预防。肺部受累患者要求戒烟。
在阿糖胞苷治疗第6和12个周期后进行临床评估、体格检查和影像学检查(FDG-PET、胸腹部CT和MRI),之后每6个月进行1次疾病评估。根据《实体瘤PET疗效标准》(PERCIST 1.0)评估疾病缓解,根据实体瘤疗效评价标准1.1 (RECIST 1.1),结合临床体征、体格检查和实验室检查,对PET无法评估的患者进行评估。
从43例患者福尔马林固定和石蜡包埋(FFPE)保存的病灶活检样本中提取DNA,并对183个基因进行二代测序(NGS)
主要终点为无事件生存期(EFS),次要终点包括对阿糖胞苷的ORR(部分缓解[PR]+完全缓解[CR])、毒性和总生存期(OS)。
研究结果
患者特征
共纳入61例患者,基线特征见表1,包括男性38例(62.3%)。年龄18~66岁,中位年龄33岁。从出现症状到确诊的中位时间为4个月(1~237个月)。研究开始时包括SS-M型骨LCH 15例(24.6%)和MS型46例(75.4%)。中位受累器官数为2(1~7)个,最常见的受累器官为骨骼(75.4%),其次为肺(45.9%)、垂体(37.7%)、淋巴结(21.3%)、肝脏(19.7%)、甲状腺(13.1%)、皮肤(9.8%)、下丘脑(3.3%)、腮腺(3.3%)、脾脏(3.3%)和胃肠道(3.3%);所有患者均无造血系统受累。12例(19.7%)肝脏受累患者定义为存在危险器官受累,其中2例合并脾脏受累。注:危险器官及其受累定义为:肝脏,肋缘下肿大>3cm 和/或高胆红素血症和/或GGT水平升高和/或ALP水平升高和/或FDG(PET);脾脏,肋缘下肿大>2cm 和/或FDG摄取(PET);造血系统,活检证实骨髓受累伴贫血(血红蛋白<100g/L)和/或白细胞减少(白细胞计数<4.0X109/L)和/或血小板减少(血小板<100 X109/L)。
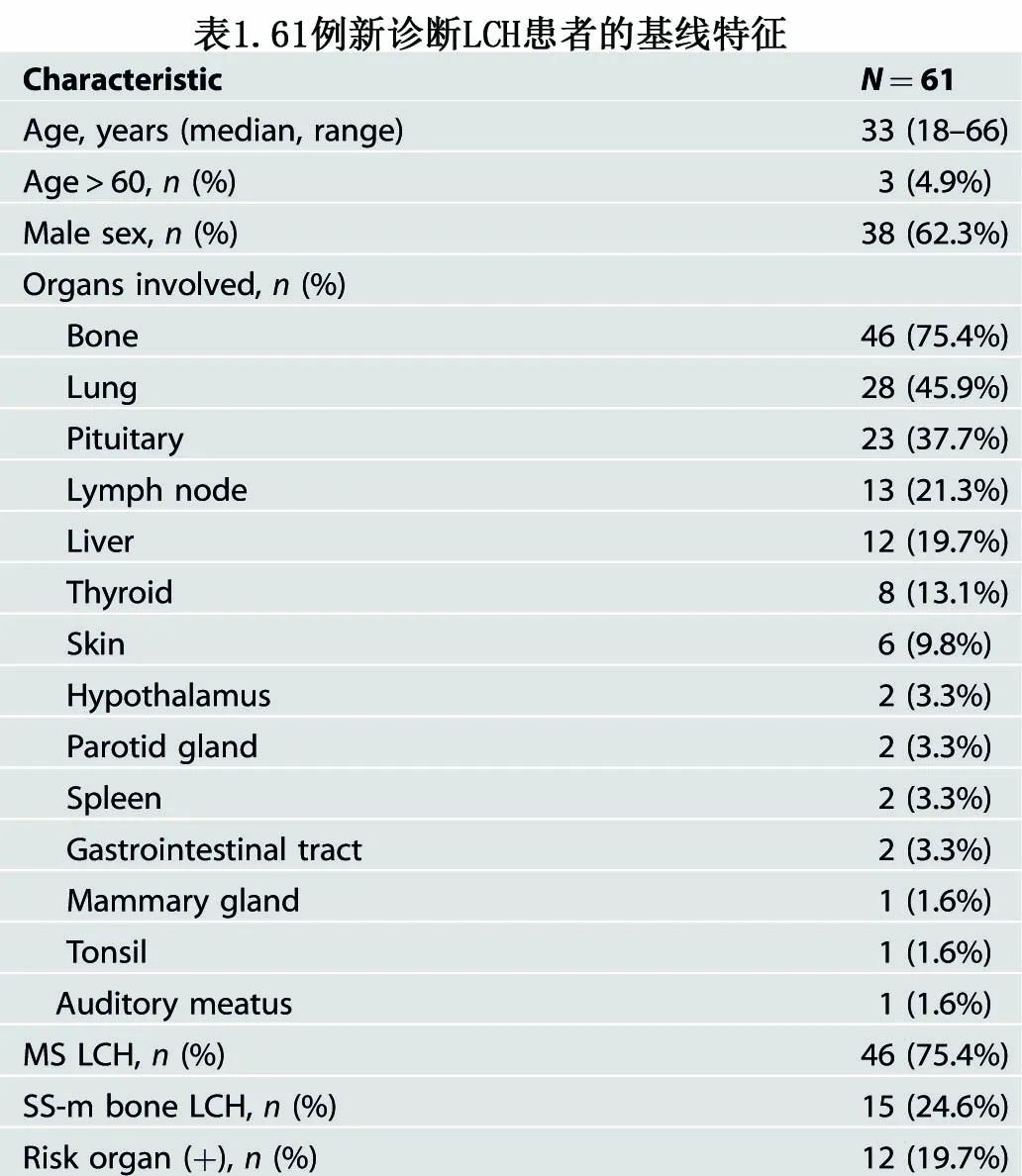
基因组分析
在43例接受NGS检测的患者中,37例(86.0%)共检测到97个单核苷酸变异、插入和缺失,候选基因的体细胞突变中位数为每例患者2个(0~8个)。29例患者存在多基因改变,其中11例患者存在≥3个改变,最常见的是BRAFV600E(25.6%)和BRAF缺失(18.6%),其次为TP53(16.3%)、MAP2K1(14.0%)和IDH2(11.6%)。28例(65.1%)患者存在MAPK通路改变。BRAF基因缺失在MS患者中的发生率趋向于高于SS-M患者(25.0% vs 0%,p=0.066)。患者的详细基因谱如图1所示。
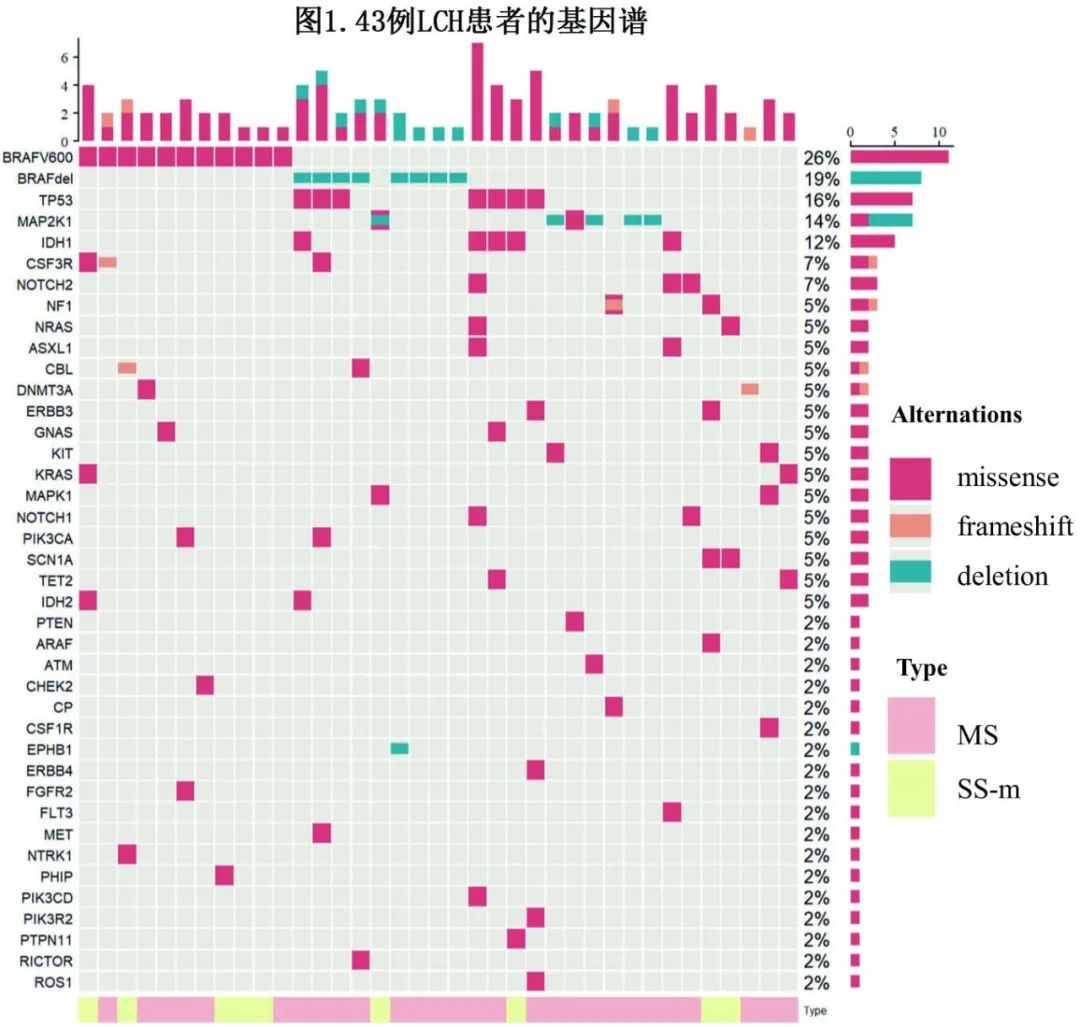
治疗和生存结局
所有患者均接受至少6个疗程的阿糖胞苷治疗,中位疗程数为12(6~12)个,47例患者(77.0%)完成完整的方案治疗,14例患者(23.0%)因患者决策(n=8)和反应不良(n=6)而退出方案,如图2中的患者流程图所示。
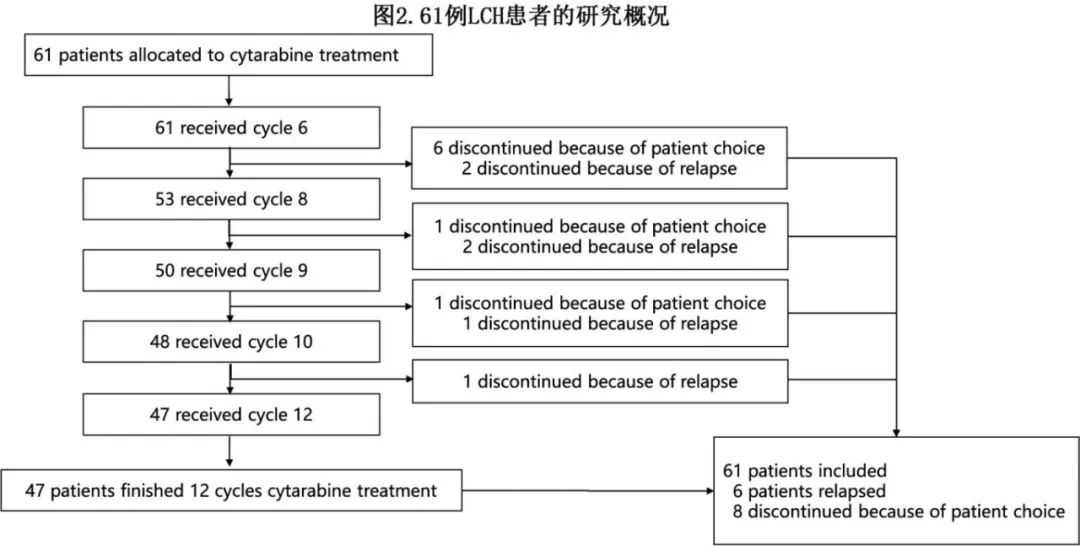
ORR为93.4%,CR 20例(32.8%),PR 37例(60.7%),疾病稳定(SD) 1例(1.6%),疾病进展(PD) 3例(4.9%);1例SD患者和2例PR患者随着治疗周期的继续而出现疾病进展。12例危险器官受累患者经阿糖胞苷治疗后,5例(41.7%)达CR, 6例(50.0%)达PR, 1例(8.3%)为PD;在有或无危险器官或CNS受累的患者之间,ORR无统计学差异。BRAF突变型和野生型患者的ORR分别为89.5%(17/19)和100.0%(24/24),TP53突变型与野生型的ORR分别为7/7(100.0%)和33/36(91.7%)。
中位随访30个月(13~46个月),21例(34.4%)患者出现疾病再激活,但无死亡病例。在复发病例中,19/21(90.5%)仅累及单个既往受累器官,包括骨7例、肝4例、外耳道2例、皮肤2例、淋巴结2例、肺1例和口腔1例;余2例出现多系统激活。CR组和PR组的再激活率分别为15.0%(3/20)和37.8%(14/37)。复发后治疗包括沙利度胺为主治疗(7例),靶向治疗(7例),大剂量甲氨蝶呤为主治疗(5例),观察(2例)。预计3年OS和EFS分别为100.0%和58.5%(图3A)。未见中枢神经系统变性表现。
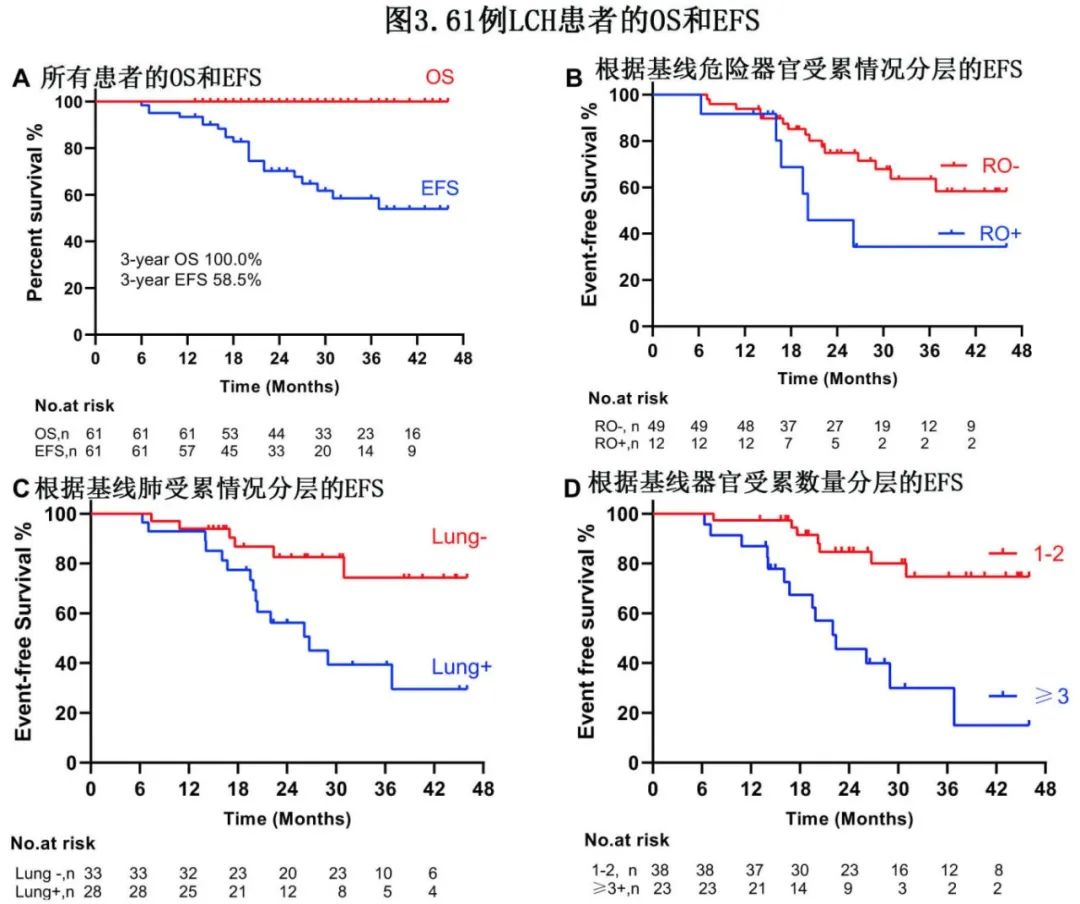
对EFS相关预后因素进行的单因素分析显示,基线时有危险器官受累的患者比无危险器官受累的患者EFS更差(20.2个月 vs 未达到,P=0.064)(图3B)。基线时有肺部受累的患者与无肺部病变的患者相比EFS也降低(26.7个月 vs 未达到,P=0.020)(图3C)。受累器官数≥3个的患者EFS明显低于1~2个的患者(22.4个月 vs未达到,P<0.001)(图3D)。
SS-M型患者EFS优于MS型患者(未达到vs 31.0个月,P=0.038)。基线时骨、皮肤、垂体、淋巴结、甲状腺受累患者EFS差异均无统计学意义。此外,BRAFV600E、MAP2K1或TP53异常患者之间无显著的EFS差异。
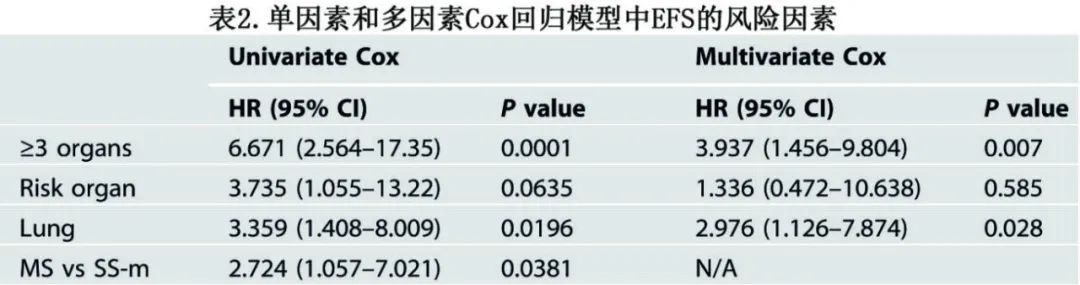
在以受累器官数、肺部受累、危险器官受累为协变量的多因素Cox回归模型中,受累器官≥3个的患者(HR=3.937;P=0.007)和肺部受累患者(HR=2.976;P=0.028)的EFS显著较低(表2)。
不良反应
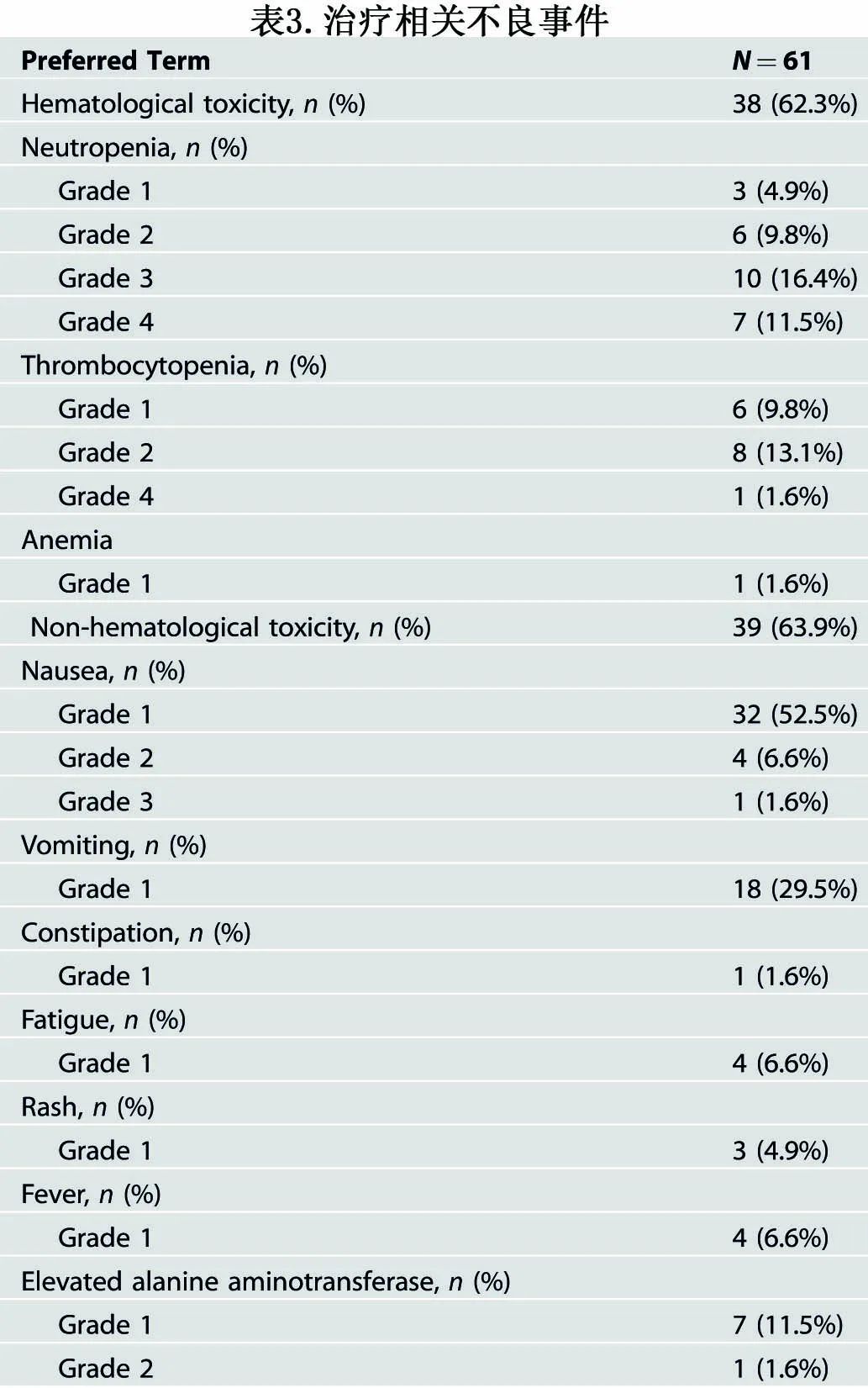
最常见的治疗相关不良反应为血液学不良事件和胃肠道并发症。38例(62.3%)患者发生中性粒细胞或血小板减少,其中4级中性粒细胞减少7例(11.5%),3级中性粒细胞减少10例(16.4%),仅1例(1.6%)患者出现4级血小板减少。在治疗周期中,没有患者接受预防性抗微生物药物治疗或输血。未发生发热性中性粒细胞减少。最常见的非血液学不良反应为胃肠道反应,包括恶心37例(60.7%,其中3级恶心1例)、呕吐18例(29.5%)和便秘1例(1.6%)。通过支持性治疗,所有胃肠道毒性均得到成功控制。7例(11.5%)患者发生1~2级丙氨酸转氨酶升高,均完全缓解。3例(4.9%)出现1级乏力,3例(4.9%)出现1级皮疹,3例(4.9%)出现1级发热。未观察到治疗相关死亡。没有患者因不良反应而停止研究治疗。开始阿糖胞苷治疗后的不良事件总结见表3。随访期间未发现继发性原发恶性肿瘤。
总结
该单中心、2期前瞻性研究纳入61例新诊断的多系统或多灶单系统LCH患者。皮下注射阿糖胞苷(100 mg/m2,5d), 35d/周期,共12个周期。患者年龄18 ~ 66岁,中位年龄33岁。12例(19.7%)患者基线存在肝脏受累,其中2例合并脾脏受累。在43例接受NGS的患者中,BRAF改变(44.2%)最常见,其次为TP53(16.3%)、MAP2K1(14.0%)和IDH2(11.6%);28例(65.1%)患者发生MAPK通路改变。结果ORR为93.4%,其中CR 20例(32.7%),PR 37例(60.7%)。中位随访30个月,21例(34.4%)复发,无患者死亡;预计3年OS和EFS分别为100.0%和58.5%。多因素分析发现受累器官≥3个(HR=3.937;P=0.007)和基线肺部受累(HR=2.976;P=0.028)是EFS的不良预后因素。最常见的3~4级毒性为中性粒细胞减少(27.9%)、血小板减少(1.6%)和恶心(1.6%)。
总的来说,12个月阿糖胞苷单药治疗新诊断成人LCH患者具有良好的疗效和安全性,但基线肺部受累或≥3个器官受累提示接受阿糖胞苷单药治疗的预后较差。
参考文献
hang, L., Lang, M., Lin, H. et al. Phase 2 study using low dose cytarabine for adult patients with newly diagnosed Langerhans cell histiocytosis. Leukemia (2024). https://doi.org/10.1038/s41375-024-02174-1
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#阿糖胞苷# #朗格汉斯细胞组织细胞增生症#
24