深度解析:瑞德西韦用于新冠肺炎的临床试验详情
2020-02-06 MedSci MedSci
2月5日下午,北京中日友好医院王辰、曹彬团队在武汉市金银潭医院宣布启动瑞德西韦(remdesivir)治疗2019新型冠状病毒感染研究。目前在Clinicaltrials上能查询到remdesivir针对轻中度新冠肺炎的研究。研究试验的名称:A Phase 3 Randomized, Double-blind, Placebo-controlled Multicenter Study to Eva
2月5日下午,北京中日友好医院王辰、曹彬团队在武汉市金银潭医院宣布启动瑞德西韦(remdesivir)治疗2019新型冠状病毒感染研究。目前在Clinicaltrials上能查询到remdesivir针对轻中度新冠肺炎的研究。
研究试验的名称:A Phase 3 Randomized, Double-blind, Placebo-controlled Multicenter Study to Evaluate the Efficacy and Safety of Remdesivir in Hospitalized Adult Patients With Mild and Moderate 2019-nCoV Respiratory Disease.
研究计划纳入308名患者,平行对照,对所有参与人员均进行遮蔽(包括患者,研究者,照顾者和结局评估者)。研究预计4月10日纳入最后一例,4月27日完成试验(不过结局为TTCR,即临床症状完全恢复时间。当然绝大部分患者症状应该在7-10天左右得到缓解。整个治疗周期为10天,病人整体观察周期为28天。意味着按计划最后一例入组后,治疗能完全结束,最长观察时间约为17天,不满28天)。
但是,研究有可能会比预计时间提前。因为,整体来说,研究的纳排标准不是特别严格,除掉重型与危重(主要是肝肾功能,SaO2/SPO2≤94%或Pa02/Fi02 ratio <300mgHg),轻中度中限定的是成人,起病8天以内的确诊患者,这样的患者在武汉应该相当多(当然如何定义疾病开始,可能有些争议,是核酸检测确诊算第1天,还是有发热或其它症状算第1天,则需要看研究方案的定义了)。如果入组速度加快,研究尽快结束,尽快明确结果。一旦确实发现Remdesivir效果不错的话,后面不少病人可能有望用得上这个药物了(否则如果试验4月27日结束,即使国家局加速审批,吉利德公司再进口进入国内,基本要到6月份了,疫情应该已结束了)。
用药采用第一天为负荷剂量,即200mg/d,后续9天为100mg/d剂量给予。
网传开始设计时样本为270例是真是假?实际上,从Clinicaltrials上记录来看,是真实的。在1月31日的最初设计时确实为270例,后经统计样本量重新计算为308例。主要研究终点也从Rate of composite advers outcomes更改为TTCR。部分内容与昨天推测的相符:刚刚,瑞德西韦临床试验在武汉金银潭医院启动!确实轻中度与重症是两个独立的试验。
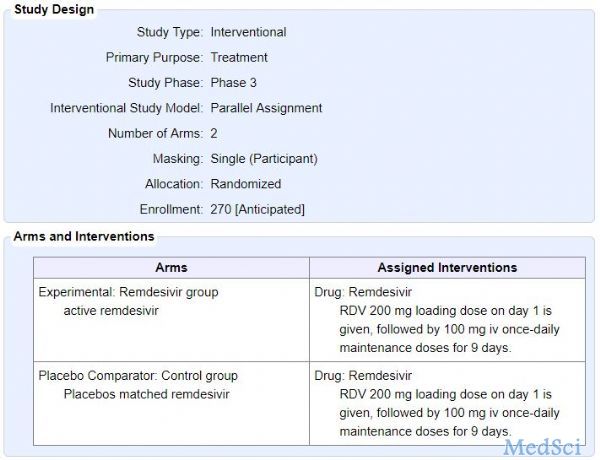
当然,两组患者是否是1:1还是2:1暂时不知道,其实如果能设计为2:1或3:1,也许对患者更为有利。
另外,这个研究设计是相当苛刻的,在整个治疗期间,研究者是不知道是药物还是安慰剂,那么安慰剂组患者即使无效(且试验药物很有效的前提下)。
今天有些媒体开始关注患者治疗效果了,其实这是很困难的。其一,这是盲法设计,并不知道是药物还是安慰剂(当然,如果药物疗效十分理想的话,也很容易鉴别出药物还是安慰剂,因为安慰剂虽然也有一定的效应,但是整体效应还是有限的。如果对于重症的试验而言,安慰剂效应很轻微,这时候更容易“判断”出是试验药物还是安慰剂。),其二,药物需要使用10天,第一例治疗都没有结束,因此,很难判断是否有效。其三,整个研究数据需要到研究结束后才能揭盲,那么现在就是有效,也不清楚是安慰剂还是试验药物(除非对于重症人,安慰剂效应不可能很大的时候,而且许多患者用药后快速好转,这时候数据管理委员会,可以考虑提前中止试验,因为可以推断治疗效应很有可能来自于试验药物组)。
因此,有关瑞德西韦真正的作用,还需要静静等待。
此前,国家药监局已经同意中日友好医院和中国医学科学院可以在感染新型冠状病毒的患者中开展临床试验。
另外,最近几天,还会观察对于重症的另一项研究,纳入重症患者453例,整个研究设计可能与目前研究有较大差别。
相关研究报道:
新型冠状病毒肺炎综合工具:自我诊断,科普知识,实时动态,趋势,辟谣
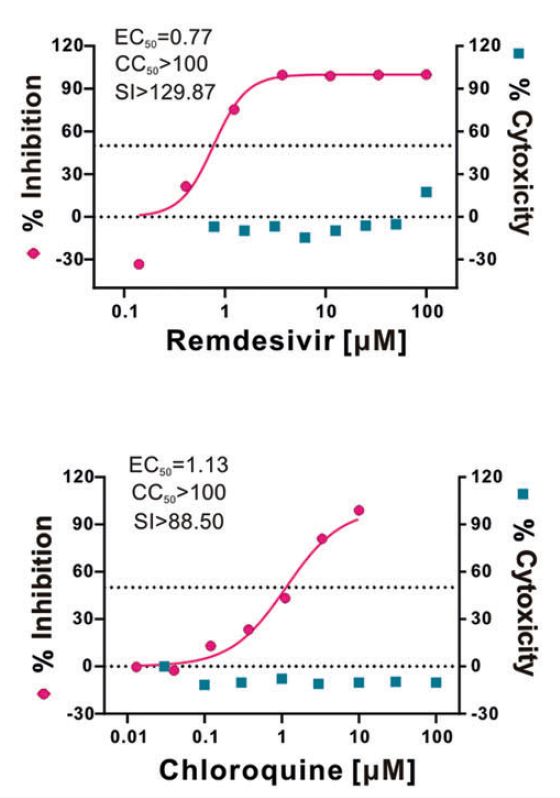
Cell Res:瑞德西韦和磷酸氯喹能在体外有效抑制新型冠状病毒(2019-nCoV))
Remdesivir(瑞德西韦)的临床试验昨日并未入组200例患者
NEJM和Science齐发文,这种药物可能是治疗新冠病毒最好的选择
新冠肺炎药物Remdesivir(瑞德西韦)在2020年2月3日在中国开始临床试验,中日友好医院牵头
美国“神药”Remdesivir轻松搞定新型冠状病毒肺炎,到底是什么来头?
NEJM:美国首例新型冠状病毒感染者使用新型抗病毒药物后退烧,病情好转
抗击2019-nCoV:实验性埃博拉药物Remdesivir或具有抗新型冠状病毒的潜力
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#解析#
32
新冠肺炎,疫情何时才能消失
49