欧洲药品管理局(EMA)授予ARU-1801治疗镰状细胞病的优先药品资格(PRIME)
2021-02-04 Allan MedSci原创
ARU-1801是一种针对镰状细胞疾病的研究性基因疗法。
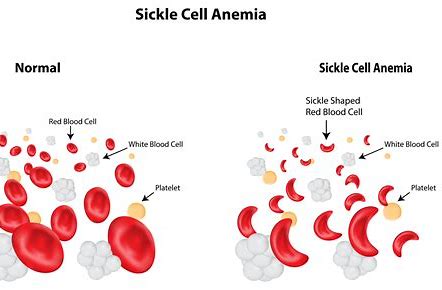
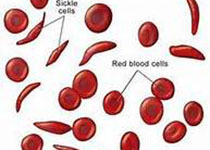
镰状血红蛋白的产生是由β珠蛋白基因的镰状点突变所致,这种血红蛋白的溶解性较正常的胎儿或成人血红蛋白差。镰状细胞病(SCD)几乎仅见于黑人。大约 10% 的美国黑人有一个镰状细胞病基因(也就是说他们有镰状细胞性状)。有镰状细胞性状者并不一定会发生镰状细胞病,但他们出现尿血等某些并发症的风险的确会增大。约 0.3% 的黑人携带两个基因。

生物制药公司Aruvant Sciences今天宣布,欧洲药品管理局(EMA)向ARU-1801授予治疗镰状细胞病的优先药品资格(PRIME)。ARU-1801是一种针对镰状细胞疾病的研究性基因疗法。
Aruvant首席执行官Will Chou博士表示:“PRIME凸显了镰状细胞疾病的医疗需求。有了PRIME,我们能够与EMA紧密合作以开发ARU-1801,我们的目的是将这种潜在的治疗方法迅速地带给欧洲SCD患者”。
根据I/II期临床试验(MOMENTUM研究)的临床数据,ARU-1801治疗严重镰状细胞疾病,能够持久地减轻疾病负担。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#镰状细胞病#
53
#药品管理#
32
#EMA#
33
#欧洲#
24
#欧洲药品管理局#
29
#镰状细胞#
35
涨知识
69
嘻嘻,学习了
79