2022年FDA有望批准的18款创新疗法
2022-01-16 药智网 药智网
近日,FDA发布2021年药物审评审批报告,获批50种新药,低于2020年53种,包括具有里程碑意义的mRNA疫苗与两款CAR-T细胞疗法、多款ACD新药、颇具有争议的阿兹海默症Aduhelm....
近日,FDA发布2021年药物审评审批报告,获批50种新药,低于2020年53种,包括具有里程碑意义的mRNA疫苗与两款CAR-T细胞疗法、多款ACD新药、颇具有争议的阿兹海默症Aduhelm.....新药研发,医药创新又上了一个新的台阶。
此外,还有多款火爆行业圈的明星药物因显著疗效获指定的突破性疗法、优先审评审批资格等。据《Nature》期刊报告统计,值得关注的有望2022年获批上市18款重磅药物,其中近半数为指定的突破性疗法,以及在未来5年里能产生大量销售额的药物,包括2款治疗阿尔兹海默症的单抗,2型糖尿病的GIP/GLP-1双靶点激动剂以及治疗hATTR的RNAi疗法等。
2022年值得关注的批准药物一览
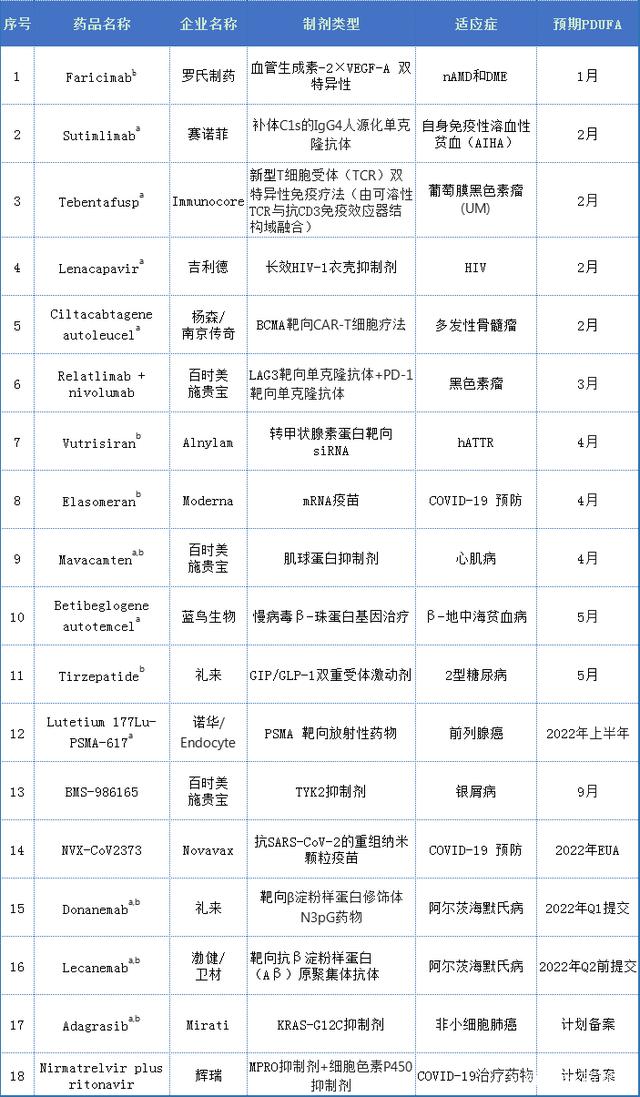
注:a.指定的突破性疗法。b根据 Cortellis 数据库,预测到 2027 年销量大涨的药物。
BMS 3+礼来2,2022年最大创新收获者
从企业角度而言,百时美施贵宝2022年或将是最大赢家,有三款药品重磅新药即将上市,分别是Relatlimab + nivolumab组合疗法、Mavacamten、以及BMS-986165。其次是礼来有2款,一款有望成为新的糖尿病王者药物Tirzepatide和一款阿尔茨海默病新药Donanemab。
Relatlimab + nivolumab 新型LAG-3+PD-1双重阻断疗法
Relatlimab和nivolumab(纳武利尤单抗)皆由百时美施贵宝(BMS)开发,为一种新型LAG-3+PD-1双重阻断疗法,临床研究显示relatlimab 和nivolumab的固定剂量使用,与单独使用O药相比,无进展生存期(PFS)基本上翻倍,临床试验研究数据显示组合疗法中位无进展生存期从4.6个月延长到10.1个月,1年无进展生存率从36.0%提高到47.7%。
目前,FDA已经受理relatlimab+nivolumab固定剂量复方组合的上市申请,PDUFA预定审批期限是2022年3月19日。
Mavacamten,first-in-class心肌病新药
Mavacamten由MyoKardia发现、开发,是首个(first-in-class)、口服、心脏特异性肌球蛋白 (cardiac myosin) 结构抑制剂。2020年10月百时美施贵宝以131亿美元收购MyoKardia获得,目前该药已经获得了FDA授予的突破性疗法资格,原定于2022年1月获批,2021年11月FDA将其审查期限延长了3个月,最新的PDUFA日期为2022年4月28日。
值得提及的是Mavacamten在EvaluatePharma的最大潜力新药上市名单中排名第三。公开数据显示,美国潜在患有梗阻性HCM人群高达20万人,由于在这领域中竞争对手稀缺,有机构预测mavacamten在2026年的全球销售额将达到20亿美元。联拓生物拥有其核心药物Mavacamten中国区权益。
BMS-986165 全球首款上市的TYK2抑制剂
Deucvacitinib(BMS-986165)是百时美施贵宝公司开发的Tyk2 JH2结构域抑制剂,尽管该药在溃疡性结肠炎(IBD)中期试验未能达到主要或次要终点,但在第3阶段银屑病试验中战胜了Otezla。
现阶段,美国食品和药物管理局(FDA)、欧洲药品管理局(EMA)以及日本厚生劳动省均已受理了Deucravacitinib的上市许可申请。Deucravacitinib有望成为全球首款上市的TYK2抑制剂。
Tirzepatide 糖尿病领域新王者
tirzepatide是由礼来开发的一种新型每周一次首个葡萄糖依赖性促胰岛素多肽(GIP)和胰高血糖素样肽-1(GLP-1)的双受体激动剂。2021年10月26日,礼来宣布已经向美国FDA和欧盟EMA提交了tirzepatide的新药上市申请,并获FDA优先审评,有望于2022年5月快速获批上市。
Tirzepatide是礼来继度拉糖肽,糖尿病市场又一张王牌。此外,Tirzepatide以 187 亿美元的净现值位居Evaluate Pharma 发布的更有价值 TOP10第一,妥妥的糖尿病领域新王者。
Donanemab 终点冲刺
礼来公司开发的靶向 β- 淀粉样蛋白(Aβ)单克隆抗体,2021年6月24日,礼来宣布Donanemab获得FDA的突破疗法认定,2021年12月,礼来宣称将于2022完成FDA BLA滚动提交,以期获得针对早期阿尔茨海默病的加速批准,有望于2022年冲向终点。
值得注意的是Donanemab的二期临床虽然达到主要终点,但次要终点均未达到。不过有渤健Aducanumab获批在前,Donanemab的获批预期也有所增强。
多个第一,引领first-in-class新浪潮
从上文可看出,无论是BMS还是礼来,first-in-class药物是2022年主旋律。事实,除此之外,罗氏、赛诺菲、吉利德……也冲线在first-in-class前沿,各自又有重磅炸弹药即将面世。
Faricimab,下一个获批的双特异抗体
Faricimab为罗氏开发的一款专门为眼睛设计的、同时靶向VEGF和Ang2的双特异性抗体,该候选药可在抑制VEGF活性的同时,还可通过抑制Ang2活性来改善血管稳定性,降低视网膜炎症。其于2021年7月末获FDA生物制品许可申请(BLA)以及获优先审评资格,有望今年1月获批,成为第一个也是唯一一个旨在靶向驱动视网膜疾病的2个独特信号通路的药物。或将接替“Avastin”药物成为罗氏制药新“三驾马车”之一的药物,拉动罗氏制药经济效益。
Sutimlimab,改变CAD治疗模式
Sutimlimab是赛诺菲于2018年花费116亿美元收购Bioverativ时获得的一款抗补体C1s的IgG4人源化单克隆抗体药物,主要用于CAD等补体途径介导的疾病治疗。
值得注意的是,2020年11月14日,FDA称其负责制造的第三方设施进行批准前检查(PLI)时发现了某些缺陷,拒绝了Sutimlimab上市申请。目前赛诺菲正在解决这类问题,且2022年5月,FDA已受理其用于CAD成人患者治疗溶血的BLA申请,并授予了优先审查资格。
此外,FDA此前已授予Sutimlimab突破性药物资格和孤儿药资格,欧盟EMA也已授予孤儿药资格。有望于2022年2月获批上市,成为第一个也是唯一一个治疗CAD溶血的药物,或将改变CAD的治疗模式。
Tebentafusp,40年来新突破
Tebentafusp是由Immunocore公司研发的一种新型双特异性蛋白,由可溶性TCR与抗CD3免疫效应器结构域融合而成。被专门设计成靶向gp100。2021年8月末,其治疗HLA-A * 02:01基因阳性、转移性葡萄膜黑色素瘤 (mUM)成人患者的监管申请,获FDA和EMA受理,同时FDA授予其优先审评资格,PDUFA日期为2022 年 2 月 23 日;此前还给予其治疗葡萄膜黑色素瘤的孤儿药资格以及突破性疗法资格。而欧盟EMA也将在加速评估程序中对Tebentafusp的MAA进行评估。如若获批,有望成为40年来治疗mUM方面第一个显著改善总生存期(OS)的新疗法。
lenacapavir,第一个衣壳抑制剂
Lenacapavir是吉利德开发的一种潜在的“first-in-class”长效HIV-1衣壳抑制剂,用于治疗HIV-1感染,且与目前批准的任何抗逆转录病毒疗法(ART)没有重叠耐药性。
2019年5月,FDA授予lenacapavir突破性治疗;2021年6月向FDA提交新药申请,目前正在审查中,上市可期。不过好事多磨,在2021年12月末,lenacapavir因“颗粒问题”FDA对lenacapavir的10项研究进行了临床搁置,不过吉利德正在与时间赛跑,全力解决问题,使lenacapavir计划快速回归正轨。仍有望今年获批,成为第一个衣壳抑制剂,也是唯一一个每年给药2次(每6个月给药一次)的HIV-1治疗方案。
Ciltacabtagene autoleucel,中国首个突破性治疗品种
Ciltacabtagene autoleucel(cilta-cel)是南京传奇生物和杨森(Janssen)公司合作开发研发的一种基因编辑的自体CAR-T细胞疗法,靶向作用于癌细胞表面的B细胞成熟抗原,用于治疗成人复发或难治性多发性骨髓瘤(RRMM)。
此前,FDA授予cilta-cel突破性疗法和孤儿药称号,以及欧洲药品管理局授予的孤儿药和优先药物(PRIME)称号以及加速审评。值得提及的其是首个获得FDA批准临床试验的中国自主研发的细胞疗法,也是中国首个突破性治疗品种。
FDA原计划定于2021年11月29日批准cilta-cel药上市,不过后因要求审查关于“更新的分析方法”的其他信息,FDA决定延长至2022年2月28日。如若顺利获批,该药物将成为在美国上市销售的第二种靶向BCMA的CAR-T细胞疗法。
Betibeglogene autotemcel,全球第一款针对TDT的基因疗法
betibeglogene autotemcel(beti-cel)是蓝鸟生物的一款使用BB305慢病毒载体(LVV)制造的一次性基因疗法,同时是蓝鸟生物的首个基因疗法,也是全球第一款针对TDT的基因治疗产品。用于所有基因型的成人、青少年和儿童输血依赖型β-地中海贫血(TDT)患者。
2019年6月初,beti-cel被欧盟委员会(EC)有条件批准,用于治疗12岁及以上的非β0/β0基因型输血依赖性β-地中海贫血患者,然而由于数据和制造问题被EMA推迟到2020年1月,才在德国首次商用,商品名为Zynteglo。
2021年9月21日,蓝鸟公司(bluebird bio)宣布已完成该产品在FDA的滚动提交生物制剂许可申请(BLA)。此前,FDA此前授予了beti-cel孤儿药和突破性疗法认定。若此次获批,beti-cel将成为美国首个造血(血液)干细胞(HSC)体外基因疗法。
又有两款新冠疫苗将粉墨登场,辉瑞Paxlovid全面获批?
值得提及的是,在新冠疫情全球持续弥漫的当下,无论是有效预防,还是能针对疫情起到疗效的新药,是全世界目前最紧缺与必需的药物。尽管目前全球已有多款新冠疫苗获批,2022年仍有两款值得期待的2款新冠疫苗获批,以及辉瑞Paxlovid的全面获批。
Elasomeran,销售额将超170亿美元
Elasomeran(Spikevax)是由Moderna开发的针对新型冠状病毒SARS-CoV-2的一款mRNA疫苗(mRNA-1273/TAK-919),经肌肉注射给药。早在2020年12月获得了COVID-19的欧盟许可,预计到2022年4月将获得美国FDA的全面批准。
此外,近日公布了mRNA新冠疫苗对奥密克戎变异株中和抗体数据,与未接种加强针相比,目前批准的50g mRNA-1273加强针接种将Omicron(奥密克戎)的中和抗体水平提高了约37倍,100g剂量加强针接种将中和抗体水平提高了约83倍。分析师预测2021年elasomeran的销售额将超过170亿美元。
NVX-CoV2373,新型新冠疫苗
NVX-CoV2373是Novavax公司研发的一种基于蛋白质的疫苗,根据SARS-CoV-2(新冠肺炎致病病毒)首个毒株的基因序列改造而成。2021年12月22日欧洲药品管理局(EMA)已建议授予Novavax的NVX-CoV2373有条件上市许可,用于18岁及以上人群预防新冠肺炎。 目前尚未获准在美国使用,不过有望于2022年会批EUA。
Evaluate预测,Novavax 的COVID-19疫苗的销售额在2021年将达到23.7亿美元,2026年销售额将达到27.3亿美元。
Paxlovid新冠口服药,辉瑞将获全面批准?
Paxlovid是3CL蛋白酶抑制剂nirmatrelvir与低剂量利托那韦(Ritonavir)的复方制剂。2021年圣诞前夕通过FDA紧急授权使用,用于治疗非住院、具有发展成重症疾病高风险成人COVID-19感染。
不过仅仅获批用于新冠感染高风险患者是远远不够的。此前,FDA已建议将该药物用于治疗12岁及以上患有轻度至中度症状且疾病恶化风险高的Covid阳性患者。或于2022年获批,给予更多新冠肺炎患者生命健康福利的同时,拓宽适应症,拓展市场。
有分析师预测辉瑞新冠药物Paxlovid 2022年预计能达242亿美元,销售额仅次于其新冠疫苗,排名第二。
其它新药批准
除首创新药和孤儿药认定药品外,2022年新药领域还包括以下值得关注几款即将获批的新药。
Vutrisiranb,第5款RNAi疗法
Vutrisiranb为Alnylam公司开发的一款皮下注射RNA干扰(RNAi)疗法,用于治疗成人遗传性转甲状腺素蛋白介导(hATTR)淀粉样变性的多发性神经病。2021年6月FDA接受该vutrisiran新药上市申请,并给予优先审评,《处方药用户收费法》(PDUFA)目标日期为2022年4月14日。
此外,此前在美国和欧盟,vutrisiran均被授予了治疗ATTR淀粉样变性的孤儿药资格(ODD),如果获得批准,这将是多年来第5个RNAi批准,Alnylam第四款获得FDA批准RNAi疗法。
Lecanemab,卫材和渤健又一款AD药物
Lecanemab是卫材和渤健合作研发一种拟用于治疗AD的人源化单克隆抗体。2021年6月获FDA突破性疗法认定,2021年9月,卫材开始根据加速批准通道向FDA滚动提交lecanemab的生物制剂许可申请(BLA),2021年12月获FDA快速通道资格。
值得一提的是颇受争议的Aducanumab同样为卫材和渤健共同开发的产品。有此产品在前,lecanemab能否顺利获批拭目以待。
Adagrasib,第二款重磅的KRAS抑制剂
Adagrasib(MRTX849)是Mirati公司开发的一款针对KRAS G12C突变体的特异性优化口服抑制剂。公开资料显示,2021年6月,Adagrasib获FDA突破性认证,目前其正在筹备其NSCLC适应症的上市申请,有望于2022 年获得批准。一旦获批,将是继Sotorasib后的第二款重磅KRAS抑制剂。
另据EvaluatePharma预计2026年adagrasib的销售额为17.4亿美元。目前国内再鼎医药已引进adagrasib在大中华区的权益。
参考来源:
1.2021 FDA approvals:https://www.nature.com/articles/d41573-022-00001-9
2.各企业公告、官网、生物谷、识林、新浪医药等公开信息
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言




.jpg)




学习了
63
学到只是个
0
#创新#
0
#新疗法#
58
学习
69