JCO:Dara-Rd治疗RRMM的POLLUX研究80个月随访,进一步证实生存获益
2023-01-18 聊聊血液 聊聊血液 发表于上海
在新诊断多发性骨髓瘤 (NDMM) 和复发/难治性多发性骨髓瘤 (RRMM) 患者中开展的多项 III 期研究证实,达雷妥尤单抗联合标准治疗 (SOC) 方案可显著降低疾病进展或死亡风险,并获得深度且
POLLUX研究
在新诊断多发性骨髓瘤 (NDMM) 和复发/难治性多发性骨髓瘤 (RRMM) 患者中开展的多项 III 期研究证实,达雷妥尤单抗联合标准治疗 (SOC) 方案可显著降低疾病进展或死亡风险,并获得深度且持久的缓解,包括≥CR率和微小残留病 (MRD) 阴性率显著高于SOC。
例如其重磅III 期POLLUX研究的初始分析(中位随访13.5个月)中,与来那度胺和地塞米松 (Rd) 疗相比,达雷妥尤单抗+来那度胺和地塞米松 (D-Rd) 可显著改善 RRMM 患者的无进展生存期 (PFS)(HR 0.37,P< 0.001),深度缓解率也很高(≥CR率 43.1% v 19.2%;MRD阴性率 [10-5灵敏度] 22.4% v 4.6%;P< 0.001)。在中位随访25.4个月的更新分析中,D-Rd持续改善PFS(HR 0.41;P< 0.0001),且缓解随时间而加深,≥CR和 MRD 阴性率(10-5灵敏度)分别为51.2%与21.0%(P< 0.0001)和26.2%与6.4%(P< 0.000001)。在 POLLUX 的最新分析中(中位随访54.8个月),与 Rd 单独治疗相比,D-Rd可使疾病进展或死亡风险降低56%(中位PFS45.0个月vs.17.5个月;HR 0.44;P< 0.0001),缓解持续加深且MRD阴性率更高。此外在既往接受过一线治疗的患者中,D-Rd组和Rd组的中位PFS分别为53.3和19.6个月(HR 0.42;P< 0.0001),且无论细胞遗传学风险状态如何,D-Rd的 PFS 获益均得以维持。
继去年11月报道Dara-Vd的CASTOR研究72.6个月随访结果后,近期《Journal of Clinical Oncology》报告了POLLUX研究超过6.5年随访的疗效和安全性结果更新,重点在于总生存期的改善,D-Rd和Rd分别为67.6和51.8个月。

POLLUX研究是一项多中心、随机、开放标签、阳性对照III期研究,纳入RRMM患者(排除来那度胺难治患者)进行1:1随机进入D-Rd或Rd组。所有患者均接受28天/周期的来那度胺(每个周期第1-21天口服25mg每日一次,肌酐清除率为30-60 mL/min的患者为10mg每日一次)和地塞米松(40mg每周一次)治疗,直至疾病进展、出现不可接受的毒性或死亡。对于 D-Rd 组患者,在第1周期和第2周期每周一次(第1、8、15和22天)给予达雷妥尤单抗(16mg/kg静脉给药),在第3-6周期每2周一次(第1和15天)给药,此后每4周一次。
主要终点为PFS,次要终点包括ORR、≥VGPR率和≥CR率、MRD阴性率、至缓解时间和OS。
患者
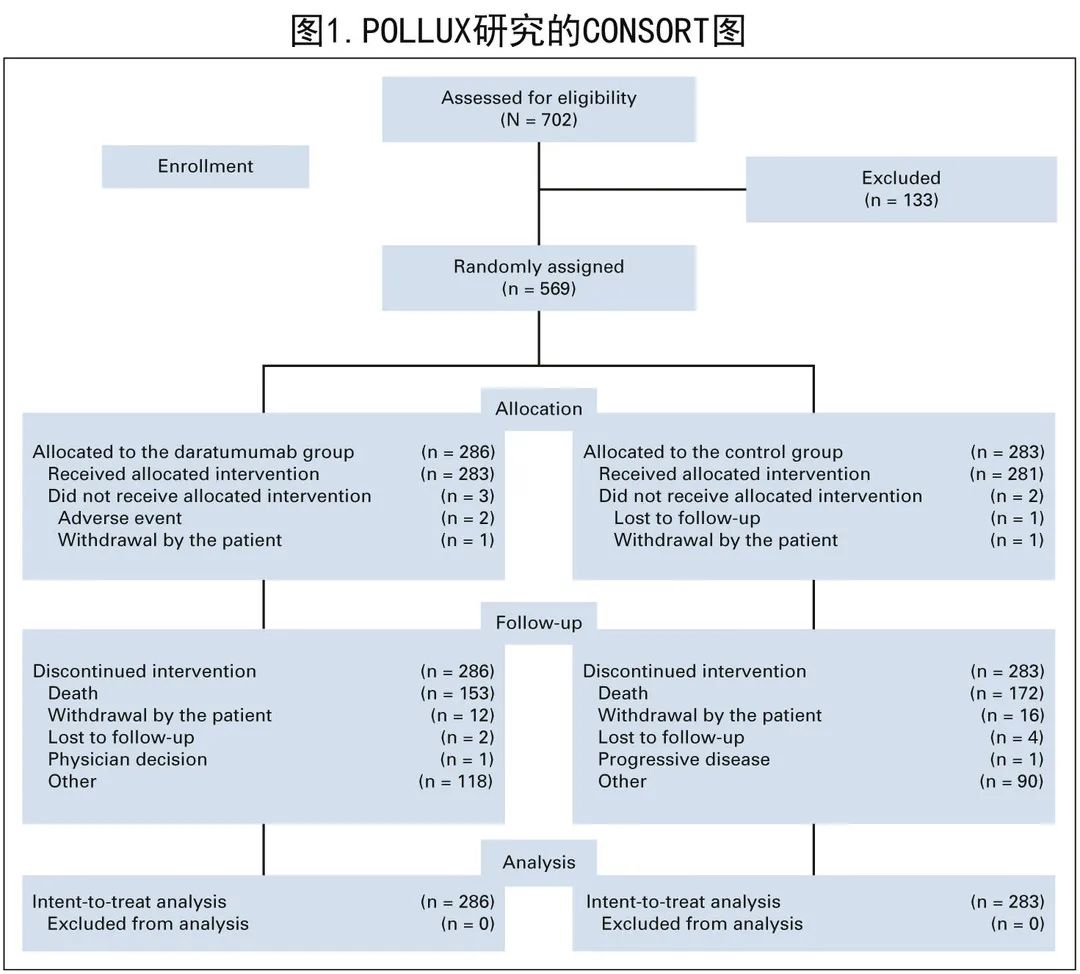
共有569例患者被随机分配接受 D-Rd (n=286) 或Rd(n=283;图1)。
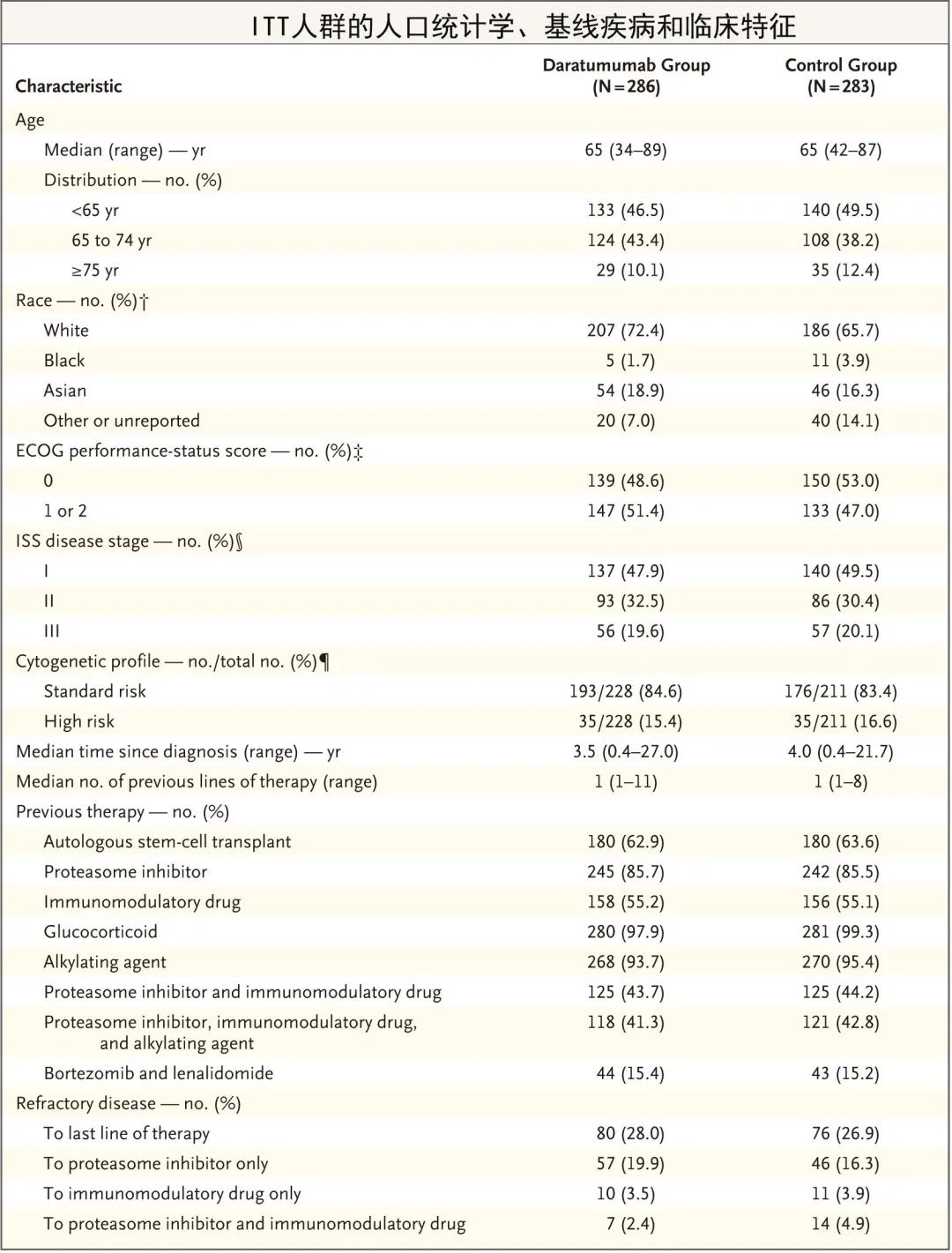
患者基线人口统计学和临床特征之前已发表,组间通常平衡良好。患者的中位年龄为65岁。约一半 (51.8%) 患者既往接受过1线治疗,84.2%既往接受过硼替佐米,17.6%既往接受过来那度胺,43.9%接受过蛋白酶体抑制剂 (PI) 和免疫调节剂,20.6%为硼替佐米难治。
D-Rd组和Rd组的中位研究治疗持续时间分别为34.3个月和16.0个月,接受的中位治疗周期总数分别为37和17。Rd 组122例接受后续治疗的患者接受了含达雷妥尤单抗治疗:根据研究方案,Rd组66例患者在疾病进展后接受后续达雷妥尤单抗单药治疗,患者接受中位7.0 个周期治疗,中位持续时间为5.8个月;另外56例患者接受达雷妥尤单抗作为研究外的后续治疗。
疗效
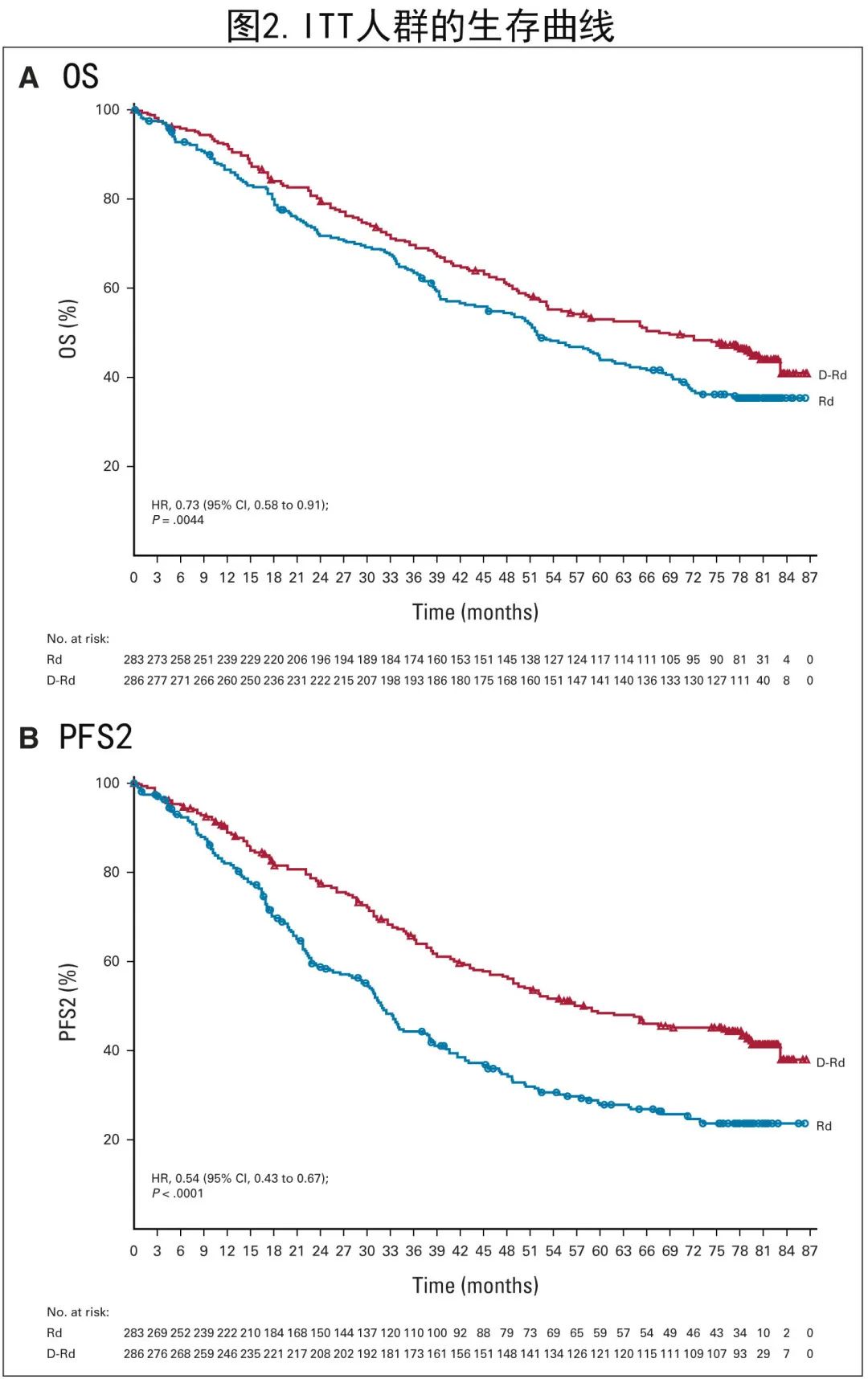
中位随访79.7个月,D-Rd组286例患者中的153例 (53.5%) 和 Rd 组283例患者中的175例 (61.8%) 死亡,死亡HR为0.73(P= 0.0044;图2A),死亡风险降低27%。D-Rd 组和 Rd 组的中位 OS 分别为67.6个月和51.8个月。D-Rd组283例患者中的127例 (44.9%) 和 Rd 组281例患者中的210例 (74.7%) 接受了后续治疗,其中Rd 组约58%(122/210例)接受后续治疗的患者接受达雷妥尤单抗治疗。与 Rd 组相比,D-Rd组至后续治疗的中位时间显著延长(69.3个月vs.23.1个月;HR 0.40;P< 0.0001),且后续治疗的 PFS 也显著延长(中位57.9个月vs. 32.0个月;HR 0.54;P< 0.0001;图2B)。
预先设定的亚组分析表明,在大多数患者亚组中D-Rd与 Rd 相比的 OS 获益均得以维持,包括年龄≥65岁的患者、既往接受过一线、二线或三线治疗的患者、ISS III期患者、高危细胞遗传学异常患者、既往暴露于 PI 的患者以及既往最后线治疗或 PI 难治的患者(图3)。对于既往接受过一线治疗的患者,D-Rd组的中位 OS 为77.8个月,而Rd组为57.7个月 (HR 0.75)。

D-Rd 组的 MRD 阴性率(10-5灵敏度阈值)显著高于 Rd 组 (33.2% v 6.7%;P< 0.0001)。且无论治疗组如何,MRD阴性均与 OS 改善相关(图4)。
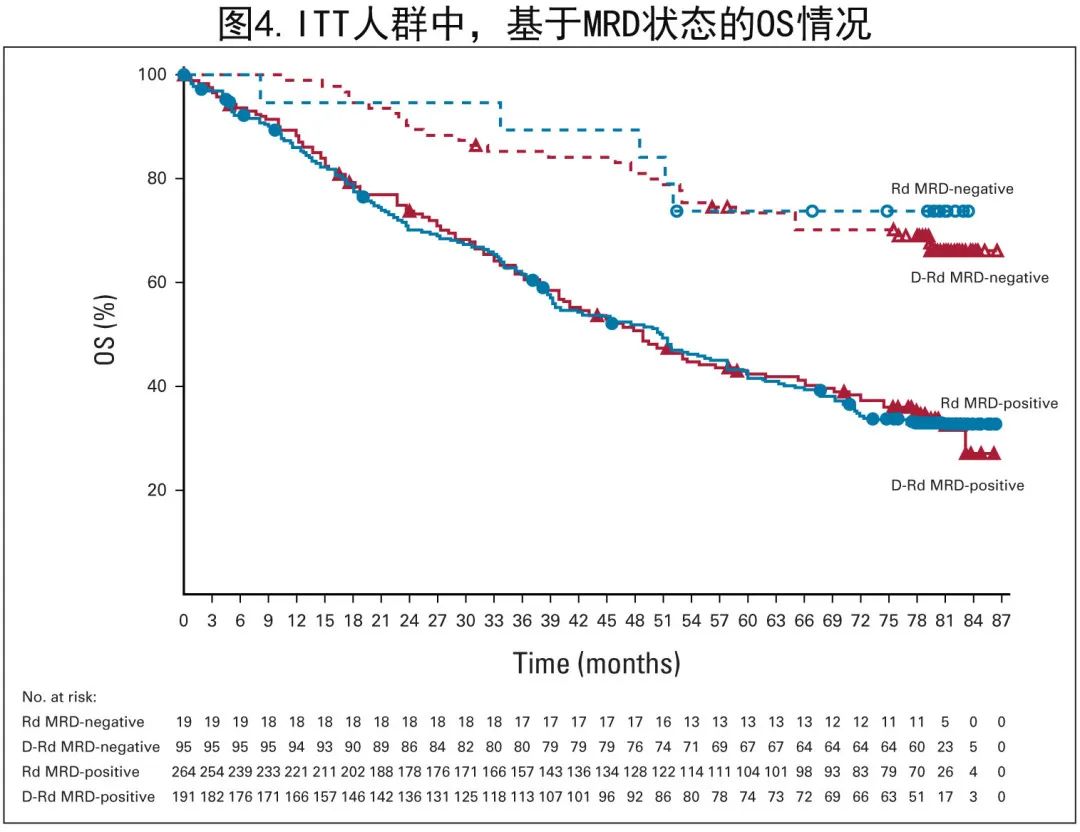
Rd 组患者在疾病进展后交叉至达雷妥尤单抗后续治疗的中位时间为28.2个月。Rd 组有66例患者在疾病进展后接受后续达雷妥尤单抗单药治疗(根据研究方案提供),其中24例 (36.4%) 患者仍存活,中位 OS 为65.6个月。
安全性
延长随访期间未报告新的安全性问题(表1)。D-Rd 组和 Rd 组中最常见 (≥10%) 3/4级治疗期间不良事件 (TEAE) 为中性粒细胞减少症 (57.6% vs. 41.6%)、贫血 (19.8% vs. 22.4%)、感染性肺炎 (17.3% vs. 11.0%)、血小板减少 (15.5% vs. 15.7%) 和腹泻 (10.2% vs. 3.9%)。D-Rd 组和 Rd 组中3/4级感染的发生率分别为44.5%和28.1%。D-Rd 组和 Rd 组分别有72.4%和52.7%的患者报告了严重TEAE,其中肺炎最为常见(分别为17.0%和11.4%)。两组间发生导致治疗终止的 TEAE 的患者比例相当(D-Rd组19.1%;Rd组16.0%)。在 D-Rd 组中,13例 (4.6%) 患者因感染停止治疗,而在 Rd 组中,11例 (3.9%) 患者因感染停止治疗。
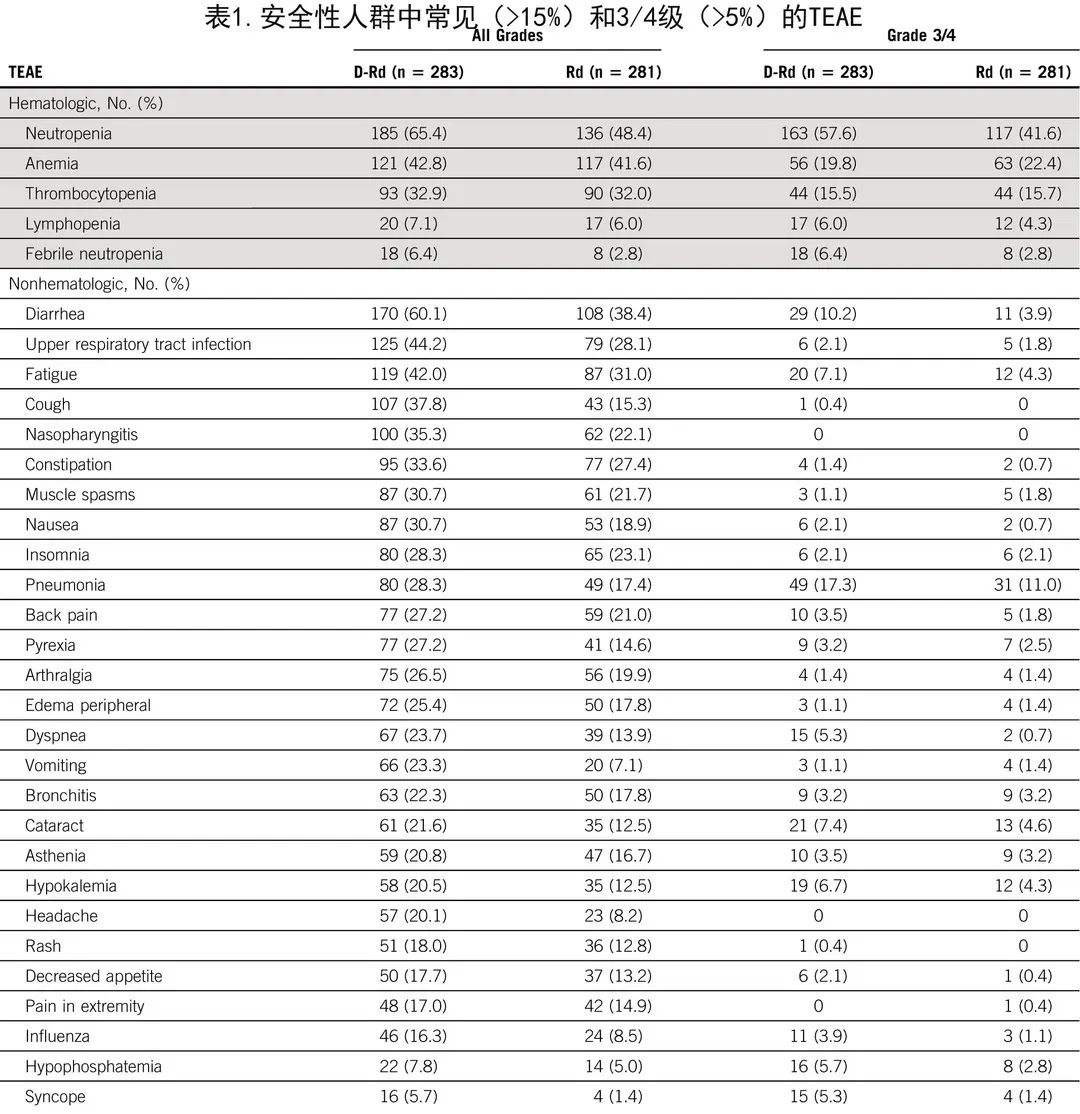
D-Rd 组283例患者中的35例 (12.4%) 和 Rd 组281例患者中的24例 (8.5%) 报告了导致死亡的TEAE。结局为死亡的最常见 TEAE 为脓毒性休克 (1.4% v 0.4%)、心脏停搏 (1.1% v 0.4%)、猝死 (1.1% v 0.4%)、感染性肺炎 (0.7% v 1.1%)、急性肾损伤 (0.4% v 1.1%) 和脓毒症 (0% v 1.1%)。研究期间未发生因新冠肺炎导致的死亡。
D-Rd 组283例患者中有40例 (14.1%)、Rd组281例患者中有30例 (10.7%) 在长期随访期间发生第二原发恶性肿瘤(皮肤、侵袭性和血液学)。在两个治疗组中,第二原发恶性肿瘤均未发现主要类型。校正研究治疗暴露后,D-Rd组和 Rd 组的第二原发恶性肿瘤发生率相似(0.35 VS 0.45起事件/100患者-月风险)。
结论
在超过6.5年的随访(中位随访79.7个月)后,在 RRMM 患者中,与 Rd 单独治疗相比,在 Rd 方案中添加达雷妥尤单抗继续显示出显著的临床获益,包括随访时间更长时的显著 OS 优势。与Rd相比,达雷妥尤单抗联合Rd可显著延长OS(67.6 VS 51.8个月),死亡风险降低27%;OS曲线在约7个月时分离,并随时间持续分离。这也是迄今为止在RRMM患者中开展的基于Rd的三联治疗的III期研究获得的最长中位OS。
此外基于预先指定的亚组分析,在几乎所有亚组中均观察到 D-Rd 组的OS改善,不考虑年龄、ISS分期、细胞遗传学风险、既往PI暴露或PI /末线治疗难治情况。按既往治疗线数分析时,D-Rd组既往接受过1线治疗的患者的中位 OS 最长(77.8个月),而Rd组为57.7个月。
在POLLUX研究最终分析中,D-Rd组的 MRD 阴性率几乎是 Rd 组的5倍 (33.2% vs. 6.7%),与中位随访54.8个月的结果一致。并且无论治疗组如何,MRD阴性均与 OS 改善相关,进一步证明了实现MRD阴性的重要性。
此外,POLLUX研究的长期随访结果补充并加强了III 期CASTOR研究中达雷妥尤单抗+Vd (D-Vd) 的OS获益。
参考文献
Meletios A Dimopoulos,et al. Overall Survival With Daratumumab, Lenalidomide, and Dexamethasone in Previously Treated Multiple Myeloma (POLLUX): A Randomized, Open-Label, Phase III Trial. J Clin Oncol . 2023 Jan 4;JCO2200940. doi: 10.1200/JCO.22.00940
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言