生物医药中专利之争:诺奖获得者本庶佑准备起诉小野制药
2020-06-11 柏柏 医麦客
6月5日,2018年的诺贝尔奖获得者Tasuku Honjo(本庶佑)宣布,他将对Ono Pharmaceutical Co.(小野制药)提起诉讼,要求小野制药对其PD-1抗癌药物
6月5日,2018年的诺贝尔奖获得者Tasuku Honjo(本庶佑)宣布,他将对Ono Pharmaceutical Co.(小野制药)提起诉讼,要求小野制药对其PD-1抗癌药物Opdivo,向他支付226亿日元(合2.07亿美元)的和解金。该诉讼将于6月中旬在大阪地方法院提起。

此次本庶佑教授的起诉,还要从百时美(BMS)与默沙东(Merck)的一场PD-1明星药物Opdivo与Keytruda的专利之战上说起。事件发展历程如下:
-
早在1992年,本庶佑教授领导的团队就已经鉴定出PD-1基因,并且陆续在1999年到2002年间发表PD-1的免疫机制转导研究。2006年,本庶佑教授团队、小野制药和美国生技公司Medarex共同合作开发抗PD-L1和抗PD-1人用单株抗体中的一种抗PD-1单株抗体——Opdivo,向美国FDA递交研究性新药(IND)申请;并于同年开始针对复发及难治型实体肿瘤患者(非小细胞肺癌、大肠癌、黑色素瘤等)进行临床试验。
-
2009年,Medarex被BMS收购,Opdivo的临床试验、知识产权与后续开发权利由BMS所主导。因而,Opdivo的专利权包括小野制药和本庶佑教授,BMS则拥有此专利权的独占实施许可。 -
2014年12月,Opdivo得到美国FDA的上市许可;而在此之前,2014年9月,默沙东的一款PD-1新药Keytruda已得到FDA的上市许可。因而,两家公司就这两款PD-1药物的专利权展开了长时间的拉锯战。(早在2011年,两家公司就已于德国慕尼黑的欧洲专利局(EPO)对该类专利权展开较量) -
2015年7月,BMS和小野制药在美国德拉瓦州联邦地方法院对默沙东进行起诉,控告默沙东公司于2014年9月获得FDA批准用于治疗转移性黑色素瘤的Keytruda侵犯了其Opdivo的专利权,因为两款药物的作用机制相同。 -
2017年,BMS和小野制药与默沙东和解了该专利诉讼,默沙东公司同意支付6.25亿美元的专利使用费,以及Keytruda在2017年至2026年之间的部分销售收入。

可以说,BMS和默沙东的PD-1专利之战算是告一段落。在此次专利诉讼方中,除了BMS和小野制药外,本庶佑教授团队作为PD-1的最初发现者和研究贡献者,理应也分得一部分和解金和专利使用费。
根据本庶佑教授诉讼说明,小野制药曾表示会向他支付默沙东提供和解金的40%,而之后小野制药又表示,只会向他支付1%的报酬;而持续到目前,小野制药还未向他支付任何款项
本庶佑教授还表示,除了226亿日元的和解金外,他还有资格从小野制药和BMS公司收取专利费,因为两家公司都销售Opdivo。此外,本庶佑教授还说,他将计划利用这笔资金建立一个拥有1000亿日元资金的基金会,以支持年轻的研究人员。
除了此次PD-1专利之争,在CAR-T细胞疗法,CRIPRS基因编辑等领域,也曾发生了过令人咋舌的专利权纠纷。
CAR-T专利之争
众所周知,CAR-T疗法的出世引起了医药界的广泛关注,作为一次性治愈的新型疗法,其治疗的标价一直居高不下,这也引起了国内外不少企业的相继竞争,其专利权更是他们关注的重点。
在CAR-T领域 —— 190专利的获得者,Juno利用其专利权先后起诉了全球仅两款上市的药物开发企业:诺华和吉利德。
-
早在2007年,Kite与一位名为“A”的科学合作者向“190专利发明人之一”的"B"博士请教了一些问题。诉讼称,基于A作为美国国立癌症研究所(NCI)研究员的地位,B向A介绍了2002年一篇关于该专利的期刊文章,因此Juno认为Kite间接性的获取了190专利,并用于实践。 -
2013年,Juno从斯隆·凯特琳和纪念斯隆·凯特琳癌症中心(MSKCC)获得“190专利”的独家授权许可。借此,Juno认为Kite侵犯了其190专利的专属权。 -
随后2017年,吉利德斥资120亿美元收购Kite公司以获得其CAR-T疗法Yescarta,同年,该重磅疗法获得FDA批准上市。 -
故此,2017年,Juno公司起诉吉利德的Kite公司,称其通过抄袭斯隆·凯特琳的研究成果(即190专利权),进而推动其在CAR-T疗法方面的进展,最终使得Yescarta获得FDA批准上市。 -
在起诉的过程中,2018年,新基(celgene)以90亿美元收购了Juno公司,全面布局CAR-T疗法。 -
2019年,BMS豪掷740亿美元收购了新基公司。于是,最初Juno对Kite的起诉转为了BMS和吉利德的对簿公堂。

-
2019年12月,两大公司在加利福尼亚对簿公堂,进行了为期两周的审判,随后陪审团宣布了审判结果:百时美施贵宝(BMS)胜诉,吉利德(Gilead)败诉,吉利德旗下的Kite Pharma因此需要向BMS旗下的Juno Therapeutics及合作伙伴支付7.52亿美元 -
2020年4月,加州法官Philip Gutierrez将判决总额(吉利德向BMS支付)从此前的7.52亿美元扩大到12亿美元,并且根据吉利德支付的时间长短,BMS还将被判给判决后利息。目前,吉利德表示还会进行上诉。

▲ Emmanuelle Charpentier(左)、Jennifer Doudna(中)和张锋(右)
关键人物:在美国和欧盟等多个地区,CRISPR/Cas9专利之战的主要核心是Broad研究所的华人科学家张锋团队和加州大学(UC)伯克利分校代表的国际团队,领军人物为UC的Jennifer Doudna和维也纳大学的Emmanuelle Charpentier。
-
2012年6月,Science在线发表了由加州大学伯克利分校的 Jennifer Doudna 和维也纳大学的Emmanuelle Charpentier所在团队共同完成的一项研究,他们首先找到了将CRISPR-Cas9分子剪刀引导到基因组上目标位置的方法,开发出了实验室可用的基因编辑工具,并称可以用于任何生物。
-
2012年5月,他们提交了专利申请,并称其为“本世纪最大的科学发现”。
-
2013年1月,Broad研究所的张锋及其同事在Nature上首次发表了CRISPR-Cas9基因编辑技术在真核细胞中起作用的报道,这比加州大学和其他研究团队发表类似实验有关的研究早了好几周。
-
2014年4月,Broad研究所率先获得有针对性地改变真核生物(包括动植物)的基因组,进行商业化产品研发的几项CRISPR专利。而加州大学伯克利分校关于CRISPR用于编辑细菌、植物、动物和人类等所有类型细胞的专利申请迟迟没获批,其律师很快对此向美国专利和商标局(USPTO)提出上诉。
-
2017年2月,专利审判和上诉委员会(PTAB)称Broad研究所的专利“不干涉事实”,这意味着它们与UC申请的专利不同,不应该被推翻。
-
2018年4月,美国联邦巡回上诉法院审理革命性基因编辑工具CRISPR的专利纠纷案件。
-
2018年9月,上诉法院驳回加州大学的上诉,判决张锋所在Broad研究所的专利有效。
-
2019年6月,美国专利及商标局(USPTO)发布一份重磅文件,宣布对Broad研究所与加州大学伯克利分校之间的CRISPR/Cas9基因编辑技术专利发了一项新的“干涉 ”(Interference)审查程序。这项声明意味着,两家机构的专利间可能涵盖重叠的知识产权。
基于PTAB的干涉计划,此次干涉很可能在未来一年内完成。根据文件,Broad研究所可以通过与加州大学达成和解协议来避免进一步的麻烦(和律师费)。到目前为止,各方尚未达成停战协议。这一干预措施,使CRISPR的专利归属权再一次蒙上了神秘的面纱。
其判决结果,不仅影响到CRISPR疗法潜在数十亿美元或更大(该技术的价值有多大还不得而知)的市场价值,还可能影响到科学记录册上认定谁是这项革命性技术的发明者,乃至诺贝尔奖的评估获得者。
专利之争的背后,无一不是利益的龙争虎斗。目前,随着生物药的发展,各类创新药物和创新技术也相继走上了商业化之路,这毫无疑问的存在着利益竞争关系,从而也引发了大家对于专利权的重视。
-
2019年PD-1抗体销售额
BMS的Opdivo作为全球第一款上市的PD-1药物,于2014年7月在日本获批上市,上市首年销售额为9.42亿美元。BMS 2019年财报显示,Opdivo销售额为80.15亿美元,较2018年同期增长约7%。而2019年BMS营收总额为261.5亿美元,在全球跨国药企中排名第十,Opdivo的销售占据其全年营收将近三成。据悉,2018年,Opdivo为全球销售额排名首位的PD-1药物,销售额为67.35亿美元。
默克的Keytruda作为全球第二个获批上市的PD-1药物,于2014年9月在美获批上市,上市首年销售额5.66亿美元。Keytruda销售在2018年首次实现超越Opdivo后,2019年首次突破百亿美元大关,销售额达到111亿美元,跻身2019年全球药物销售额TOP3。
-
2020年CAR-T销售额
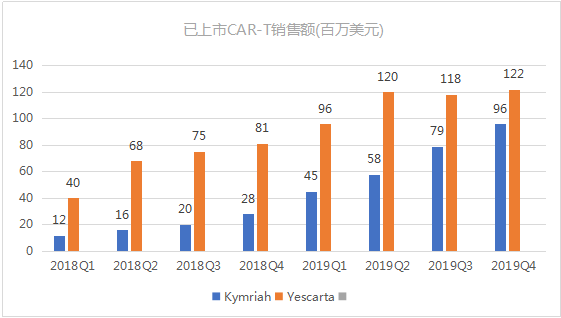
▲数据来源:Novartis季报、Gilead季报
仅从2019年PD-1以及CAR-T的市场销售额,就可以看到一款创新药物的市场价值有多大。而创新的CRISPR基因编辑技术,也在药物研发以及遗传病的治疗中发挥着巨大潜力。
这些潜在的市场价值推动着企业创新,同时促进科研发展进步,为患者提供更优质的治疗方式。从以上专利纠纷之路来看,无论是对个人还是对企业而言,各自专利的维护是有必要的,而努力实现创新才是维护自身利益的关键条件。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#医药#
33
#诺奖#
47
#起诉#
38
#专利#几大有名专利之争
164