【Cancer Treat Rev】DLBCL中改良R-CHOP的路线图
2024-02-20 聊聊血液 聊聊血液 发表于上海
《Cancer Treatment Reviews》近日发表一篇综述,强调DLBCL治疗面临的挑战,以及开发不再依赖于化疗基石的方案的必要性。
DLBCL的治疗
Scylla 和 Charybdis 是希腊神话中的两个海妖,分别是六头海怪和巨大漩涡,守护在狭窄的Messina海峡的两侧,Odysseus想要穿过海峡必须面对两个海妖。弥漫性大B细胞淋巴瘤(DLBCL)的治疗同样如此,传统上依赖于R-CHOP这一化疗支柱作为标准治疗,但也会面临两种危险,一种是侵袭性疾病(Charybdis),另一种是治疗毒性(Scylla)。为了提高治愈率,几十年来一直是通过在R-CHOP标准方案的基础上递增(升阶梯治疗方案)或递减(降阶梯治疗方案)来导航淋巴瘤的治疗前景(图1)。

近些年提出了替代策略,其中维泊妥珠单抗联合R-CHP在治疗方面取得突破,但该方案仍未达到普遍治愈。幸运的是,基因组和分子学技术的进步可以更好地理解疾病的异质性分子性质,从而帮助开发和指导更有针对性、更精确和更个体化的治疗。此外,新的制药技术促进了新型细胞疗法(如CAR-T细胞疗法)的开发,这些疗法可能更有效,同时保持可接受的安全性。
《Cancer Treatment Reviews》近日发表一篇综述,强调DLBCL治疗面临的挑战,以及开发不再依赖于化疗基石的方案的必要性。此外鉴于在人工智能与多组学(基因组学、表观基因组学、转录组学、蛋白质组学、代谢组学)的交叉,还提出需要分析多维的生物学数据,以靶向和个体化的方式对DLBCL发起决定性的攻击。现整理主要内容供参考。

引言
数十年来,DLBCL的标准一线(1L)治疗一直是R-CHOP(表1),直至维泊妥珠单抗联合R-CHP(Pola-R-CHP)获得批准。R-CHOP可治愈50-70%的患者,其余结局则受疾病分期、患者合并症和缓解类型的影响。约20%的 R-CHOP 治疗失败患者存在原发性难治性疾病,而达到完全缓解 (CR) 后约有30%复发。不幸的是,复发/难治性 (R/R) 患者即使接受挽救治疗,但预后和结局仍往往较差。
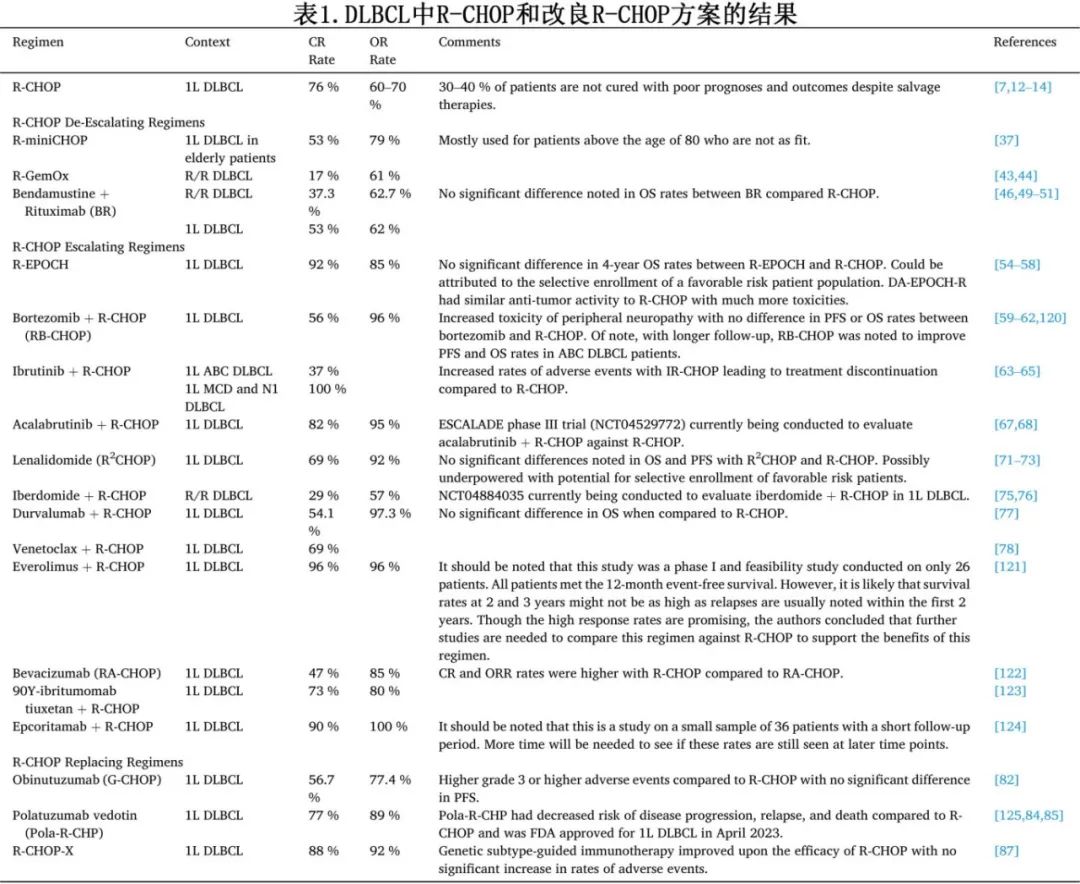
高危 DLBCL 患者,例如 MYC 和 BCL2/BCL6 重排(双打击或三打击淋巴瘤)患者,经常发生 R-CHOP 耐药。耐药疾病患者还经常显示 MYC 和 BCL2 蛋白过表达(双表达淋巴瘤),与非双表达淋巴瘤相比的预后更差。但并非所有双打击淋巴瘤均相同,例如MYC-IG重排患者的至疾病进展时间和总生存期往往劣于MYC-nonIG重排患者。此外, 其他预后因素包括起源细胞亚型,因为GCB和non-GCB 亚型似乎可预测新诊断 DLBCL 的结局。
肿瘤学家致力于改善R-CHOP 疗效时都会面临两个问题:毒性可能增加的升阶梯治疗(例如硼替佐米+RCHOP)与疗效降低的降阶梯治疗(例如mini-RCHOP)。作者为 DLBCL 的药物开发提供了路线图,尝试放弃R-CHOP,并以Pola-RCHP作为所有患者的一线治疗。
航行之旅的开始
DLBCL的治疗模式类似霍奇金淋巴瘤,因为两者均采用了抗体药物偶联物(分别为 Pola 和BV[维布妥昔单抗])的替代策略来放弃之前的标准治疗(分别为 R-CHOP 和ABVD)。随着 HL 治疗取得进展,研究者开始认识到,阻碍 R-CHOP 成功治疗 DLBCL 的障碍是该疾病固有的分子学异质性,而组织学上一致的形态学无法反映这一点。技术进步(例如二代测序[NGS]及基因组和转录组分析)可将 DLBCL 细分为多种亚型(图2和3)。
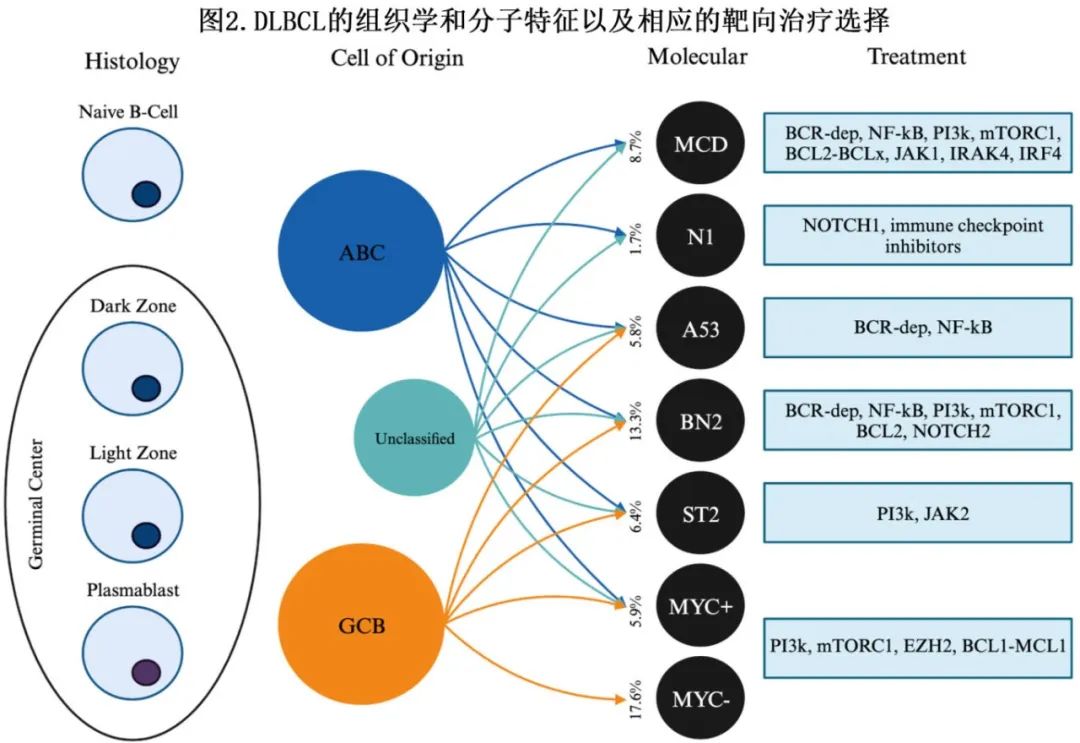
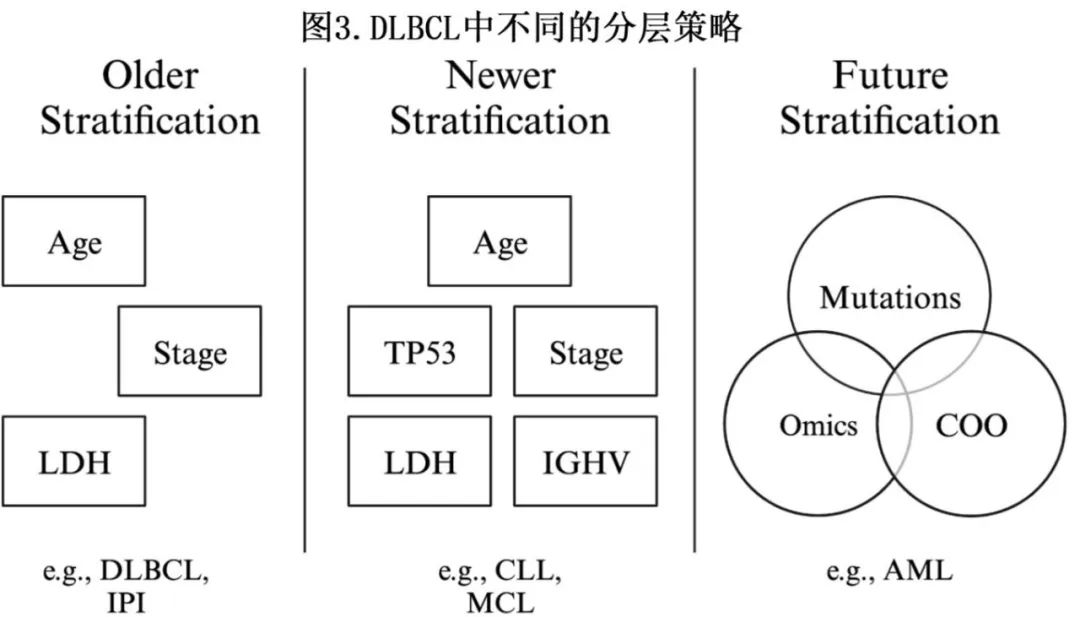
基因表达谱可将 DLBCL 分类为不同亚型:活化 B 细胞样 (ABC)、生发中心 B 细胞样 (GCB) 和无法分类。GCB亚型比 ABC 和无法分类亚型更普遍(GCB 56%,ABC 32%,无法分类11%),GCB 亚型患者初始治疗的结局优于ABC 亚型 (78% vs 56%)。
DLBCL 也可按基因异常(genetic alterations)分层,5种主要的基因亚型为:MCD(MYD88 L265P、CD79B和BCL2 突变)、N1(NOTCH1突变)、A53(TP53突变)、BN2(BCL6和 NOTCH2 突变)、和EZB(EZH2和 BCL2 易位)。关于每种亚型对免疫化疗(R-CHOP或 CHOP 样方案)的反应的分析显示,BN1和 EZB 亚型预后良好,而 MCD 和 N1 亚型预后较差,但MCD 和 BN2 亚型信号通路对 B 细胞受体信号传导的治疗性抑制有反应。最终,DLBCL的高度多样性使得在 R-CHOP 中添加单靶点药物不太可能显著改善所有试验的结局。
改良R-CHOP
改良R-CHOP的方案包括降级、升级和替代策略 (图4),部分具有小的获益,但尚未看到治愈率的显著变化;部分方案因较高副作用而牺牲疗效,因此降低了治愈率;也有许多改良方案的疗效或安全性与 R-CHOP 单独给药相比无明显差异;用 Pola-RCHP 替代 R-CHOP 显示 PFS 改善,但还需要进一步增强。因此,在现有化疗上稍加修改的“一刀切”方案仅具有边际获益,需要放弃。

R-CHOP降阶梯策略示例
R-miniCHOP
降低剂量强度的R-miniCHOP旨在解决 R-CHOP 的毒性特征,帮助老年患者耐受治疗。尽管 R-CHOP 的降阶梯方案(即 R-miniCHOP)并非改善 R-CHOP 结果的真正策略(在这种情况下是通过降低毒性),但它们对于老年unfit患者是必须的。为了改善 R-CHOP 方案,作者提出第一步是从最常用的化疗药物骨架(例如R-miniCHOP)中降级化疗组分,然后添加新药,如双特异性抗体。对≥75岁患者进行的一项研究发现,R-miniCHOP的 ORR 为79%,CR为53%,部分缓解 (PR) 率为26%;与 R-CHOP 相比,R-miniCHOP治疗老年患者的缓解率更高,PFS和 OS 显著改善。由于这些原因,R-miniCHOP用于老年患者,主要是≥80岁的患者,他们不足以耐受全剂量R-CHOP。
R-GemOx
在 DLBCL 中,利妥昔单抗治疗后12个月内复发的患者预后不佳,由于疗效有限和毒性较高,通常不适合强化挽救治疗。利妥昔单抗、吉西他滨和奥沙利铂单药治疗 R/R 淋巴瘤均有效且毒性有限,联合起来就称为R-GemOx,具有有希望的结果。一项初步研究显示,4个周期后,R/R DLBCL患者的 ORR 为83%,2年无事件生存率为43%,2年 OS 为66%;治疗耐受良好。一项 II 期多中心研究显示,4个周期后的 CR 率为44%,PR率为17%,ORR为61%,5年 PFS/OS 率为12.8%和13.9%;耐受良好。由于 R-GemOx 在 R/R 中的疗效,该治疗得以探索作为老年 DLBCL 和体能状态较差患者的 1L 选择,研究仍在进行中(NCT01670370);治疗结束时ORR和 CR 率分别为75%和47%,3级或4级不良事件的发生率较低,无治疗相关死亡。
苯达莫司汀+利妥昔单抗(BR)
在利妥昔单抗治疗后的 R/R DLBCL 患者中,BR达到ORR 为62.7%,CR率为37.3%,中位 PFS 为6.7个月,表明 BR 作为挽救治疗有效。在 DLBCL 一线治疗的 II 期研究中证实了 BR 的疗效,其中53%达到CR,中位 PFS 为10个月,3-4级不良事件的发生率为15.6%,最常见的事件为中性粒细胞减少。最后,在 BRIGHT 研究中,BR在惰性 NHL 中的疗效优于R-CHOP,在 PFS 方面可提供更好的长期疾病控制,且 OS 无显著差异。
R-CHOP升阶梯策略
R-EPOCH
剂量调整的利妥昔单抗、依托泊苷、泼尼松、长春新碱、环磷酰胺和多柔比星 (R-EPOCH) 是 R-CHOP 的强化变体。在最初的 EPOCH 中,早期研究显示R/R、低、中和高级别 NHL 的 ORR 和 CR 较高。一项使用 EPOCH 作为一线 DLBCL 治疗的 II 期研究达到 100% ORR 和92% CR。R-EPOCH在高危患者中达到85%的 ORR 和79%的1年OS。在 MYC 重排病例中,R-EPOCH在 II 期研究中显示总体4年 OS 率为77%,其中双打击淋巴瘤患者为82%。然而,一项最近的回顾性研究发现剂量调整 R-EPOCH 治疗 DLBCL 患者与 R-CHOP 相比4年OS无差异。
DA-EPOCH-R是在研究显示肿瘤耐药性随药物暴露时间延长而降低、多柔比星长期给药的心脏毒性较小以及根据每个周期的中性粒细胞最低值调整药效学剂量后的最大剂量强度后开发的。一项 III 期研究在 III 或 IV 期 DLBCL 患者中比较了剂量调整的 R-EPOCH (DA-EPOCH-R) 与 R-CHOP 的疗效和安全性。中位随访5年,DA-EPOCH-R的2年 PFS 率为78.9%,R-CHOP为75.5%,两组间无显著差异,OS 率也无显著差异(分别为86.5%和85.7%)。但DA-EPOCH-R 组3-4级 AE 发生率显著高于 R-CHOP 组,AE 包括感染(16.9%和10.7%)、发热性中性粒细胞减少症(35.0%和17.7%)、粘膜炎(8.4%和2.1%)和神经病变(分别为18.6%和3.3%)(p<0.001)。因此,DA-EPOCH-R 和 R-CHOP 方案具有相似的抗肿瘤活性,但 DA-EPOCH-R 的毒性更大,这也是其无法作为DLBCL 患者标准治疗的原因。需要注意的是,尽管数据有限,很多淋巴瘤中心在高危患者中使用R-EPOCH。
硼替佐米
在non-GCB DLBCL 患者中以硼替佐米替代长春新碱治疗,相比 R-CHOP 并未显著改善 CR 且引起额外的外周神经病变。最初,REMoDL-B III期研究评估了R-CHOP +硼替佐米 (RB-CHOP),结果显示与 R-CHOP 相比无显著 PFS 或 OS 差异。许多其他随机研究也显示,R-CHOP加用硼替佐米缺乏获益。但随访长达5年REMoDL-B III期研究发现,在 ABC DLBCL 患者中,RB-CHOP组的 PFS 和 OS 率优于 R-CHOP 组(5年OS:RB-CHOP组和 R-CHOP 组分别为80%和67%),因此对于ABC DLBCL 患者亚组,RB-CHOP可能是更适合的一线治疗。
伊布替尼
BTK抑制剂伊布替尼在 ABC DLBCL 中值得关注。PHOENIX III期研究最初发现,伊布替尼 +R-CHOP (IR-CHOP) 与 R-CHOP 治疗组的无事件生存期、PFS或 OS 无显著差异,但事后分析显示年轻(<60岁)non-GCB DLBCL 患者可能从 IR-CHOP 治疗中获益。进一步分析显示,伊布替尼治疗 ABC DLBCL 患者的缓解率 (37% vs. 5%) 和中位总生存期(10.3 vs. 3.4个月)均高于 GCB DLBCL 患者。此外,携带促 BTK 突变的 MCD 和 N1 亚型患者中,IR-CHOP 治疗的生存率为100%。额外的分析显示,在 RNA 测序显示 BCL2/MYC 高共表达的患者中,IR-CHOP的无事件生存率显著高于R-CHOP。在 BCL2/MYC 高共表达的年轻患者中,IR-CHOP 可改善无事件生存期和OS。ABC DLBCL和 MCD 分子亚型可从该靶向治疗中获益,这与淋巴瘤的生物学密切相关。然而,IR-CHOP对>60岁患者有不良影响,导致更多严重事件(如发热性中性粒细胞减少症、腹泻和感染性肺炎)、治疗中止(22.4% vs. R-CHOP组13.6%)和更差的生存趋势。
阿可替尼
ACCEPT试验研究了阿可替尼+R-CHOP 1L治疗DLBCL,达到 95%的ORR 和82%的代谢CR,83%的ABC、88%的GCB和50%的无法分类亚型达到CR。副作用可控,最常见的≥3级事件为发热性中性粒细胞减少症 (13%) 和腹泻 (11%)。ESCALADE III期研究 (NCT04529772) 正在比较阿可替尼+R-CHOP与 R-CHOP 治疗未经治疗的non-GCB DLBCL 的疗效。
来那度胺
来那度胺+R-CHOP (R2CHOP) 的24个月 EFS 达到59%,且无亚型差异。另一项研究报告 R2CHOP 的 ORR 为92%。但比较 R2CHOP 与 R-CHOP 的研究显示 OS 或 PFS 无显著差异。ROBUST研究显示R2CHOP较R-CHOP[治疗 ABC DLBCL 的2年 OS 率相似,R2CHOP组的血液学毒性更多。E1412试验显示R2CHOP 与R-CHOP组的 PFS 相当,但3/4级毒性更多。最后,SENIOR研究使用较低剂量的来那度胺 (R2-miniCHOP),与 R-CHOP 相比,无 PFS 或 OS 获益,但仍发现中性粒细胞减少症、感染和肺栓塞的风险增加。
Iberdomide
Iberdomide(CC-20) 是一种大脑调节剂,通过影响泛素 E3 连接酶活性增强杀肿瘤和免疫刺激作用,可优化 Ikaros 和 Aiolos 蛋白降解,以改善组织分布。在 R/R DLBCL 患者中进行的一项 I/II 期研究发现,Iberdomide+利妥昔单抗达到57%的ORR、29%的 CRR 和29%的PRR。基于这些结果,正在进行一项 Ib 期研究,以评估Iberdomide+ R-CHOP治疗未经治疗的DLBCL(NCT04884035)。
度伐利尤单抗
度伐利尤单抗是一种免疫检查点抑制剂,可破坏 PD-L1/PD-1 和 B7 相互作用,防止 T 细胞抑制。一项在未经治疗的高危 DLBCL 患者中比较度伐利尤单抗+ R-CHOP与 R-CHOP 的 II 期研究中,前者CR 和 PR 率分别为54.1%和18.9%,AE发生率与 R-CHOP 组相似。但该研究未显示 PR 或 CR 结局与 R-CHOP 相比存在显著差异。
维奈克拉
在 II 期 CAVALLI 研究中,维奈克拉+ R-CHOP在既往未经治疗的 DLBCL 患者中达到69%的 CR 率,中位随访时间为32.2 个月;86%的患者发生3/4级不良事件,但死亡率没有明显增加。
探索维奈克拉联合 R-EPOCH 治疗初治双打击或双表达淋巴瘤的研究结果不一致。虽然一项 I 期研究表明安全性可接受,但随后的 II/III 期研究显示,与单独使用R-EPOCH(3.3%) 相比,维奈克拉联合 R-EPOCH 的治疗相关死亡率增加 (17.1%)。
R-CHOP的替代策略
奥妥珠单抗
奥妥珠单抗是一种2型抗 CD20 抗体,与利妥昔单抗相比,可增强细胞定向死亡和抗体依赖性细胞毒性。但比较奥妥珠单抗+ CHOP (G-CHOP) 与 R-CHOP 的 GOYA III 期研究发现 DLBCL 各亚型的3年 PFS 无显著差异。G-CHOP组发生更频繁的≥3级不良事件 (73.7% vs. 64.7%) 和更高的治疗中止率,由于试验结果为阴性,因此G-CHOP 不太适合于DLBCL 治疗。
维泊妥珠单抗
维泊妥珠单抗是一种靶向 CD79b 的抗体偶联物,与BR相比,维泊妥珠单抗联合BR可改善R/R不适合移植的 DLBCL 的疗效。一项 II 期研究评估了维泊妥珠单抗+利妥昔单抗、环磷酰胺、多柔比星和泼尼松 (Pola-R-CHP) 治疗 DLBCL 的疗效;由于神经病变的风险重叠而省略长春新碱。ORR 为89%,CR和 PR 率分别为77%和12%,≥3级不良事件主要为中性粒细胞减少症、发热性中性粒细胞减少症和血小板减少症。随后的 POLARIX III 期研究证实Pola-R-CHP 在无进展生存期 (PFS) 和疾病进展、复发或死亡风险方面优于R-CHOP,尽管总生存率相似,但 Pola-R-CHP 组无疾病进展的患者比例更高 (76.6% vs 70.2%)。此外,基于 POLARIX 研究的成本效益分析表明,Pola-R-CHP是更具成本效益的策略,因为其 PFS 率高于R-CHOP(见表2)。
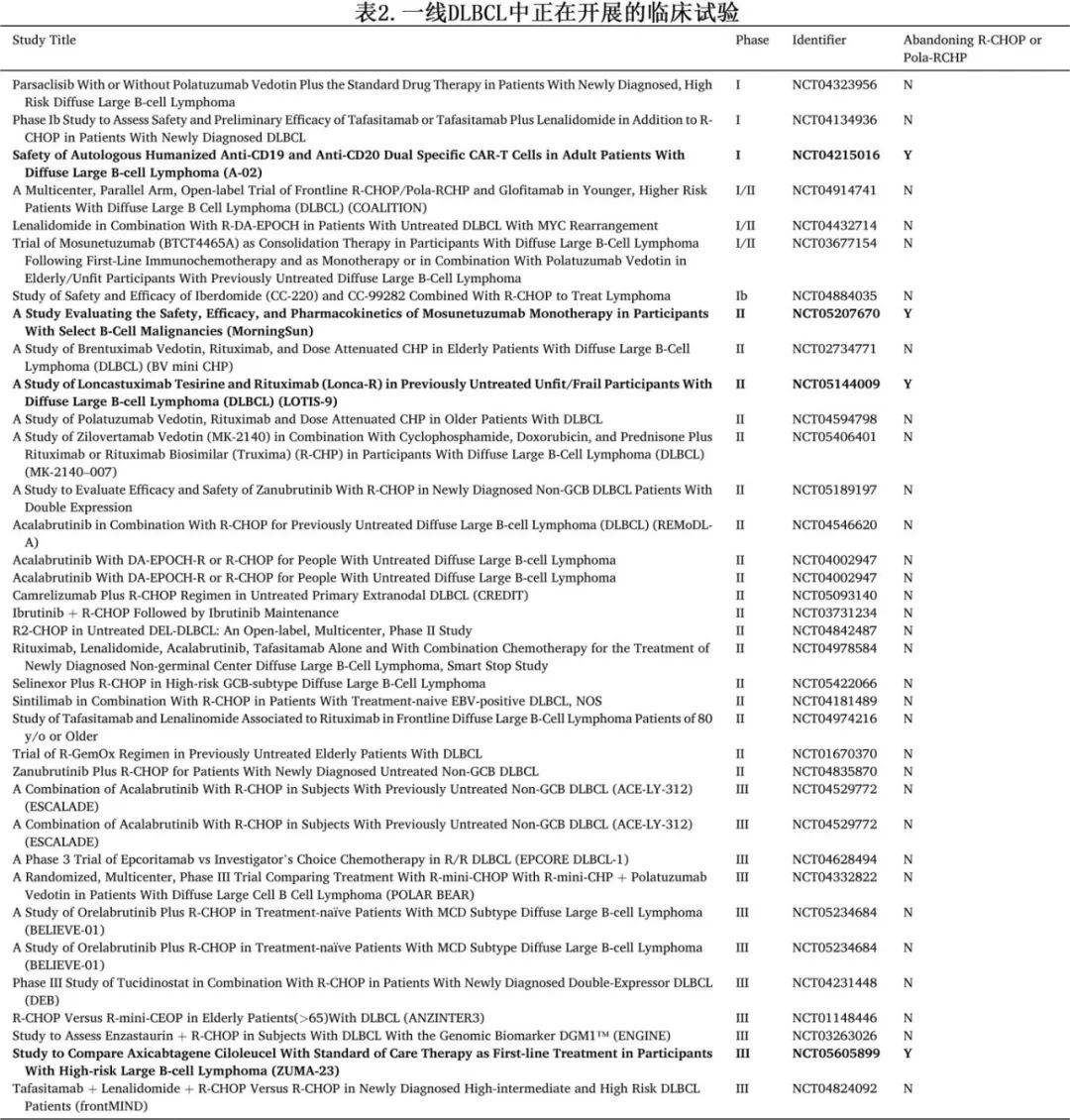
R-CHOP-X
赵维莅教授团队的随机、II期GUIDANCE-01试验 (NCT04025593)旨在评价 R-CHOP 单药或 R-CHOP 联合靶向药物 (R-CHOP-X) 在新诊断 DLBCL 的遗传和淋巴瘤微环境亚型分型指导下的疗效。使用全基因组测序和 RNA 测序数据,将患者分类为 MCD-like、BN2-like、N1-like、EZB-like和 TP53 突变亚型。关于所选靶向药物,MCD-like和 BN2-like(由于该组中观察到BCR-NF-kB异常)给予伊布替尼;N1-like和无法分类组给予来那度胺;EZB-like组(由于 CREBBP/EP300 突变)给予组蛋白去乙酰化酶抑制剂tucidinostat;TP53突变组给予去甲基化药物地西他滨。研究发现 R-CHOP-X 组的 CR 和 ORR 率显著高于 R-CHOP 组 (CR:88% vs. 66%;ORR:92% vs. 73%),2年 PFS 和 OS 率也是如此(PFS:88% vs. 63%;OS:94% vs. 77%)。此外,事后 RNA 测序分析验证了用于选择个体化治疗靶向药物的20基因算法,也证实致癌信号通路在 DLBCL 基因亚型之间存在很大差异。最终,本研究强调R-CHOP-X(基于机制的个性化治疗)可改善 R-CHOP 治疗 DLBCL 的疗效,且不会显著增加毒性。此外,本研究表明,基因亚型指导的免疫疗法是一种非常有前景的DLBCL 一线疗法。
优于R-CHOP+X(或Pola-RCHP+X)的路线图
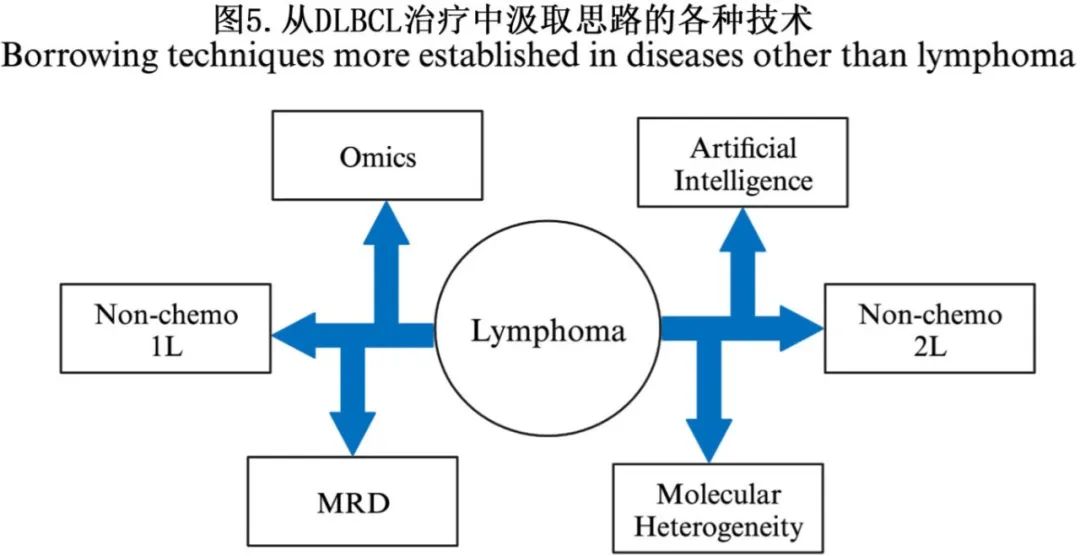
肿瘤学家治疗 DLBCL 的下一个步将是放弃6个周期的 R-CHOP 或 Pola-RCHP,以及几十年来改良标准化疗基石的策略。此外,目标也需要修正(即,寻找一种对所有人或大多数人都有效的治疗方案),因为技术进步揭示出 DLBCL 在不同患者亚组之间存在显著差异。相反,需要利用基因和分子技术的许多进展,在基因组/转录组水平更好地了解每例患者的疾病。现有药物和联合治疗可能已经可以达到持久的治愈率,但许多研究尚未基于疾病的基因组全景对缓解率进行充分分析。因此,如果致力于对患者更完整的基因组认知,就可以利用和开发针对每个患者的定制化新药和治疗策略,并达到多年来一直追求的治愈率。(见图5)。
CAR-T细胞疗法
对于多种 B 细胞淋巴瘤,如DLBCL、套细胞淋巴瘤和滤泡性淋巴瘤,靶向 CD19 抗原的CAR-T 细胞疗法均显示出较高的疗效以及可管理的副作用。Axicabtagene ciloleucel (axi-cel) 的ZUMA-1试验首先研究了两线或多线全身治疗后使用 axi-cel 治疗 R/R LBCL。中位随访63个月时,接受 axi-cel 治疗的患者的中位总生存率为25.8个月,5年总生存率为43%。之后ZUMA-7 试验比较了 axi-cel 与标准治疗 (SOC) 用于二线治疗 R/R LBCL的疗效和安全性,结果83%的患者经 axi-cel 治疗后达到缓解,65%的患者达到完全缓解,而SOC组分别仅为50%和32%;2年OS率分别为61%和52%。毒性方面,91%接受 axi-cel 治疗的患者和83%接受 SOC 治疗的患者发生≥3级不良事件。对于 CAR-T 细胞治疗特异性毒性,主要关注的不良事件为细胞因子释放综合征 (CRS) 和神经系统事件,≥3级 CRS 或神经毒性事件分别为6%和21%。在 R/R 背景下获得这些有前景的结果后,进行了 ZUMA-12 研究(一项前瞻性、II期、多中心、单臂试验),以评价 axi-cel 作为 DLBCL 一线治疗的疗效和安全性,完全缓解率为78%,客观缓解率为89%。在中位随访15.9个月时,73%的患者维持客观缓解。毒性方面,分别有8%和23%的患者出现≥3级 CRS 或神经系统事件。因此,该研究最终强调 axi-cel 作为 DLBCL 的一线治疗高度有效,且副作用可控。后续进行了额外的分析,以确定 DLBCL 的突变情况是否影响对 CAR-T 细胞治疗的反应:MYC、BCL2、CDKN2A和 KLHL6 突变导致 CAR-T 细胞治疗的 PFS 率较低,而BTG2、MYD88和 CD79B 突变导致 PFS 率较高。基于 ZUMA-12 的研究结果,目前正在进行 ZUMA-23 试验,以比较 axi-cel 与一线标准治疗 DLBCL 的疗效和安全性 (NCT05605899)。
有趣的是,与无创术前(prenatal)检测相似,血液活检的全基因组无细胞 DNA 测序可以检测到基因组不稳定数 (GIN),在初步研究中可用于预测 CAR-T 细胞治疗后的反应与复发。
靶向治疗
靶向治疗(伴或不伴化疗)代表着 DLBCL 治疗的下一个前沿。Smart Start研究引入了利妥昔单抗、来那度胺和伊布替尼 (RLI) 方案作为non-GCB DLBCL 的一线治疗,证实靶向治疗联合方案在新诊断DLBCL 患者中的安全性。患者接受 RLI 后接受 RLI 联合 EPOCH 或 CHOP 化疗。值得注意的是,42%的患者为高危,62%的患者有 MYC 和 BCL2 的双表达。两个周期后的ORR为86.2%,CR为36.2%。2年PFS和 OS 分别达到91.3%和96.6%。不良反应包括恶心、周围神经病变、腹泻和粘膜炎等常见症状;16%、38%和12%的患者发生≥3级不良事件。
Smart Start 试验的良好结果促使启动了 Smart Stop 试验 (NCT04978584),旨在评价non-GCB DLBCL 中不同靶向治疗方法。该进行中的研究评价来那度胺、阿可替尼、tafasitamab和利妥昔单抗 (LTRA) 作为独立治疗和联合CHOP 化疗的疗效和安全性,主要目的是测量 LTRA 单药治疗和与 CHOP 联合治疗后的ORR。除生存和安全性评估外,该试验还研究了 LTRA 诱导的 ctDNA 反应和免疫调节。
在 R/R 背景下,靶向治疗联合方案ViPOR(维奈克拉、伊布替尼、泼尼松、奥妥珠单抗和来那度胺)显示出显著的 ORR 和 CR 率(分别为70%和49%),且non-GCB(62% ORR,54% CR) 和GCB (50% ORR,21% CR)DLBCL有所差异。中位 PFS 为9个月(non-GCB 13 个月,GCB 3个月)。不良事件包括血小板减少症 (23%)、中性粒细胞减少症(23%)、腹泻 (67%) 和其他;3-4级不良事件为发热性中性粒细胞减少症 (6%)、低钾血症 (19%)、腹泻 (8%)和房颤 (6%)。加入维泊妥珠单抗 (ViPOR-P) 时结果相似,ORR 和 CR 率为64%和36%;6个月 PFS和 OS 率分别为69.8%和75%。3-4级不良事件为血小板减少症 (17%)、贫血 (7%)、中性粒细胞减少症 (5%) 和低钾血症 (10%);未观察到发热性中性粒细胞减少事件。由于有前景的 R/R 反应,可以期待在一线治疗中研究多种新药联合方案。
值得注意的是,许多研究表明,p53是癌症中最常见的突变基因之一,因此是治疗的理想靶点。正在研究的一种策略是使用复活剂 APR-246 (eprenetapopt/PRIMA-1MET) 直接靶向突变,以恢复野生型活性或稳定野生型,目前正在多项 II 期或 III 期临床试验中进行研究。其中许多研究是在急性髓性白血病或骨髓增生异常综合征患者中开展,但考虑到部分 DLBCL 患者存在TP53 突变,同样可以热切期待靶向策略。
双特异性抗体
在DLBCL一线治疗领域,双特异性抗体(可同时结合两种不同抗原的单克隆抗体)已成为一种有效的治疗途径。Mosunetuzumab靶向CD20和CD3,重定向T细胞以消除恶性B细胞,在一项I期研究中,R/R DLBCL患者的ORR为34.9%(侵袭性)和66.2%(惰性),中位完全缓解持续时间为22.8个月。主要不良事件包括中性粒细胞减少症 (28.4%)、CRS(27.4%) 和低磷血症 (2[13 0.34]%F)。具体到CRS,≥3级事件仅发生1%。随后的 I/II 期试验评估了Mosunetuzumab作为一线治疗用于老年/unfit患者的可能性,在1年随访时,ORR、CRR和 PR 率分别为43%、35%和7%,具有中位15.8个月的持久CR。3例患者发生与 mosunetuzumab 无关的致死性不良事件(自然原因和 COVID-19 性肺炎)。不良事件包括皮疹 (31%) 和疲乏 (26%),还观察到中性粒细胞减少症 (15%) 和CRS(26%)。R/R 背景下有前景的结局促使启动 MorningSun 试验 (NCT05207670),评价Mosunetuzumab单药治疗既往未经治疗的老年/unfit DLBCL 患者。
另一种双特异性抗体是格菲妥单抗(glofitamab),它也靶向 B 细胞上的 CD20 和 T 细胞上的CD3。在 DLBCL 的 R/R 背景下,一项 I/II 期试验表明,格菲妥单抗的 CRR 为56%,CR为43%。在12.6个月的后期随访中,39%的患者达到CR,12个月 PFS 为37%。62%的患者发生≥3级 CRS 事件 (4%) 和≥3级神经系统事件 (3%)。
最后,epcoritamab是一种新型抗 CD20/CD3 双特异性抗体,通过皮下而非静脉给药。在≥2线既往治疗后的 R/R 背景下,EPCORE NHL-1试验发现 epcoritamab 的 ORR 和 CR 率分别为63.1%和38.9%,中位缓解持续时间为12个月。最常见的不良事件为CRS、发热和疲乏,2.5%的患者发生≥3级 CRS 事件。
抗体药物偶联物
抗体药物偶联物 (ADC) 通过连接分子将靶向单克隆抗体与细胞毒素连接。维泊妥珠单抗是一线 DLBCL 治疗中成功的ADC,在 R/R 背景下,PolaR-ICE研究将 Polatuzumab 与 RICE 联合使用,达到的OR、CR和 PR 率分别为92%、55%和37%。副作用与 RICE 相当,没有额外的维泊妥珠单抗相关毒性。正在进行的 POLARGO 研究探索了维泊妥珠单抗与R-GemOx。除了在 R/R 背景下显示了有利的结局,POLARIX研究也证明 ADC 作为 1L DLBCL 治疗的有效性。
另一种试验性 ADC 是loncastuximab tesirine,将抗 CD19 抗体与吡咯苯二氮卓二聚体毒素偶联。在 R/R 背景下,继有希望的 I 期结果后,一项 II 期试验表明该 ADC 获得的ORR、CR和 PR 率为48.3%、50%和50%。≥3级不良事件为中性粒细胞减少症(26%)、血小板减少症 (18%) 和γ-谷氨酰转移酶升高 (17%);39%的患者发生严重不良事件。目前,LOTIS-5 III期试验正在评价 loncastuximab tesirine 联合利妥昔单抗治疗R/R DLBCL (NCT04384484)。
维布妥昔单抗(一种 CD30 ADC)在 CD30 表达水平不同的 R/R DLBCL 患者中显示44%的 ORR 和17%的完全缓解率。
CD47阻断
CD47 被肿瘤细胞过表达,作为生存的抗吞噬信号。在 I/IB 期研究中,抗 CD47 抗体 Magrolimab 显示出与利妥昔单抗联合治疗 R/R 疾病的前景,达到40%的 ORR 和33%的 CR 率。II 期试验 (NCT02953509) 中正在进行进一步评价。值得注意的是,CD47作为信号调节蛋白α (SIRP α) 的配体,可阻止巨噬细胞吞噬肿瘤细胞。因此目前正在开发SIRP α抑制剂。
XPO1抑制
Exportin I(XPO1) 是一种核输出蛋白,可将肿瘤抑制蛋白如 p53 穿梭于细胞核外,而抑制 XPO1 可以恢复肿瘤抑制功能。在 R/R DLBCL 中研究了 XPO1 抑制剂塞利尼索(SADAL研究),OR率达到28%,但具有明显的胃肠道毒性,可能限制其使用。
结论
如本文所示,当试图改善治疗 DLBCL 的基石R-CHOP时,肿瘤学家面临的历史难题为升阶梯治疗的毒性增加和降阶梯治疗的疗效降低。Pola-RCHP的替代策略取得显著成功,但即使是这种策略也尚未达到预期的普遍治愈。因此,一个可能的解决方案可能在于放弃 R-CHOP 或Pola-RCHP,转而进入包括靶向细胞治疗和双特异性抗体的一线药物的新领域,根据每个患者的遗传/分子学组成进行选择。需要强调的是,许多新药需要健康的 T 细胞才能发挥最佳功能,因此需要进一步放弃较老化疗的联合方案。目前,试验正在评价mosunetuzumab单药治疗(MorningSun试验)和 loncastuximab tesirine 联合利妥昔单抗 (LOTIS-5) 的疗效和安全性,可以期待结果。此外,许多试验最初在老年患者中进行(研究者认为无法耐受 R-CHOP 或Pola-RCHP),但也应外推至年轻高危患者。目前在老年unfit患者中研究 loncastuximab tesirine 和利妥昔单抗的 LOTIS-9 试验,由于≥3级不良事件的发生率较高,包括1.7%的5级级别,最近暂停了入组。但需要强调的是,在老年患者中观察到的这些不可接受的副作用可能不会在更年轻、更fit的患者中报告,因此应在过早的完全放弃这些方案前,在年轻患者之前研究它们。
最后,新技术允许进行全外显子组和转录组测序,人工智能 (AI) 也在整合中,研究发现 AI 模型在从组织病理学载玻片诊断淋巴瘤方面取得近100%的准确性,非编码 RNA 的 AI 分析有利于检测新的生物标志物。因此,利用并基于从这些技术进步中获得的知识,可能是了解每例 DLBCL 患者弱点的路径,并为此类患者制定优化治疗,与实体瘤精准肿瘤学领域中的模型相似。最终,对于DLBCL,随着技术和药理学的进步,放弃 R-CHOP 或Pola-RCHP,尤其是对于特定的患者亚群,将是不可避免的。
参考文献
Munoz J,et al.Navigating between Scylla and Charybdis: A roadmap to do better than Pola-RCHP in DLBCL.Cancer Treat Rev . 2024 Jan 17:124:102691. doi: 10.1016/j.ctrv.2024.102691.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#R-CHOP# #DLBCL#
21