以患者为中心的药物临床试验设计技术指导原则(试行)
药审中心组织制定了《以患者为中心的药物临床试验设计技术指导原则(试行)》,经国家药品监督管理局审查同意,现予发布,自发布之日起施行。
国家药品监督管理局药品审评中心 - 药物临床试验 - 2023-07-27
临床试验方案修订对临床试验结果和费用的影响
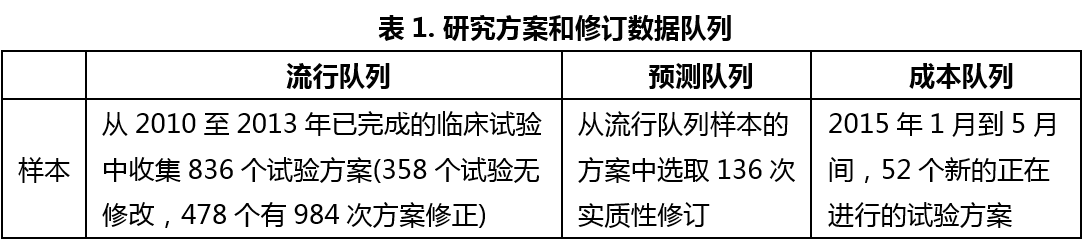
临床试验方案是保证临床试验顺利有序开展的前提,其一经制订并批准就应严格执行。在实际的临床试验开展过程中,有时对临床试验方案确有必要进行修订。但是,如果修订不够谨慎的话,就可能影响到试验结果、试验周期和试验经费。长期以来,对于制药公司和CRO公司而言,因临床试验方案的修订而导致的计划外的推迟、中断和花费都是很大的挑战。
国际药品检查动态研究 - 试验方案,修订 - 2019-12-26
《以患者为中心的药物临床试验设计技术指导原则》(试行)解读
“以患者为中心”的药物研发是以患者的需求为出发点,让患者参与药物研发,该理念已经成为目前药物研发的核心指导思想,因此为了指导以患者为中心的临床试验设计, CDE于20
药融圈 - 临床试验,以患者为中心 - 2023-08-15
临床试验用药品(试行)
根据《药品生产质量管理规范(2010年修订)》第三百一十条规定,现发布《临床试验用药品(试行)》附录,作为《药品生产质量管理规范(2010年修订)》配套文件,自2022年7月1日起施行。
国家药品监督管理局官网 - 临床试验 - 2023-06-10
注意缺陷多动障碍(ADHD)药物临床试验技术指导原则(试行)
为解决注意缺陷多动障碍(ADHD)治疗药物缺乏,鼓励和推动ADHD药物研发,规范临床研究设计,提供可参照的技术规范,在国家药品监督管理局的部署下,药审中心组织制定了《注意缺陷多动障碍(AD
CDE - 注意缺陷多动障碍 - 2021-10-15
多臂随机对照平行临床试验报告规范:CONSORT规范扩展
重要性:随机临床试验的报告质量欠佳。在当今时代,需要更高的研究透明度至关重要,报告不足会阻碍对试验结果的可靠性和有效性的评估。制定《 2010年合并试验标准报告》(CONSORT)的目的是改善随机临床
JAMA . 2019 Apr 23;321(16):1610-1620. doi: 10.1001/jama.2019.3087. - CONSORT规范,报告规范 - 2020-09-24
以患者为中心的临床试验设计技术指导原则(征求意见稿)
“以患者为中心”的药物研发是指以患者需求为出发点、视患者为主动参与者、以临床价值为最终目的,该理念已成为当前药物研发的核心指导思想。为了指导以患者为中心
CDE - 以患者为中心 - 2022-08-09
临床试验有关SOP汇总
临床试验方案修改SOP1. 申办者(包括药厂、CRO等)向中心药物临床试验办公室提出修改申请,填写“药物临床试验修改申请表”。2.提供资料,包括:药物临床试验前研究资料,含试验药物的化学、药学、毒理学、药理学和临床的(包括以前的和正在进行的试验)资料和数据、研究者手册、试验药品药检报告、申办者资质证明、SFDA药物临床试验批文、试验方案和知情同意书药物临床试验办公室根据
MedSci原创 - 临床试验,SOP - 2014-03-28
全球临床试验概况分析
根据美国clicaltrial网站中的临床试验进行统计分析结果,我们可以了解到全球临床试验的概况。整体来说,国际上临床试验处于快速发展阶段,但是美国仍然处于领先地位。中国临床试验数量约占全球的8%。一、临床试验分布情况 据美国clicaltrial统计的结果显示,全球约131,478个临床试验,全在美国占42%,而非美国42%,另外,还有6%的临床试验与美国有关。从些结果来看,美国还是全球绝
MedSci原创 - 临床试验 - 2012-08-26
临床试验也能做公益?
有数据显示,近年来随着国家对生物医药技术创新领域的投入不断加大,药品生产企业及科研单位研发新药的热情日益高涨,我国每年所做的药物临床试验的数量以40%的惊人速度增加,我国正日益成为全球临床试验服务中心。然而与企业和科研单位高涨的热情相比,我国患者参与临床试验的程度的不高,其中的原因:(1)由于患者对临床试验不了解担心患者招募的安全性,(2)患者想参与临床试验,但缺乏途径。仔细分析其中的原因就是临床
MedSci原创 - 2017-07-18
临床试验中的自查
自从15年起国家局对临床试验的一大波动作之后,对临床试验行业的震慑力不用言语,首先是一小批项目被查出数据质量问题公示了,之后是各省局纷纷召集业界开会,一大批项目的自查四起,一时间医院机构神兵降临、烽烟
Clinical Discovery - 2020-03-29
揭露临床试验数据内幕
近日,一系列临床试验敏感数据的公开计划使制药公司、药物监管机构与研发团队们陷入了僵局。然而就在这场“斗争”似乎即将白热化时,一项研究揭示了为什么这些保密资料对于研究者而言是极其重要的。这项研究的分析结果表明,大多数公开的临床试验数据都缺少一些至关重要的信息(例如死亡率与严重的副作用)。但是这些信息却通常能在制药行业制定的、非公开化的标准文件中找到,而这类文件被称为临床研究报告(
生物探索 - 临床试验数据 - 2013-10-29
以患者为中心的临床试验实施技术指导原则(征求意见稿)
“以患者为中心”的药物研发是指以患者需求为出发点、视患者为主动参与者、以临床价值为最终目的,该理念已成为当前药物研发的核心指导思想。为了实施更加患者可及
CDE - 以患者为中心 - 2022-08-09
E17 多区域临床试验规划和设计的一般原则
随着药物开发的日益全球化,来自多区域临床试验 (MRCT) 的数据可以被跨区域和国家的监管机构接受作为支持药物(医药产品)上市批准的主要证据来源变得非常重要。 本指南的目的是描述 MRCT 规划和设计
FDA - 临床试验 - 2021-10-22
为您找到相关结果约500个