Ponesimod治疗成人多发性硬化症:强生已向美国FDA提交新药申请(NDA)
2020-03-19 Allan MedSci原创
强生制药公司今日宣布,已向美国食品和药品监督管理局(FDA)提交新药申请(NDA),以寻求Ponesimod治疗成人复发性多发性硬化症(MS)的上市许可。
强生制药公司今日宣布,已向美国食品和药品监督管理局(FDA)提交新药申请(NDA),以寻求Ponesimod治疗成人复发性多发性硬化症(MS)的上市许可。
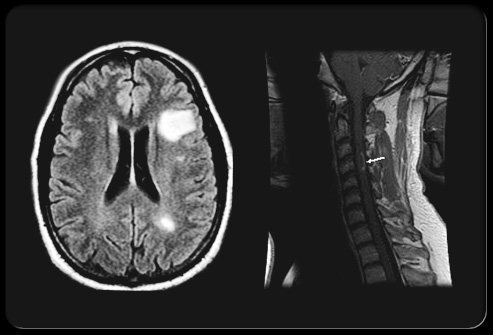
Ponesimod是一种研究性选择性鞘氨醇-1-磷酸受体1(S1P1)调节剂,可抑制S1P蛋白活性,从而可减少可穿过血脑屏障的循环淋巴细胞数量。在MS患者中,免疫细胞进入大脑会损害髓磷脂,髓磷脂的损伤会减慢或停止神经传导,产生MS的神经系统体征和症状。
强生制药公司研发全球负责人Mathai Mammen博士说:“在美国,有将近100万18岁以上的人患有MS,约有85%的患者被诊断患有复发性MS。尽管有新的进步和疗法进入市场,但仍有许多未满足的医疗需求。在接下来的几个月中,我们将与FDA紧密合作,使Ponesimod尽快进入市场”。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#多发性#
38
#硬化症#
42
#新药申请#
41
#强生#
36
#美国FDA#
38
#NDA#
36
#ESI#
24
#Ponesimod#
23