60年来首次!FDA批准重度抑郁口服速效药物Auvelity(右美沙芬与安非他酮缓释复方制剂),1周起效!
2022-08-21 MedSci原创 MedSci原创
重症抑郁(major depressive disorder,MDD)并非是罕见病,全球约有3亿患者,但约2/3的患者对当前抑郁症治疗反应不佳,甚至部分患者在长达6-8周治疗之后也无法达到临床有意义的
重症抑郁(major depressive disorder,MDD)并非是罕见病,全球约有3亿患者,但约2/3的患者对当前抑郁症治疗反应不佳,甚至部分患者在长达6-8周治疗之后也无法达到临床有意义的反应。氯胺酮是第一个上市的NMDA受体调控剂,吸入制剂剂型限制了其应用。对于寻找药代性质更好的NMDA受体拮抗剂的寻找从未停止,但在Auvelity之前尚未有成功案例。
周五,FDA 批准了 Axsome Therapeutics 的 Auvelity,这是 MDD 的第一个速效口服治疗药物,也是60年来第一个口服速效制剂!
Axsome表示,Auvelity是首款获批用于抑郁症治疗的口服NMDA受体拮抗剂,同时也是60年来抑郁症治疗的里程碑式新突破。

Auvelity是两种已获批药物的组合:安非他酮是GSK的抗抑郁药Wellbutrin中的活性药物成分;右美沙芬则是多种咳嗽药物中的常见成分之一。这个组合中,右美沙芬充当NMDA受体拮抗剂,并起到调节谷氨酸神经传递等作用;而安非他酮竞争性抑制细胞色素 P450 2D6 (CYP2D6) 可以增加右美沙芬的生物利用度,还能作为去甲肾上腺素和多巴胺再摄取抑制剂起效。AUVELITY 在治疗 MDD 中的确切作用机制尚不清楚。 AUVELITY 的血液水平是由其成分之间独特的药代动力学相互作用决定的,在稳态时发现这种相互作用是非线性的。
Auvelity的疗效和安全性在包含超过1100名抑郁症患者的综合临床开发项目中得到验证。
III期Gemini研究的结果积极:Auvelity比安慰剂显著改善第6周Montgomery-Åsberg 抑郁评定量表 (MADRS) 分值。Auvelity起效很快,在第一周时候就表现出了具有统计学意义的抗抑郁效果,与安慰剂组形成鲜明对比。在接受治疗2周后,进入缓解期的患者比例更是安慰剂组的两倍以上。
“随着继续治疗,这种对Auvelity的早期益处持续维持并增加,并伴随着良好的安全性和耐受性。”Axsome在新闻稿中指出。
ASCEND试验中,主要终点测量是通过评估从第 1 周到第 6 周 MADRS 总分相对于基线的变化,然后取这些分数的平均值。在主要终点方面,Auvelity在改善1-6周平均MADRS分值上显著优于每天两次安非他酮缓释片105mg治疗。
在安慰剂对照临床研究中,Auvelity主要副作用是眩晕、头疼等中枢症状,其发生率≥5%,是安慰剂的两倍多,但Axsome表示是在预期范围内。
Auvelity 与目前市场上的抗抑郁药名册之间的主要区别在于其快速起效的能力。 虽然目前抗抑郁药的典型反应时间是六到八周或更长时间,但纽约大学抑郁症专家 Dan Iosifescu 医学博士在一次电话会议上表示,Auvelity 的好处可以在一周内看到。
Axsome 的商业和业务发展执行副总裁 Lori Englebert 说:“随着症状在第一周出现改善,然后在第二周出现缓解,这两者的结合目前在市场上具有令人难以置信的差异化。” “如果你看看市场上仍然存在的高度未满足的需求——2/3的患者没有达到缓解,医生现在正朝着缓解作为治疗目标的方向发展——我们对该产品感到非常兴奋。”
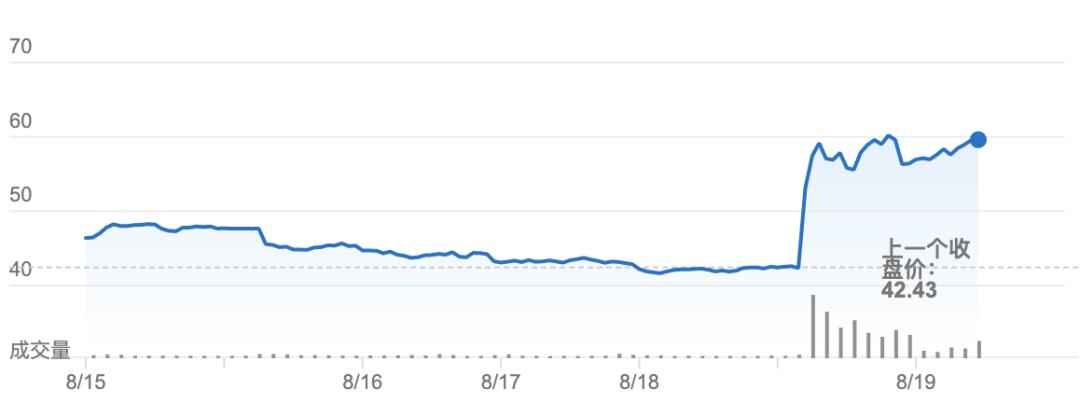
Auvelity于2021年8月提交了上市申请,但由于新药申请存在缺陷,FDA宣布推迟其批准决定。幸好只是好事多磨。获批抑郁症消息一出,当日Axsome的股价就开始飙升,在8月19日交易日结束时上涨40%,达到59.55美元。
据悉,获批治疗抑郁症之外,这款创新疗法还获得FDA授予的突破性疗法认定,用于治疗阿尔茨海默病患者的激越(agitation)症状,目前III期临床试验正在进行中。
Axsome并没有公布该产品的定价,只是表示公司将会结合“确保患者可以广泛使用”以及“支持Auvelity治疗价值”两点因素进行价格决策。Cantor Fitzgerald分析师Charles Duncan在一份报告中指出,Auvelity的年销售额峰值有望达到22亿美元,最终会占据重症抑郁症5%的市场份额。预计该产品每年的定价约为7500美元。
Auvelity是Axsome自研管线的首款成功获批的产品,据悉,该药物的专利保护将持续到2037-2040年。
在等待获批期间,Axsome组建了一个165名员工的销售团队。据该公司透露,此销售团队将服务于包括精神科医生和其他心理健康顾问等在内的约2.5万名美国医疗保健提供者。这些行业人士将覆盖Auvelity约70%的潜在市场。同时,该公司还推出援助计划,对于需要帮助开始使用 AUVELITY 的患者,Auvelity On My Side 患者支持计划将提供全面的患者支持服务,包括 Auvelity On My Side 储蓄卡,以帮助符合条件的商业保险患者更负担得起治疗。此外,Auvelity On My Side 将包括一个示例程序、事先授权支持以及其他患者支持工具。所有程序将在启动后立即可用。
抗抑郁药会增加儿科和年轻成人患者出现自杀念头和行为的风险。 Auvelity 未被批准用于儿童。
关于重度抑郁症 (MDD)
重度抑郁症 (MDD) 是一种使人衰弱的、慢性的、基于生物学的疾病,其特征是情绪低落、无法感到愉悦、内疚和无价值感、精力不足以及其他情绪和身体症状,并损害社会、职业、教育,或其他重要功能。在严重的情况下,MDD 可能导致自杀。根据美国卫生与公众服务部的数据,估计每年有 2100 万美国成年人经历 MDD。根据世界卫生组织 (WHO) 的数据,抑郁症是全球残疾的主要原因,并且是总体全球疾病负担。 近三分之二的确诊和治疗患者在可用的一线治疗中没有获得足够的治疗反应,突显了对新疗法的需求。
关于 AUVELITY
AUVELITY 是一种新型的口服 NMDA 受体拮抗剂,具有多模式活性,被批准用于治疗成人 MDD。 AUVELITY 是一种专有的缓释口服片剂,含有右美沙芬 HBr(45 毫克)和盐酸安非他酮(105 毫克)。 AUVELITY 的右美沙芬成分是 NMDA 受体(一种离子型谷氨酸受体)的拮抗剂和 sigma-1 受体激动剂。这些作用被认为可以调节谷氨酸能神经传递。 AUVELITY 的安非他酮成分是一种氨基酮和 CYP2D6 抑制剂,用于增加和延长右美沙芬的血液水平。 Auvelity治疗抑郁症的确切作用机制尚不清楚。 AUVELITY 获得了 FDA 的突破性疗法指定用于治疗 MDD。
参考资料:
抑郁症治疗60年新突破!FDA批准新机制口服疗法Auvelity,同写意
Axsome’s Wait Pays Off With Broad Auvelity Label For Major Depression
axsome therapeutics announces fda approval of auvelity™, the first and only oral nmda receptor antagonist for the treatment of major depressive disorder in adults
60年来首款!FDA批准抑郁症新机制口服疗法;药明康德
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#FDA批准#
60
#安非他酮#
50
#右美沙芬#
41
#复方制剂#
60
新制剂#重度抑郁症#
78