JCO:特瑞普利单抗治疗鼻咽癌患者带来更长生存获益
2021-01-27 君实生物 君实生物
迄今为止全球范围内已完成的最大规模的免疫检查点抑制剂单药治疗复发或转移性鼻咽癌的临床试验
1月26日,特瑞普利单抗单药作为二线及以上治疗用于复发或转移性鼻咽癌(RM-NPC)的POLARIS-02研究(NCT02915432)的研究成果获国际著名期刊《临床肿瘤学杂志》(Journal of Clinical Oncology,IF: 32.956)在线发表,中山大学附属肿瘤医院的徐瑞华教授为本文的通讯作者,王风华教授为第一作者。
POLARIS-02研究是一项多中心、单臂、II期临床研究,旨在评估特瑞普利单抗在化疗失败的RM-NPC患者中的抗肿瘤活性及安全性,并探索治疗相关的生物标志物,是迄今为止全球范围内已完成的最大规模的免疫检查点抑制剂单药治疗复发或转移性鼻咽癌的临床试验,共纳入190例RM-NPC患者。该研究曾多次在ESMO(欧洲肿瘤内科学会)年会、ASCO(美国临床肿瘤学会)年会等著名国际肿瘤学学术大会上亮相,并获得美国食品药品监督管理局(FDA)授予的孤儿药资格和突破性疗法认定,这也是中国抗体类药物第一次获得FDA的突破性疗法认定。此次新发表的研究结果为特瑞普利单抗治疗RM-NPC的安全性和有效性提供了有力证据。

▲ POLARIS-02研究成果荣登《临床肿瘤学杂志》,
Accepted on November 9, 2020 and published at ascopubs.org/journal/ jco on January 25, 2021: DOI https://doi. org/10.1200/JCO.20. 02712
本土高发瘤种:免疫治疗方案亟需“零”突破
鼻咽癌(NPC)是一种原发于鼻咽部黏膜上皮的恶性肿瘤,分布具有鲜明的地域性特征,在中国南部两广地区(如广东、广西等)尤其高发。2018年全球有12.9万新发病例,中国有6.06万新发病例,约占全球新发病例的47.7%。此外在全球范围内,中国的死亡病例数也位居第一。
与头颈部其他鳞状细胞癌相比,鼻咽癌具有易转移扩散的特点。约5-8%的鼻咽癌患者在诊断时存在远处转移,30%-60%的局部晚期患者会出现远处转移。复发或转移性鼻咽癌患者的预后非常差,含铂双药化疗为标准一线治疗方案,但对于一线含铂类化疗失败的患者,国内外目前缺乏标准的后线治疗方案,现有治疗药物未能明显改善患者的中位生存期。接受二线或以上治疗的患者中位总生存时间(mOS)仅为11.5~12.5个月。
以往观察到与鼻咽癌密切相关的EB病毒(EBV)可诱导癌细胞表达高水平PD-L1,提示抗PD-1治疗在鼻咽癌领域具有潜在治疗作用。但截至发稿日,全球范围内尚未有免疫检查点抑制剂获批用于治疗鼻咽癌,存在迫切的未被满足的临床需求。
POLARIS-02研究:特瑞普利单抗为鼻咽癌患者带来更长生存获益
2016年12月至2019年2月,POLARIS-02研究在国内17家研究中心入组了190例既往接受过全身系统化疗失败的RM-NPC患者(≥18岁),接受特瑞普利单抗单药治疗(3mg/kg,IV,Q2W)。结果显示,特瑞普利单抗表现出持久的抗肿瘤活性和生存获益,安全性可控,且无论患者PD-L1表达如何,均可获益。
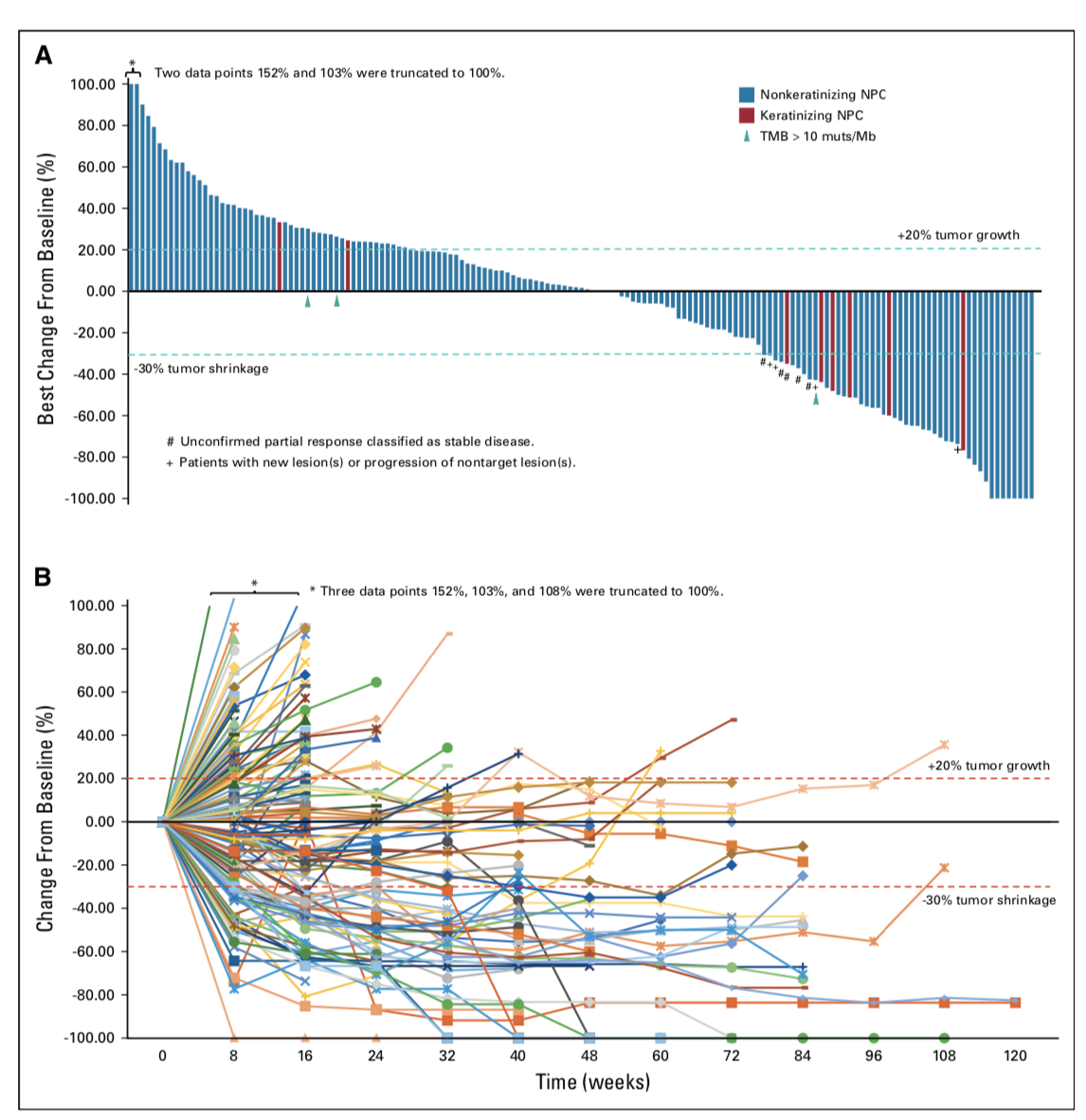 Tumor responses of patients with nasopharyngeal carcinomain this study cohort
Tumor responses of patients with nasopharyngeal carcinomain this study cohort
截至2020年2月19日(末例受试者入组1年后),在全部190例接受特瑞普利单抗单药治疗的晚期鼻咽癌受试者中,基于独立影像学评估委员会(IRC)评估的客观缓解率(ORR)为20.5%,疾病控制率(DCR)为40.0%,中位总生存时间(mOS)为17.4个月,达到了预设的研究终点。此外,在92例接受过至少二线系统化疗失败的患者中,特瑞普利单抗单药治疗的ORR为23.9%,DCR为41.3%,mOS达到15.1个月。
“特瑞普利单抗在二线及以上的鼻咽癌患者中,具有稳定的治疗疗效,而且不良反应可控。”中山大学附属肿瘤医院徐瑞华教授表示,“更难能可贵之处在于,该研究近半数的患者既往已经进行过二线,甚至三线治疗,但是治疗有效率仍然较高,患者生存期获益较大。”
研究中还发现,血浆EBV DNA滴度的动态变化可能是临床疗效的预测指标,将为定位获益人群、实施精准治疗提供重要参考。研究者对148例患者的血浆EBV DNA拷贝数进行了动态监测,在治疗早期,获得客观缓解患者的EBV DNA滴度较基线的下降幅度显著大于疾病稳定(SD)或疾病进展(PD)的患者。第28天时,EBV DNA滴度下降超过50%的患者,有48.3%可能获得客观应答,对早期疗效预判提供重要参考证据。
徐瑞华教授表示,“POLARIS-02研究为一线治疗失败的晚期鼻咽癌患者提供了新的治疗选择,期待该药尽快获批进入临床应用,以便提升晚期鼻咽癌的总体治疗水平,从而为国际鼻咽癌治疗贡献中国力量。”
全线贯穿:特瑞普利单抗加速布局鼻咽癌治疗领域
特瑞普利单抗是由君实生物自主研发,在国内上市的首款国产抗PD-1单抗。目前特瑞普利单抗已在全球开展了覆盖十多个瘤种的三十多项临床试验,其中仅针对鼻咽癌治疗领域的研究就贯穿了一线、二线及以上治疗。
此次发表的POLARIS-02研究针对接受二线及以上治疗的患者,基于其研究成果,特瑞普利单抗被纳入2020年《中国临床肿瘤学会(CSCO)头颈部肿瘤诊疗指南》复发/转移性鼻咽癌的二线或挽救治疗推荐。
同时,2020年4月,特瑞普利单抗适用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗的新适应症上市申请获得国家药品监督管理局(NMPA)受理,并于7月被纳入优先审评程序。这也是全球首个抗PD-1单抗治疗复发或转移性鼻咽癌的新药上市申请。2020年5月及9月,特瑞普利单抗治疗鼻咽癌分别获得FDA授予的孤儿药资格和突破性疗法认定,成为首个获得FDA突破性疗法认定的国产抗PD-1单抗。
在一线治疗领域,2020年9月,特瑞普利单抗联合化疗一线治疗鼻咽癌的国际多中心Ⅲ期临床研究(JUPITER-02研究)达到主要研究终点。
基于JUPITER-02研究和POLARIS-02研究结果,君实生物将于近期分别向NMPA和FDA递交新适应症/新药上市申请。
“能够在肿瘤领域的国际重磅期刊上展示研究成果,对我们中国创新药的研究者来说是极大的肯定和鼓励。”君实生物副总经理姚盛博士表示,“长期以来,鼻咽癌作为中国等特定区域的高发疾病,在全球新药研发层面未受到足够的重视,存在大量未被满足的临床需求。而君实生物是一家立足中国的创新药企,我们持续关注国人中高发,且对免疫治疗有较好响应、临床急需治疗的瘤种。目前,君实生物仅在鼻咽癌领域就布局了‘全线贯穿’的抗PD-1免疫单药和联合治疗的关键注册临床研究。我们希望能够推动更多本土创新药物循证医学证据的产生,为世界提供来自中国的标准治疗方案。”
—— 完 ——
关于拓益®(特瑞普利单抗注射液)
拓益®(特瑞普利单抗注射液)作为我国批准上市的首个国产以PD-1为靶点的单抗药物,获得国家科技重大专项项目支持。本品获批的第一个适应症为用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗,并获得2019年和2020年版《中国临床肿瘤学会(CSCO)黑色素瘤诊疗指南》推荐。2020年4月,拓益®适用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗的新适应症上市申请获得国家药监局受理。2020年5月,拓益®适用于既往接受系统治疗失败或不可耐受的局部进展或转移性尿路上皮癌患者的治疗的新适应症上市申请获得国家药品监督管理局受理。2020年7月,上述两项新适应症上市申请已被国家药品监督管理局纳入优先审评程序。2020年9月,拓益®用于治疗鼻咽癌获得美国食品药品监督管理局突破性疗法认定。目前,拓益®已在黏膜黑色素瘤、鼻咽癌、软组织肉瘤领域获得FDA授予1项突破性疗法认定、1项快速通道认定和3项孤儿药资格认定。2020年12月,拓益®成功通过国家医保谈判,被纳入新版目录。
拓益®自2016年初开始临床研发,至今已在全球开展了30多项临床研究,积极探索本品在黑色素瘤、鼻咽癌、尿路上皮癌、肺癌、胃癌、食管癌、肝癌、胆管癌、乳腺癌、肾癌等适应症的疗效和安全性,与国内外领先创新药企的联合疗法合作也在进行当中,期待让更多中国以及其它国家的患者获得国际先进水平的肿瘤免疫治疗。
关于君实生物
君实生物(1877.HK,688180.SH)成立于2012年12月,是一家以创新为驱动,致力于创新疗法的发现、开发和商业化的生物制药公司。公司具有丰富的在研产品管线,包括27个创新药,2个生物类似物,覆盖五大治疗领域,包括恶性肿瘤、自身免疫系统疾病、慢性代谢类疾病、神经系统类疾病以及感染性疾病。
凭借蛋白质工程核心平台技术,君实生物身处国际大分子药物研发前沿,获得了首个国产抗PD-1单克隆抗体NMPA上市批准、国产抗PCSK9单克隆抗体NMPA临床申请批准、全球首个治疗肿瘤的抗BTLA阻断抗体在中国NMPA和美国FDA的临床申请批准。今年,君实生物还与国内科研机构携手抗疫,共同开发的JS016已作为国内首个抗新冠病毒单克隆中和抗体进入临床试验,用本土创新为中国和世界疾病预防控制贡献力量。目前君实生物在全球拥有两千多名员工,分布在美国旧金山和马里兰,中国上海、苏州、北京和广州。
参考文献:
Wang, Feng-Hua et al. “Efficacy, Safety, and Correlative Biomarkers of Toripalimab in Previously Treated Recurrent or Metastatic Nasopharyngeal Carcinoma: A Phase II Clinical Trial (POLARIS-02).” Journal of clinical oncology : official journal of the American Society of Clinical Oncology, JCO2002712. 25 Jan. 2021, doi:10.1200/JCO.20.02712
- 梁锌,杨剑,高婷,张志超,陈艳佳,郑荣寿. 中国鼻咽癌流行概况.中国肿瘤. 2016,25(11):835-840.
- CHEN YP, CHAN ATC, LE AT, et al. Nasopharyngeal carcinoma. Lancet, 2019, 394(10192):64-80.
- Wanqing Chen, Rongshou Zheng, Peter D. Baade, Siwei Zhang, Hongmei Zeng, Freddie Bray et al., Cancer Statistics in China, 2015. CA CANCER J CLIN 2016;66:115-132.
- Xun Cao, Li-Ru He, Fang-Yun Xie, You-Fang Chen, Zhe-Sheng Wen. Factors determining the survival of nasopharyngeal carcinoma with lung metastasis alone: does combined modality treatment benefit? BMC Cancer 2011, 11:370
- UICC EML Review - NPC – 2014. Nasopharyngeal Cancer: Statistics. Cancer net. 01/2020.
- Prawira A, et al. Br J Cancer. 2017 Dec 5;117(12):1743-1752.
- ChenBJ, Chapuy B, Ouyang J, et al. PD-L1 expression is characteristic of a subset of aggressive B-cell lymphomas and virus-associated malignancies. Clin CancerRes 2013;19:3462-73.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#瑞普利单抗#
38
#生存获益#
45
#JCO#
26
迄今为止全球范围内已完成的最大规模的免疫检查点抑制剂单药治疗复发或转移性鼻咽癌的临床试验
68