【衡道丨笔记】细胞学快速现场评估在肺泡蛋白沉积症中的诊断价值
2023-08-28 衡道病理 衡道病理 发表于上海
在诊断性介入肺脏病学操作中,细胞学快速现场评估(Rapid on-site evaluation,ROSE)是一种实时伴随于取材过程的快速现场细胞学判读技术。
内容摘要
ROSE定义及价值
快速现场评估
定义:
在诊断性介入肺脏病学操作中,细胞学快速现场评估(Rapid on-site evaluation,ROSE)是一种实时伴随于取材过程的快速现场细胞学判读技术。靶部位取材时,在基本不损失组织标本前提下,将部分标本印涂于玻片,制成细胞学片基,迅速染色并以专用显微镜综合临床信息立即判读。
三大主要作用:
-
评估样本质量,提高标本合格率及活检诊断率
-
初步确定病变的性质,在短时间内向临床医生提供参考性细胞学诊断意见
-
分流标本进行后续检查,指导病人的治疗
肺泡蛋白沉积症(PAP)
肺泡蛋白沉积症(pulmonary alveolar proteinesis,PAP)
-
以肺泡巨噬细胞功能障碍和肺泡表面活性物质在肺泡腔内积聚为特征的一种少见的弥漫性肺疾病
-
肺泡表面活性物质:
-
支气管肺泡灌洗(broncho alveolar lavage,BAL)
明确诊断依赖病理检查,细胞学检查在PAP诊断中占重要地位
肺泡表面活性蛋白(surfactant protein,SP)
SP有SPA、B、C、D4种类型,受到ACII分泌和巨噬细胞清除两者之间的严格平衡调控:
-
透射电镜可观察其特殊的嗜锇性板层小体(osmiophilic multiamellar body.OMB)
-
可以通过过碘酸-希夫(PAS)染色和淀粉酶消化PAS(PAS-D)染色显示
PAP发生时,肺泡表面活性物质在肺泡腔内聚集,可以随着痰液或者肺泡灌洗液排出,如果透射电镜在痰液或者BALF中检出OMB可以辅助PAP的诊断。
Ⅱ型肺泡细胞与表面活性物质

Ⅱ型肺泡细胞(type Ⅱ alveolar cell,AC Ⅱ):
-
较小,立方形或圆形,顶端突入肺泡腔,散在凸起于Ⅰ型肺泡细胞间,覆盖肺泡5%的表面积;
嗜锇型板层小体(osmiophilic multiamellar body,OMB)&表面活性物质:
-
ACII核上方有较多高电子密度分泌颗粒,呈同心圆、髓鞘样或平行排列的板层状结构
-
内含表面活性物质,以胞吐方式释放,分布于肺泡液体分子层表面,降低肺泡表面张力、维持稳定肺泡大小与结构
病因、分类
先天性PAP
其是由肺泡表面活性物质相关基因(如SFTPB、SFTPC和ABCA3)的突变导致了表面活性物质的代谢异常而发病,可见于新生儿、儿童和成人,约占5%
原发性PAP
是粒细胞-巨噬细胞集落刺激因子(granulocyte macrophage colonystimulating fatcor,GM-CSF)信号传导受损、导致巨噬细胞和粒细胞功能障碍所致,分为两种亚型:
①自身免疫性PAP(aPAP):又称特发性PAP,由GM-CSF自身抗体水平升高所致,最常见,约占85%
②遗传性PAP,是由编码GM-CSF受体亚基基因(CSF2RA或CSF2RB)的常染色体隐性突变引起的遗传疾病,其导致细胞表面蛋白质表达降低(<5%)
继发性PAP
其是由各种其他疾病导致的肺泡巨噬细胞的数目和/或功能异常导致肺泡表面活性物质代谢异常,约占5%
这些潜在与PAP发生相关的疾病包括:慢性血液系统疾病、恶性肿瘤、免疫缺陷综合征,慢性炎症和感染;有毒物质吸入和职业以及环境暴露等
三者共通点:肺泡巨噬细胞清除表面活性物质功能下降
发病机制
-
ACⅡ合成、组装和分泌表面活性物质(脂质+表面活性蛋白SP)
-
肺泡巨噬细胞通过磷脂的分解代谢和胆固醇的流出和反向运输将大约一半的表面活性物质清除到肝脏
-
肺泡巨噬细胞的成熟、分化以及吞噬、代谢表面活性物质的能力受到GM-CSF的调节
-
肺泡巨噬细胞清除表面活性物质功能下降
肺泡蛋白沉积症(PAP)的诊断
临床及影像学特征:
临床特征:
可发生于任何年龄,30-50岁多见,男性多于女性
临床表现变异大:多变、非特异、隐匿
-
1/3患者无明显临床症状;1/5继发感染为首发表现:发热、咳脓性痰;
-
反复咳嗽、渐进性劳力性呼吸困难,肺功能障碍;
-
胸部影像表现较重,而临床表现往往相对轻微(症状和影像表现不一致);病变晚期:肺间质纤维化及实变影
-
原发性PAP患者较少出现肺外表现,继发性PAP(感染、血液系统疾病等)常有原发病的相应症状和体征几乎没有肺部体征:部分合并纤维化的患者可闻及爆裂音,重症患者可有发绀,少数患者可见杵状指(趾)
实验室检查
-
血清和BALF中GM-CSF抗体浓度增高,是支持aPAP诊断的依据之一
-
LDH、CK19、黏蛋白KL-6升高
肺功能检查:
-
早期可能无明显受损,弥散功能下降常先于通气功能和容量异常
-
限制性通气功能障碍伴弥散功能下降
-
低氧和肺泡动脉氧分压差增加
影像学检查:
-
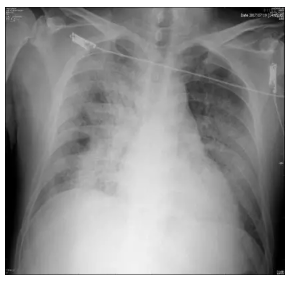
胸部X线:双侧肺门向外放射形成羽毛状或结节状浸润影("蝶翼征”),双肺弥漫磨玻璃样高密度影、散在粟粒影,进展融合成片状影
-
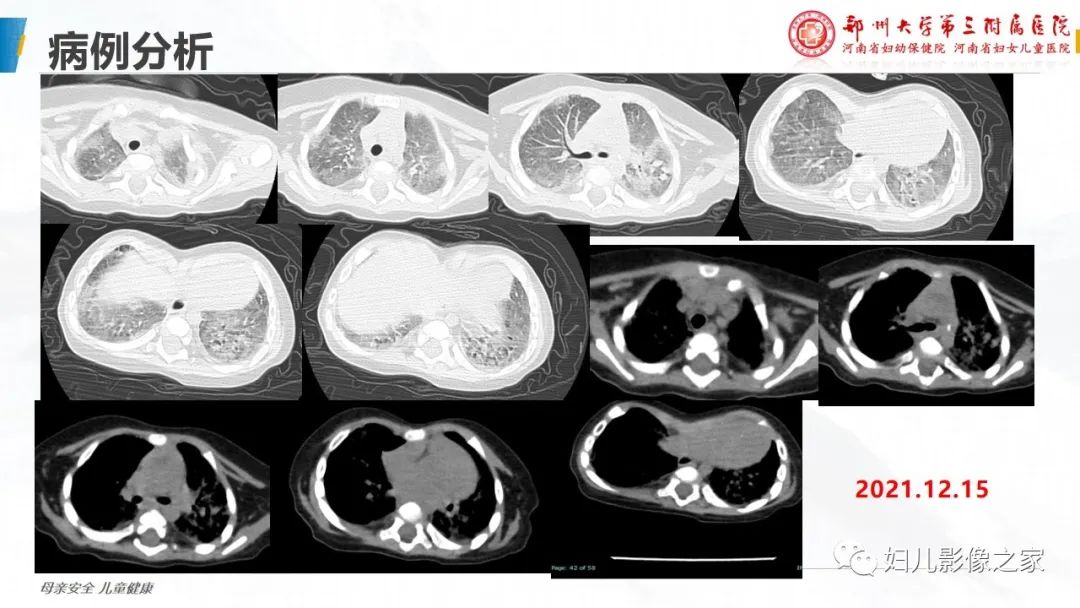
胸部HRCT;
有较高的特异性和敏感性,表现为两肺弥漫磨玻璃影,常合并小叶间隔及小叶内间质增厚使之呈网状,即“铺路石征”
病双肺多发斑片状磨玻璃改变,呈“地图征”,较少出现牵张性支气管扩张和肺纤维化
病理学特征-TBLB组织病理:
镜检:
①肺泡腔和终末呼吸性细支气管内充满细小颗粒状或嗜伊红的脂蛋白性红染物,散在分布有巨噬细胞和针状裂隙
红染物PAS-D染色呈阳性反应(提示为脂蛋白),肺泡表面活性物质免疫组化染色呈阳性反应,冷冻切片油红O染色可见针状裂隙为红染结晶,偏光显微镜下针形结晶有双折光性
②肺泡壁及呼吸性细支气管无或者轻度炎症反应,较少出现淋巴细胞等炎症细胞浸润,早期肺泡结构完好,病程进展逐步发生间质纤维化
透射电镜观察:
肺泡腔内有大量游离嗜锇性板层小体(OMB),可见巨细胞胞质中被吞噬的OMB
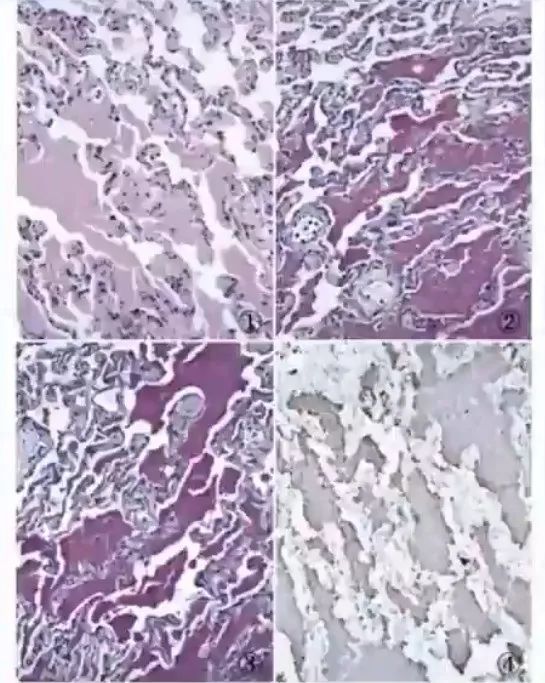
图1 肺泡结构尚存,肺泡内充满嗜伊红的脂蛋白性红染物
图2 PAS染色呈红色
图3 PAS-D 染色呈红色
图4 SP-B免疫组化染色呈棕色,EaVision法
病理学特征-细胞病理
细胞学检查在PAP的诊断中占有重要地位
-
肺活检阴性以及有禁忌症患者往往依赖于支气管肺泡灌洗液(bronchoallveolar lavage fulid,BALF)细胞学检查协助诊断
-
有禁忌症不能获得BALF的患者痰液沉淀物的光镜及透射电镜检查可协助PAP的诊断
细胞学诊断在标本采集、涂片、切片制作,染色、形态学判读和诊断等方面与组织学不同,操作的不规范性制约了PAP的细胞学诊断水平
为此,中国医师协会呼吸医师分会病理工作委员会制定了《肺泡蛋白沉积症细胞学病理诊断中国专家共识》
细胞病理-标本类型、细胞块切片及染色
细胞学标本包括BALF沉淀物、痰液和诱导痰沉淀物
BALF是PAP细胞病理诊断最重要的样本,沉淀物可分别制作离心涂片、细胞蜡块切片和电镜样本超薄切片
上述涂片和切片还可以分别进行PAS、PAS-D染色以及相关的免疫组化染色等,以协助细胞病理学诊断
BALF标本
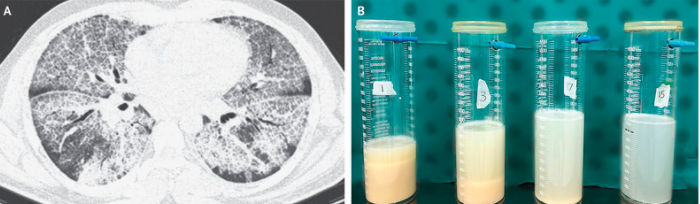
大体表现
眼观:不同程度的浑浊,典型者呈乳白色(牛奶状/泥浆样)静置或离心后可获得深褐色沉淀物

光镜表现
沉淀物石蜡包埋块切片和HE染色:
-
光镜观察可见均质嗜伊红性细颗粒状脂蛋白性物质,有时可见针状裂隙,肺泡巨噬细胞内可见粉红色颗粒蛋白样物质
-
PAS、PAS-D染色阳性,黏液卡红染色阴性
ROSE涂片、BALF离心涂片的免疫组化及特殊染色检查可达到类似或更佳的检测效果

透射电镜表现
透射电镜样本的制备:
收集新鲜BALF样本5ml放入离心管→2000r/min离心20min→弃上清液→经3%戊二醛和1%四氧化锇2ml固定1h→系列乙醇和丙酮脱水→环氧树脂618包埋→超薄切片机切片(厚50~60nm)→行醋酸铀(块染)和枸橡酸纳(片染)双重染色→透射电镜下观察并摄片
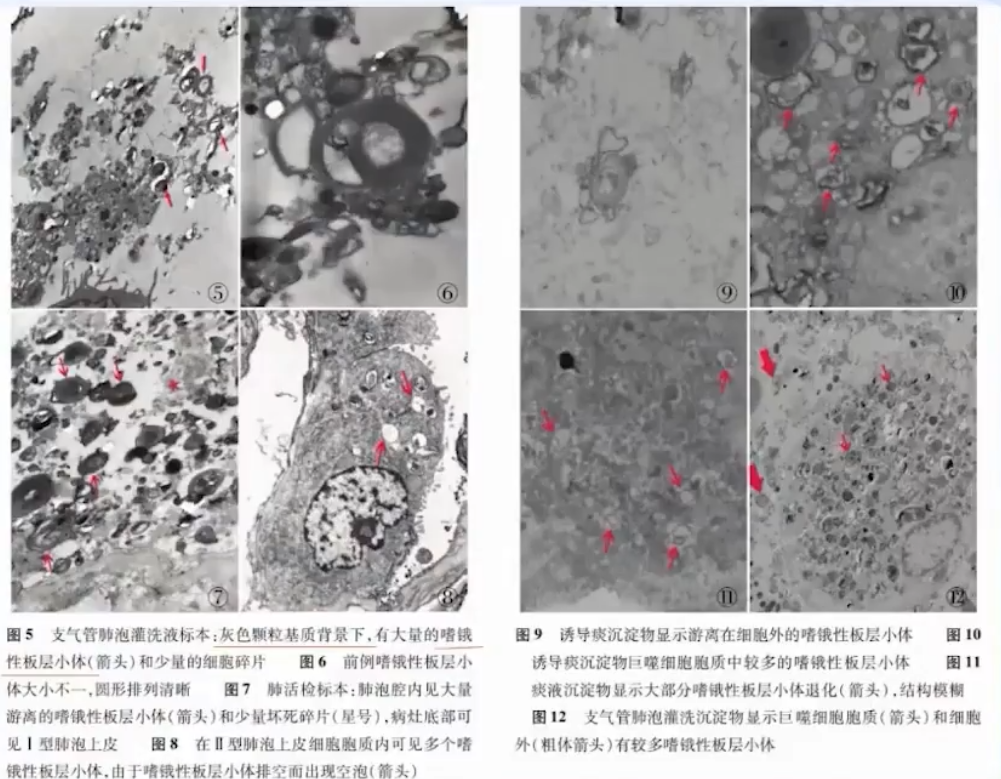
PAP细胞病理诊断标准-分级诊断建议
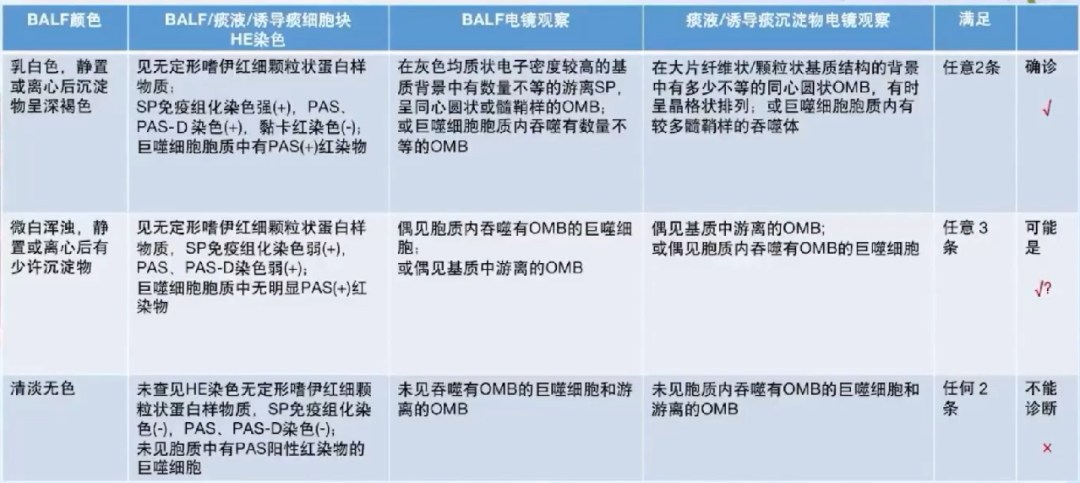
PAP诊断:目前尚无统一诊断标准
临床影像病理诊断(Clinico-Radiologic-Pathologicdiagnosis,CRP)
临床——临床表现无特异性:
无明显症状或程度不等的呼吸困难:
无阳性体征或发绀、肺部啰音和杵状指
病理——组织病理、细胞病理:
光镜、免疫组化及特殊染色
电镜
影像——胸部HRCT:
两肺弥漫磨玻璃影,呈斑片状、地图样分布,可见“铺路石征”、“地图征”
PAP细胞病理诊断流程:

ROSE对PAP的诊断价值小结
-
相较于组织病理(标本的获取、涂片/切片的制备,形态判读,免疫组化及特殊染色效果等),细胞学检查在PAP的诊断中占有重要地位;
-
尚未形成规范性的操作以及受限于实际检测条件,PAP的细胞学分级诊断运用仍然存在一定实现难度;
-
ROSE涂片对于PAP具有快速、直观、有效的诊断价值,拓展及补充了常规细胞学及组织病理学诊断。
鉴别诊断
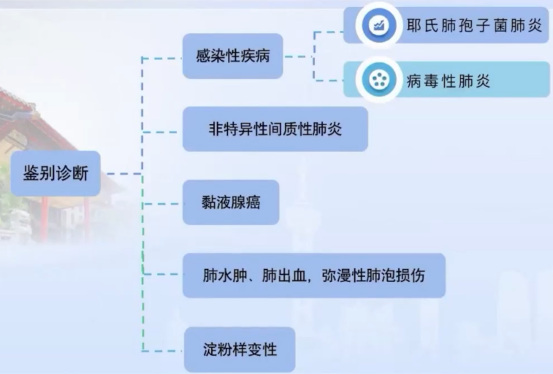
PAP治疗及预后
症状轻微或无临床表现:
可不马上治疗
对症支持治疗:
全肺灌洗(Wholelunglavage,WLL):特发性PAP标准治疗方法,迅速改善肺通气及换气功能
WLL的指征为:①动脉血氧分压≤65mmHg;或②肺泡动脉氧分压差≧40mmHg;或③分流≥10%;或④运动时严重缺氧;或⑤影像学明显进展
经支取管镜行分次肺段灌洗
一般支持治疗:
吸氧、支气管扩张药
抗感染
特异性治疗:
aPAP:抗GM-CSF抗体雾化吸入或皮下注射
继发性PAP:治疗原发病
先天性PAP:肺移植是唯一有效的治疗方法
原发性及继发性PAP:整体预后较好,60%-70%痊愈或明显改善,20%-35%因呼吸衰竭或合并感染死亡
先天性PAP:预后差
小结
1、PAP是以肺泡巨噬细胞功能障碍和肺泡表面活性物质在肺泡腔内积聚为特征的一种少见的弥漫性肺疾病;
肺泡巨噬细胞清除表面活性物质功能下降是PAP发生的重要机制。
2、细胞学检查在PAP的诊断中占重要地位,ROSE对PAP具有快速、直观的诊断价值;
典型病理改变为肺泡腔及组织细胞内充满嗜伊红细颗粒状蛋白性物质,PAS、PAS-D(+),黏液卡红(-)。
3、清除沉积在肺泡腔内的脂蛋白样物质是治疗的目标;
原发性及继发性PAP:整体预后较好。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言