Front. Cell Dev:溶酶体和α-syn之间的双向循环(下)
2022-09-01 brainnew神内神外 brainnew神内神外
brainnews白色世界,专注神经退行性疾病的前沿报道
帕金森病患者的大脑中存在溶酶体功能障碍,而同时α-syn的积累和聚集是PD主要的发病机制。研究显示,α-syn的多种形式会直接或间接干扰溶酶体功能,减少其自身降解,从而加速该蛋白聚集和疾病过程。因此,有理由认为在溶酶体和α-syn之间存在一个循环。来自德国的研究人员在此提供了关于该循环的证据,旨在寻找增强溶酶体功能作为PD治疗的可能性。

上周我们就该文的前半部分Front. Cell Dev:溶酶体和α-syn之间的双向循环(上)做了详细解读,今天我们重点阅读一下有关α-syn的后半部分。
5. 蛋白形式
蛋白形式描述了单个基因编码的所有蛋白质变体,包括翻译后修饰和序列变体等。已有的报道研究了神经退行性疾病中淀粉样蛋白的聚集动力学。
6. α-syn蛋白形式及其对溶酶体功能的影响
α-syn可以被ALP和蛋白酶体途径降解。接下来作者重点研究了α-syn不同蛋白形式的影响。
(1) 磷酸化
磷酸化可发生在丝氨酸、苏氨酸和酪氨酸侧链上,被视为分子开/关切换,但也可能对蛋白质-蛋白质结合特性和亚细胞定位产生影响。在对PD患者脑组织的免疫组化研究中,约90%的α-syn被磷酸化,而在正常人的大脑中,存在α-syn磷酸化但程度较小。在SH-SY5Y细胞中,用氯喹抑制自噬可使磷酸化α-syn水平增加2倍,这表明自噬在α-syn作为磷酸化底物的过程中起着一定作用。因此可以合理地得出结论,自噬途径的缺陷会导致α-syn磷酸化水平升高,并最终聚集。
(2) 氧化
氧化是一种共价修饰,它直接通过活性氧来修饰蛋白质,或者通过氧化应激反应间接的修饰蛋白质。蛋白质的氧化与年龄有关,氧化蛋白质的积累与多种疾病有关。
(3) 多巴胺修饰
PD的主要病理改变是黑质致密部多巴胺能神经元进行性丢失并伴有纹状体多巴胺水平的下降。与未修饰的α-syn相比,暴露于多巴胺的α-syn增加了蛋白质与溶酶体膜的结合。多巴胺修饰的α-syn与家族性PD中突变的A53T的α-syn的行为极为相似。大脑中含有较高的α-syn水平,而黑质致密部具有较高的多巴胺水平,这一现象为黑质致密部对α-syn毒性的特殊脆弱性以及PD腹侧被盖区的相对保留提供了可能的解释。
(4) 聚集
一些研究显示,当细胞开始自噬的早期步骤时,α-syn聚集体得以开始清除。
7. 突变
目前有六个已知的SNCA错义突变直接提示α-syn是PD的致病因子。在这里将回顾一下有关α-syn错义突变对ALP的直接或间接影响以及潜在机制的已知信息。
(1) A53T
α-syn-A53T的错义突变可以导致蛋白通过高亲和力占据溶酶体结合位点来阻止自身降解。
(2) E46K
(3) A30P
8. α-syn蛋白形式:从部分蛋白水解到对溶酶体功能的影响
溶酶体具有从细胞质中去除α-syn的作用,以维持其体内平衡,而α-syn的蛋白形式可调节对ALP系统的有害作用,加剧机能障碍并最终导致疾病。
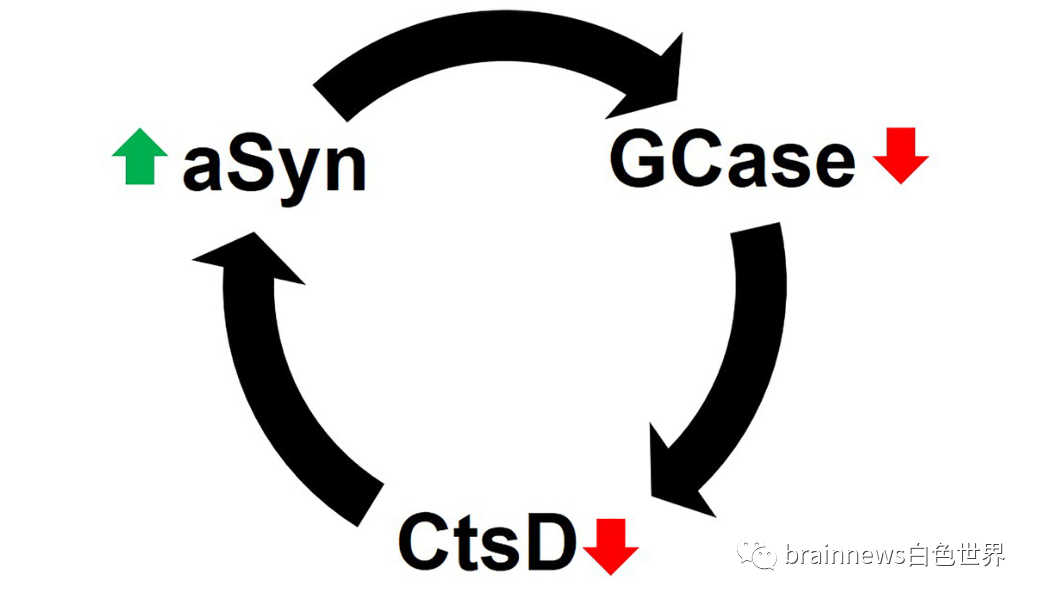
图1:GCase抑制和α-syn积累的相互反馈回路
9. 靶向溶酶体功能的治疗策略
包括α-syn RNAi和溶酶体增强。
10. 总结
总之,已有的报道显示了在溶酶体和α-syn之间存在着显著的双向关系,这一复杂的、不稳定的致病循环会驱动神经退行性疾病的发生发展。
参考文献:
WildburgerNC, Hartke A-S, Schidlitzki A and Richter F (2020) Current Evidence for aBidirectional Loop Between the Lysosome and Alpha-Synuclein Proteoforms. Front.Cell Dev. Biol. 8:598446.
编译作者:十级胖胖 (Brainnews创作团队)
校审: Simon (Brainnews编辑部)
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#CEL#
0
#Cell#
37
#Dev#
47