FDA批准Darzalex(daratumumab)皮下制剂治疗多发性骨髓瘤
FDA近日批准了强生公司的Darzalex(daratumumab)皮下制剂,以治疗成人多发性骨髓瘤。该疗法将以Darzalex Faspro的名称出售。
MedSci原创 - 多发性骨髓瘤,Daratumumab,皮下制剂 - 2020-05-04
FDA或将批准CGRP抑制剂eptinezumab以预防偏头痛
Alder Bio生物制药公司近日宣布已提交研究性CGRP抑制剂eptinezumab的申请,以获得FDA的批准用于预防偏头痛。该制药商表示,如果得到FDA的批准,eptinezumab可能会在明年第一季度上市。
网络 - CGRP抑制剂,Eptinezumab,偏头痛 - 2019-02-24
微生物疗法“春天逼近”,FDA或将批准首款药物上市
微生物组疗法领域今年取得了极大进展。8月11日,Seres Therapeutics宣布其肠道微生物组胶囊SER-109在复发性艰难梭菌感染(Clostridium difficile infecti
医药魔方 - 微生物疗法 - 2020-09-23
CRISPR编辑的iPSC衍生细胞疗法FT538:FDA已批准IND
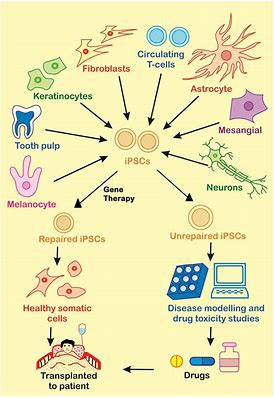
FT538是一种自然杀伤细胞(NK)癌症免疫疗法,其衍生自诱导多能干细胞(iPSC),且经过工程改造。
MedSci原创 - iPSCs,CRISPR编辑,FT538 - 2020-05-21
美国FDA已批准抗体-药物偶联物(ADC)OBI-999的IND
OBI制药公司近日宣布,美国FDA已批准其抗体-药物偶联物(ADC)OBI-999的研究性新药申请(IND),将进行I/II期临床研究。
MedSci原创 - 抗体-药物偶联物(ADC),OBI-999,FDA - 2019-09-04
RedHill Biopharma宣布FDA批准Talicia用于治疗成人幽门螺旋杆菌感染
Talicia是获批的唯一基于利福布汀治疗幽门螺杆菌感染的疗法,旨在解决幽门螺杆菌对当前基于克拉霉素的护理标准疗法的高耐药性。据估计,幽门螺杆菌对克拉霉素的耐药性在2009-2013年之间翻了一番以上。
MedSci原创 - RedHill,Biopharma,FDA批准,Talicia,幽门螺杆菌感染 - 2019-11-04
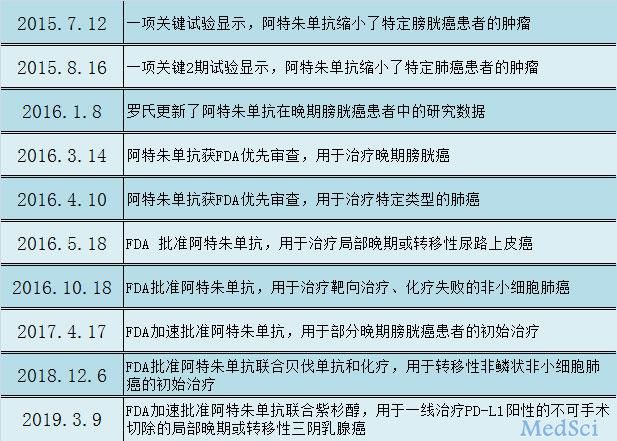
FDA批准首个针对三阴性乳腺癌的免疫治疗方案
近日,FDA加速批准阿特珠单抗(Atezolizumab,商品名:Tecentriq)联合nab-紫杉醇(Abraxane),用于一线治疗无法切除的局部晚期或转移性PD-L1阳性三阴性乳腺癌。阿特珠单抗是FDA批准的第一个PD-L1抑制剂,也成为首个针对乳腺癌的免疫治疗方案。纽约西奈山乳腺癌专家艾米·铁斯登博士称,这是个“非常令人振奋的消息”。
汉鼎好医友 - 三阴性乳腺癌 - 2019-03-17
FDA批准一新药用于治疗慢阻肺气道阻塞
美国 FDA 批准了一种新型吸入性复方支气管扩张剂Utibron Neohaler,用以长期维持治疗慢性阻塞性肺疾病患者的气道阻塞症状。
MedSci原创 - FDA,慢阻肺 - 2015-11-26
2014年FDA批准新药 抗肿瘤领域有9只药物获批
2014年美国FDA药品评价和研究中心(CDER)批准了41个新分子实体(NME)和生物制品许可申请(BLA)(不包括FDA生物制品评价与研究中心(CBER)批准的疫苗、血液制品等产品),高于2013作为FDA批准药物丰硕的一年,其中抗肿瘤领域有9只药物获批,成为获得批准药物最多的领域。其次,4只糖尿病药物,4只新型抗菌药物,其中新型抗菌药物获
FDA - 基因治疗 - 2015-01-05
美国FDA批准首个生物仿制药Zarxio(非格司亭-sndz)上市
美国FDA今天批准了美国有史以来第一个真正意义上的生物仿制药Zarxio(通用名:filgrastim-sndz)上市。Neupogen最早在1991年获得FDA批准用于治疗5种情况的中性粒细胞减少(接受骨髓抑制剂化疗的、接受诱导或巩固化疗的急性髓性白血病、接受骨髓移植的癌症患者、接受自体外周血
美中药源 - 药械,生物仿制药 - 2015-03-09
FDA批准阿斯利康痛风药物Lesinurad治疗痛风相关高尿酸血症
FDA批准阿斯利康痛风药物 Lesinurad(Zurampic) (200mg/d)与黄嘌呤氧化酶抑制剂 (XOI)一起用于治疗痛风相关高尿酸血症。Lesinurad 可尿酸的排泄,减少其生成。
MedSci原创 - 痛风,尿酸,lesinurad - 2015-12-23
FDA批准缓释艾塞那肽获准抗II型糖尿病
1月27日,美国食品和药品监督管理局(FDA)批准了艾塞那肽注射液每周一次缓释剂型的上市申请,2型糖尿病(T2CD)成人在饮食和锻炼基础上,可使用此制剂改善血糖控制。
MedSci原创 - 糖尿病,艾塞那肽 - 2012-02-06
FDA拒绝批准奈比洛尔/缬沙坦组合治疗高血压
美国食品药物监督管理局(FDA)发布了一个完整的回复信(CRL),拒绝批准固定剂量复方制剂的奈比洛尔/缬沙坦组合片剂用于治疗高血压。一个新的药物不批准时,FDA发布完整回复信。美国食品药品监督管理局的顾问团队以6:4的投票否决了固定剂量复方制剂的组合药剂用于高血压的治
MedSci原创 - FDA,药械,高血压 - 2015-01-04
FDA批准通过索林集团植入式心脏远程监控器SmartVIew
本周,索林集团宣布,FDA已经批准了其为植入有心脏节律管理装置的患者设计的远程监控应用装置SmartView 。
丁香园 - FDA,索林集团,植入,心脏,SmartVIew - 2013-05-16
FDA批准雅培HCV基因型检测试剂盒上市
2013年6月20日,美国食品与药物管理局(FDA)批准了可检测到患者携带的丙型肝炎病毒(HCV)基因型的试剂盒(Abbott RealTime HCV Genotype
MedSci原创 - 丙肝,HCV,基因型,FDA,雅培 - 2013-07-13
为您找到相关结果约500个