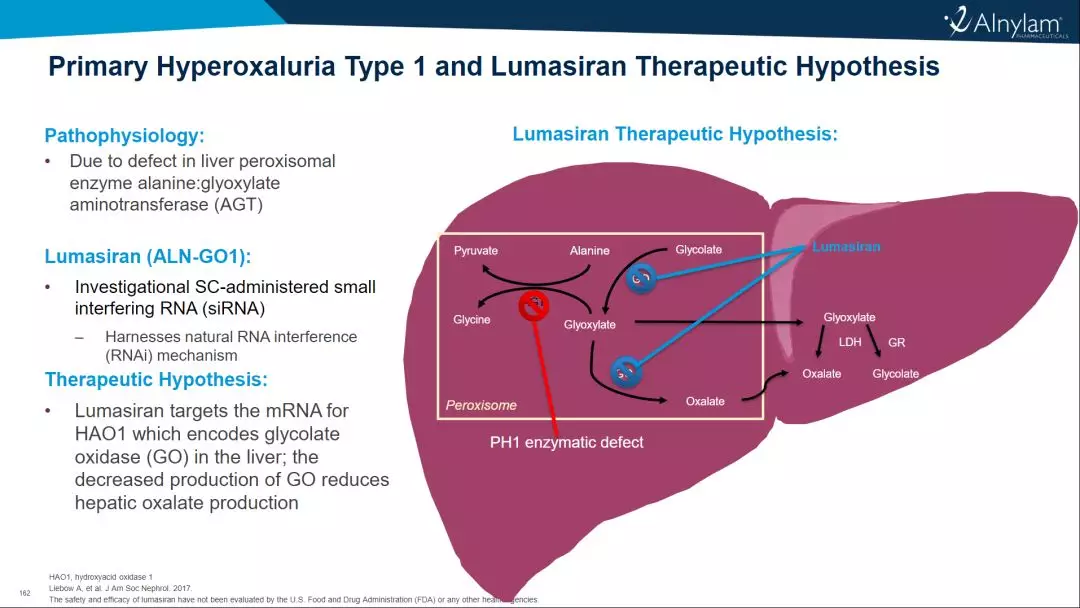
FDA为Alnylam的RNAi疗法Lumasiran授予优先审查,用于治疗1型原发性高草酸尿症
Lumasiran是靶向羟基酸氧化酶1(HAO1)、可按季度皮下给药的的RNAi治疗药物。
MedSci原创 - 优先审查,1型原发性高草酸尿症(PH1),RNAi疗法Lumasiran - 2020-06-03
全球第三款RNAi疗法lumasiran即将获批,治疗罕见肝病——1型原发性高草酸尿症
20余年历程,RNAi疗法的时代正在逐步到来。最近,
MedSci - RNAi疗法,原发性高草酸尿症,Lumasiran - 2020-10-27
Science Advances:北理工黄渊余团队开发新型脂质纳米颗粒,递送RNAi疗法,治疗和预防心血管疾病
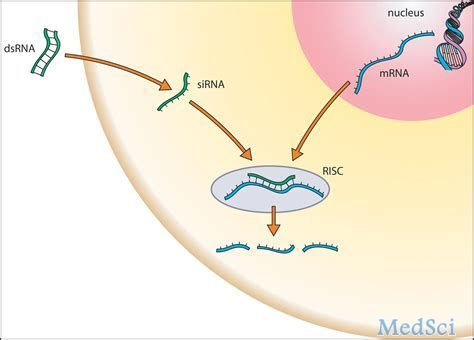
目前,抗高血脂药物主要包括小分子药和抗体药,然而他们在使用过程中存在潜在的有害影响,且治疗效率低,严重阻碍了治疗进展。幸运的是,小干扰RNA(siRNA)由于具有开发时间短、特异性高、高度可预测等优势
“生物世界”公众号 - RNA疗法,新型脂质纳米颗粒 - 2022-02-22
RNAi疗法Lumasiran治疗高草酸尿症,6个月患者恢复到正常水平
lumasiran治疗组,84%的患者草酸尿排泄达到了正常化或接近正常化的水平,而安慰剂组没有一人实现该目标。
MedSci原创 - 1型原发性高草酸尿症(PH1),RNAi疗法Lumasiran,Lumasiran,Alnylam Pharmaceuticals - 2020-06-13
ERA-EDTA 2020:RNAi疗法公司Alnylam再发力!Lumasiran治疗1型原发性高草酸尿症III期临床成功
Lumasiran达到ILLUMINATE-A的主要终点,相对于安慰剂而言,草酸尿的平均减少量为53.5%
MedSci原创 - RNAi疗法,1型原发性高草酸尿症(PH1),Lumasiran - 2020-06-08
Genet Med:lumasiran治疗原发性1型高草酸尿症的3期试验:一种新的婴幼儿RNAi疗法
原发性高草酸尿症1型(PH1)是一种罕见的进行性常染色体隐性遗传病,其特征是由AGXT编码的肝过氧化物酶丙氨酸-乙醛酸转氨酶缺乏引起的肝草酸盐生成增加。
MedSci原创 - 原发性1型高草酸尿症 - 2022-01-30
RNAi疗法的新靶点:V122I是一种普遍存在的致病性转甲状腺素(TTR)突变
领先的RNAi治疗公司Alnylam Pharmaceuticals近日公布了英国生物银行分析的最新结果,这是一项针对英国约500,000人的遗传、物理和健康数据的前瞻性队列研究,证明了转甲状腺素蛋白(
MedSci原创 - 致病性转甲状腺素,RNAi疗法,V122I - 2019-09-15
FDA批准lumasiran治疗原发性高草酸尿症1型,Alnylam的RNAi帝国再下一城!
近日,FDA批准了Alnylam的RNAi药物lumasiran的新适应症,通过降低血浆中的草酸盐水平来治疗原发性高草酸尿症1型(又称Ph1)这种罕见的遗传性疾病。主要基于一系列临床试验结果,见:NE
会会药咖 - FDA,RNAi药物,Lumasiran,原发性高草酸尿症1型 - 2022-10-11
2018十大RNA疗法公司,第一名不是Moderna?
近日,国外生物技术网站GEN发布了2018年十大RNA疗法公司榜单,包括五家上市公司和五家非上市公司。上市公司的排名以收入计,非上市公司的排名以募集资金(含融资及合作)计。
医药魔方 - 2018,RNA - 2018-12-20
FDA批准vutrisiran治疗成人遗传性转甲状腺素蛋白淀粉样变性伴多发性神经病(hATTR-PN),这是第5款siRNA药物
近日,全球领先的 RNAi 疗法公司
bioSeedin柏思荟 - 遗传性转甲状腺素蛋白淀粉样变性 - 2022-06-17
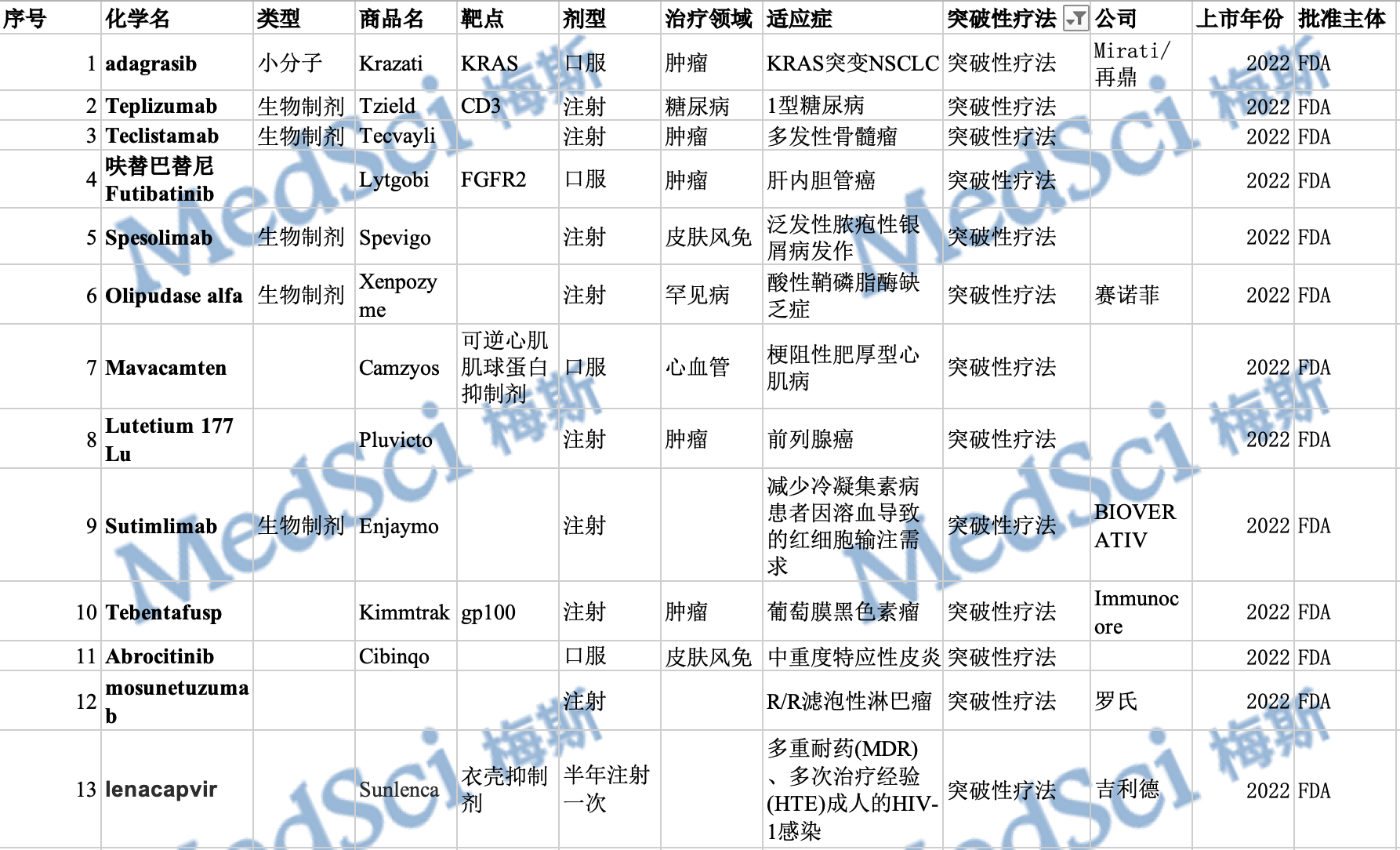
梅斯盘点:FDA在2022年度批准的创新药(上)
2022年即将结束,截至今年12月30日,美国FDA的药物评估和研究中心(CDER)已经批准了37款创新药。FDA的生物制品评估和研究中心(CBER)也批准了至少15项生物制品许可申请(BLA)。虽然
MedSci原创 - FDA,创新药物,创新药 - 2023-01-01
勃林格殷格翰通过与Dicerna的研究合作取得第二个肝病靶点的期权
勃林格殷格翰与开发研究性RNA干扰(RNAi)疗法的领导者之一Dicerna Pharmaceuticals(NASDAQ: DRNA)近日宣布,根据双方的研究合作及许可协议规定,勃林格殷格翰已经获得了第二个肝病靶点的独家权利此项合作签订于2017年10月,目的是为了探索并开发可用于慢性肝病治疗的创新GalXC™ RNAi疗法,最初的重点为非酒精性脂肪性肝炎(NASH),这是一种目前还没有获批疗
美通社 - 勃林格殷格翰,肝炎 - 2019-01-10
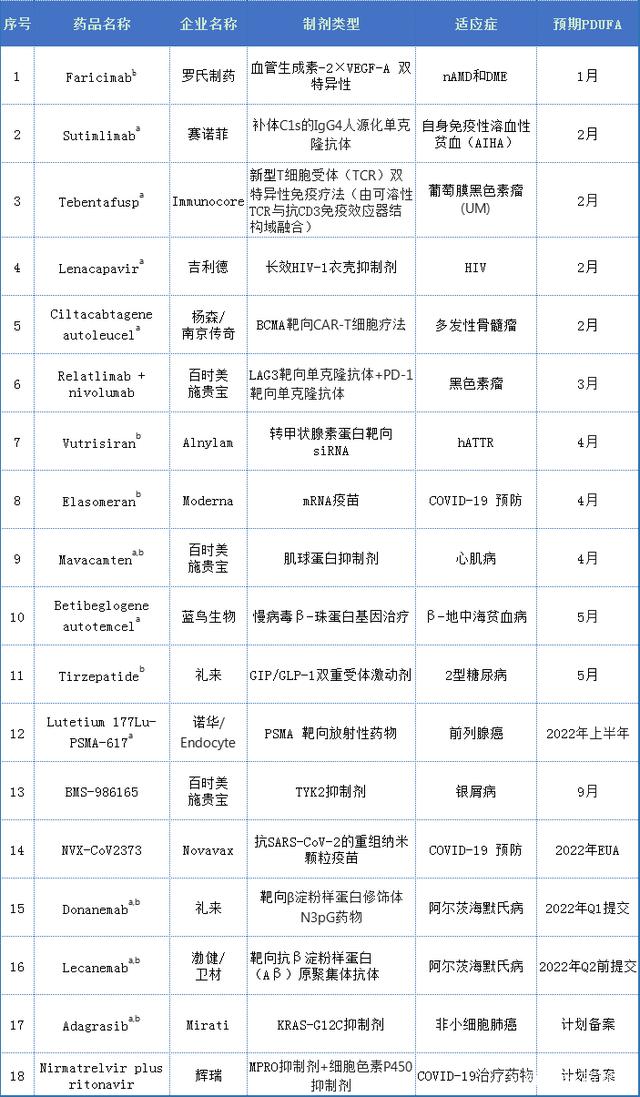
2022年FDA有望批准的18款创新疗法
近日,FDA发布2021年药物审评审批报告,获批50种新药,低于2020年53种,包括具有里程碑意义的mRNA疫苗与两款CAR-T细胞疗法、多款ACD新药、颇具有争议的阿兹海默症Aduhelm....
药智网 - FDA - 2022-01-16
Arrowhead治疗乙肝RNA药物ARC-520临床二期研究再遇阻碍
总部位于加利福尼亚州帕萨迪纳市的生物技术公司Arrowhead是一家以开发RNAi疗法为核心的生物医药公司。众所周知,RNAi被很多人认为是充满不确定性因素的研究领域,机遇与挑战并存。Arrowhead公司现有三种RNAi药物正处于研发过程,其中ARC-520是走的最远的一个项目。
生物谷 - 乙肝,RNA,药物 - 2015-01-15
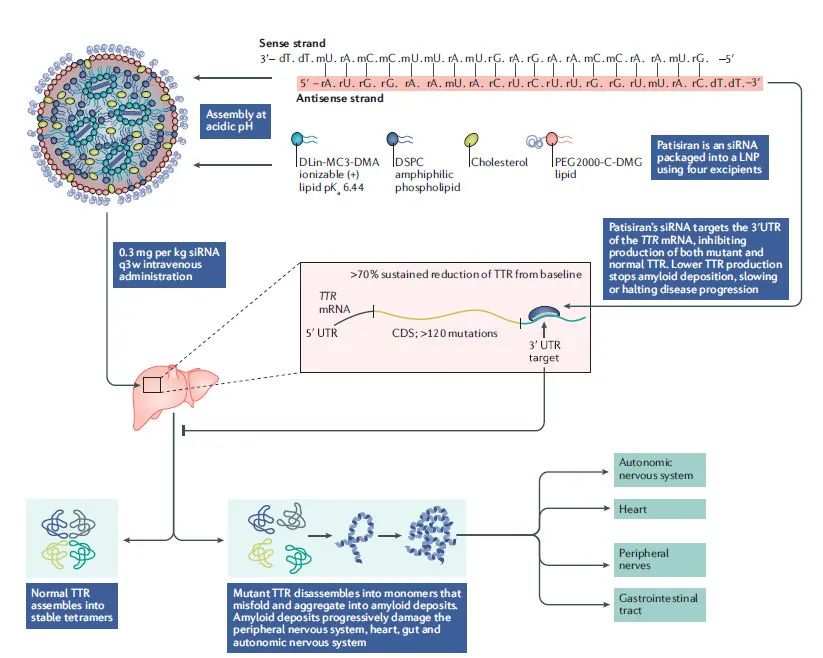
FDA批准首个基于诺奖技术的新疗法
8月10日,美国FDA宣布批准第一款基于RNA干扰(RNAi)技术的治疗药物——patisiran,适用于一种损伤心脏、神经功能的罕见病。其中,RNAi技术可以针对性沉默与疾病相关的特定基因,从而阻止致病蛋白的表达。
生物探索 - FDA,RNAi,罕见病 - 2018-08-14
为您找到相关结果约152个