全球第三款RNAi药物出炉,百亿美金市场谁主沉浮?
2020年,全球第三款RNAi药物获批上市,跟前两款一样,又是出自基因药物先锋公司Alnylam。
亿欧 - RNAi药物,百亿美金,谁主沉浮 - 2020-12-05
辟谣!“美国公司宣布人类已经攻克癌症”背后到底是个什么鬼?!
号外文讲的是美国阿尔尼拉姆生物技术公司(Alnylam Pharmaceuticals)利用他们的RNAi技术的ALN-VSP药物能够组织肿瘤生长,并宣称“假以时日,这种药物甚至有可能治愈一切疾病”。
E药经理人 - 癌症,RNAi - 2015-06-10
突破性RNAi疗法早期数据显著,即将开展3期临床
领先的RNA干扰 (RNAi)公司Alnylam已加紧对超罕见卟啉症(ultrarare porphyria diseases)候选药物的研发。日前,在法国波尔多举行的国际卟啉化合物和卟啉症大会(International Congress on Porphyrins and Porphyrias, ICPP)上,Alnylam报道了givosiran
药明康德 - RNAi疗法,血紫质病,卟啉症 - 2017-06-28
20年等待!FDA批准首个基于诺奖技术的新疗法
8月10日,美国FDA宣布批准第一款基于RNA干扰(RNAi)技术的治疗药物——patisiran,适用于一种损伤心脏、神经功能的罕见病。其中,RNAi技术可以针对性沉默与疾病相关的特定基因,从而阻止致病蛋白的表达。
生物探索 - FDA,RNAi,罕见病 - 2018-08-14
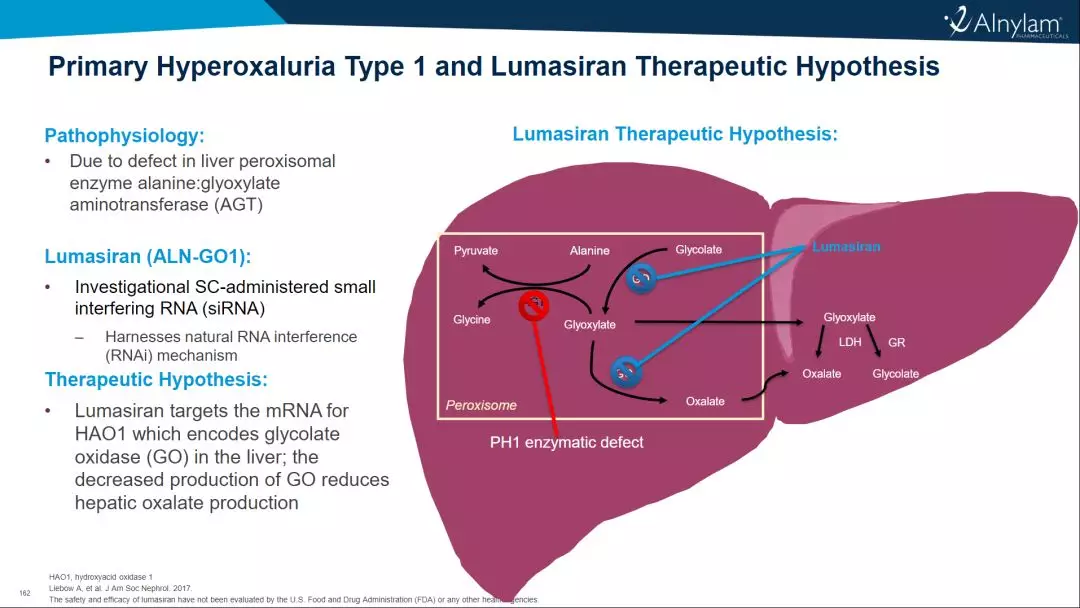
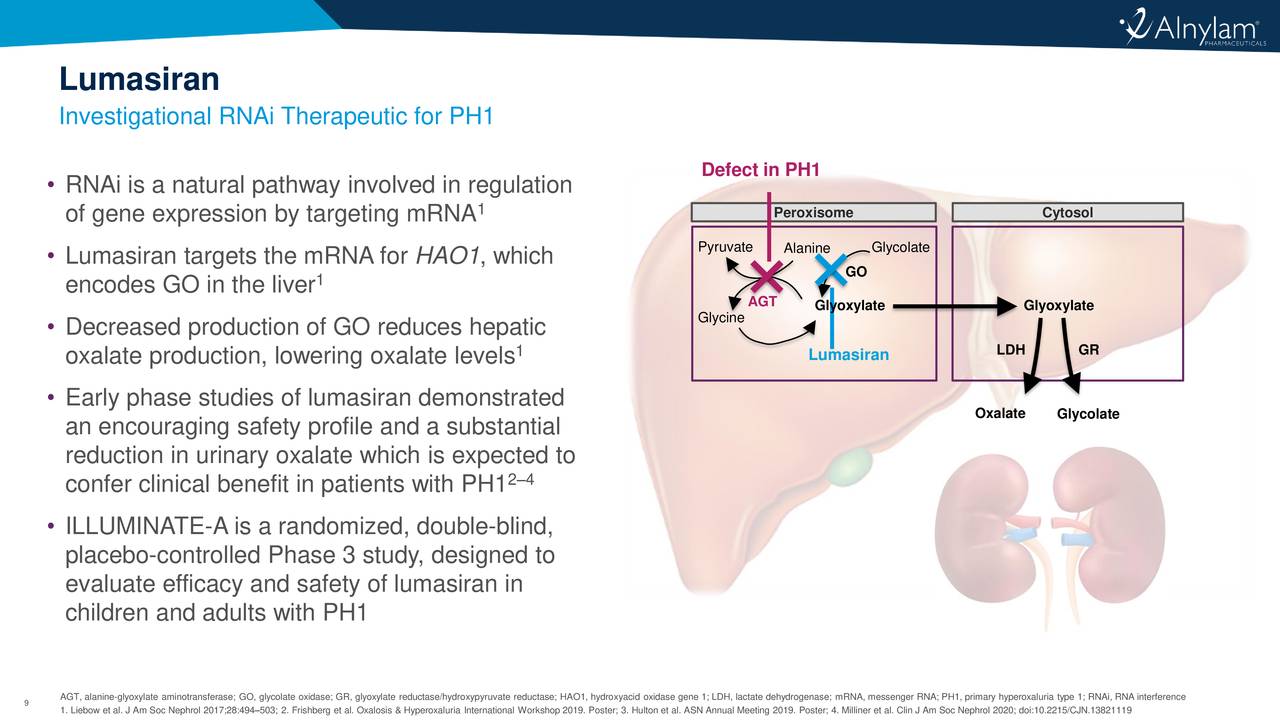
全球第三款RNAi疗法lumasiran即将获批,治疗罕见肝病——1型原发性高草酸尿症
20余年历程,RNAi疗法的时代正在逐步到来。最近,
MedSci - RNAi疗法,原发性高草酸尿症,Lumasiran - 2020-10-27
RNAi疗法lumasiran:获得英国MHRA支持治疗1型原发性高草酸尿症
Lumasiran是通过皮下给药、靶向羟基酸氧化酶1(HAO1)的RNAi治疗药物。
MedSci原创 - 1型原发性高草酸尿症(PH1),RNAi疗法Lumasiran - 2020-07-16
FDA批准vutrisiran治疗成人遗传性转甲状腺素蛋白淀粉样变性伴多发性神经病(hATTR-PN),这是第5款siRNA药物
近日,全球领先的 RNAi 疗法公司
bioSeedin柏思荟 - 遗传性转甲状腺素蛋白淀粉样变性 - 2022-06-17
Alynlam的RNAi药物lumasiran治疗原发性高草酸尿症,完成向欧盟和美国的申请
如果获得批准,lumasiran将成为1型原发性高草酸尿症(PH1)患者的首个治疗药物。
MedSci原创 - Alnylam,1型原发性高草酸尿症(PH1),RNAi药物lumasiran - 2020-04-08
FDA解除对赛诺菲血友病药物的临床控制
美国食品和药物管理局在9月份取消了对该方案的临床控制权之后,赛诺菲和Alnylam的血友病治疗药物fitusiran面临的一个主要障碍已经被消除。
MedSci原创 - 赛诺菲,血友病药物 - 2017-12-18
RNAi疗法lumasiran获得欧盟批准治疗1型原发性高草酸尿症
Alnylam Pharmaceuticals宣布,欧盟委员会批准了其RNAi治疗药物Oxlumo(lumasiran)用于治疗1型原发性高草酸尿症(PH1)。
MedSci原创 - 1型原发性高草酸尿症(PH1),RNAi疗法Lumasiran - 2020-11-20
替代凝血促进剂(ACPs)领跑基因疗法,促进血友病市场增长
GlobalData最新的分析报告显示,罗氏公司的Hemlibra和Alnylam公司的后期候选药物fitusiran可能会在扩大血友病市场中占据比基因疗法更大的份额。
MedSci原创 - 替代凝血促进剂,ACPs,基因疗法,血友病 - 2019-07-17
2018十大RNA疗法公司,第一名不是Moderna?
近日,国外生物技术网站GEN发布了2018年十大RNA疗法公司榜单,包括五家上市公司和五家非上市公司。上市公司的排名以收入计,非上市公司的排名以募集资金(含融资及合作)计。
医药魔方 - 2018,RNA - 2018-12-20
FDA批准首款RNAi药物Onpattro用于治疗hATTR
日前,美国FDA批准了一项具有里程碑意义的基因疗法,针对罕见病遗传性转甲状腺素蛋白淀粉样变性或hATTR(一种神经病变或神经损伤)的基因疗法。这也是全球第一例依据诺贝尔奖成果RNA干扰技术开发的药物Onpattro,该药作用机理通过使致病基因“沉默”,进而从根本上治愈该罕见遗传疾病。也是FDA批准的首款小干扰RNA(siRNA)药物。hATTR影响了全球约50000人,是一种罕见、使人衰弱且常
MedSci原创 - FDA,药物,RNAi - 2018-08-12
Lancet:RNAi基因治疗新药ALN-PCS明显降低患者胆固醇水平(临床I期研究)
由Alnylam 公司研发,在英国盖氏医院研究人员与美国同行一起,在英国新一期《柳叶刀》杂志上报告说,一种被称为“ALN-PCS”的新药,可通过干扰核糖核酸来抑制PCSK9 基因的表达,使身体清除有害胆固醇的能力恢复正常
新华网 - ALN-PCS,基因治疗,他汀 - 2013-10-11
比利时急性肝卟啉症专家共识声明 2021
急性肝卟啉症 (AHP) 是一组四种不同的罕见至极罕见、严重使人衰弱、有时甚至致命的疾病,它们严重影响患者的生活:5-氨基乙酰丙酸 (ALA) 脱水酶缺乏性卟啉症 (ADP)、急性间歇性卟啉症 ( A
Acta Clin Belg . 2021 Aug 7;1-7. - 急性肝卟啉症,肝卟啉症 - 2021-08-12
为您找到相关结果约68个